Температура плавления крахмал: Температура клейстеризации — Справочник химика 21
Температура клейстеризации — Справочник химика 21
Крахмал, амилоза, амилопектин нерастворимы в холодной воде, спирте, эфире. При нагревании в воде зерна крахмала разрушаются и образуются клейстеры. Сначала крахмальные зерна в воде незначительно обратимо набухают, затем при повышении температуры — сильно и необратимо набухают, увеличиваются в объеме в сотни раз, повышают вязкость растворов (разрыв водородных связей и гидратация макромолекул), на последней стадии — растворимые полисахариды переходят-в раствор, зерна теряют форму, могут разрушаться и суспендировать в раствор. При этом вязкость клейстера сильно увеличивается. Интервал температуры клейстеризации различных пищевых крахмалов показан в табл. 13. [c.32]Температура клейстеризации зависит в основном от природы крахмала, величины гранул, наличия в воде солей и от других факторов. Так как в любом крахмале имеются гранулы различного размера, то правильно говорить не о точке клейстеризации, а о температурном интервале (начала и конца) клейстеризации.
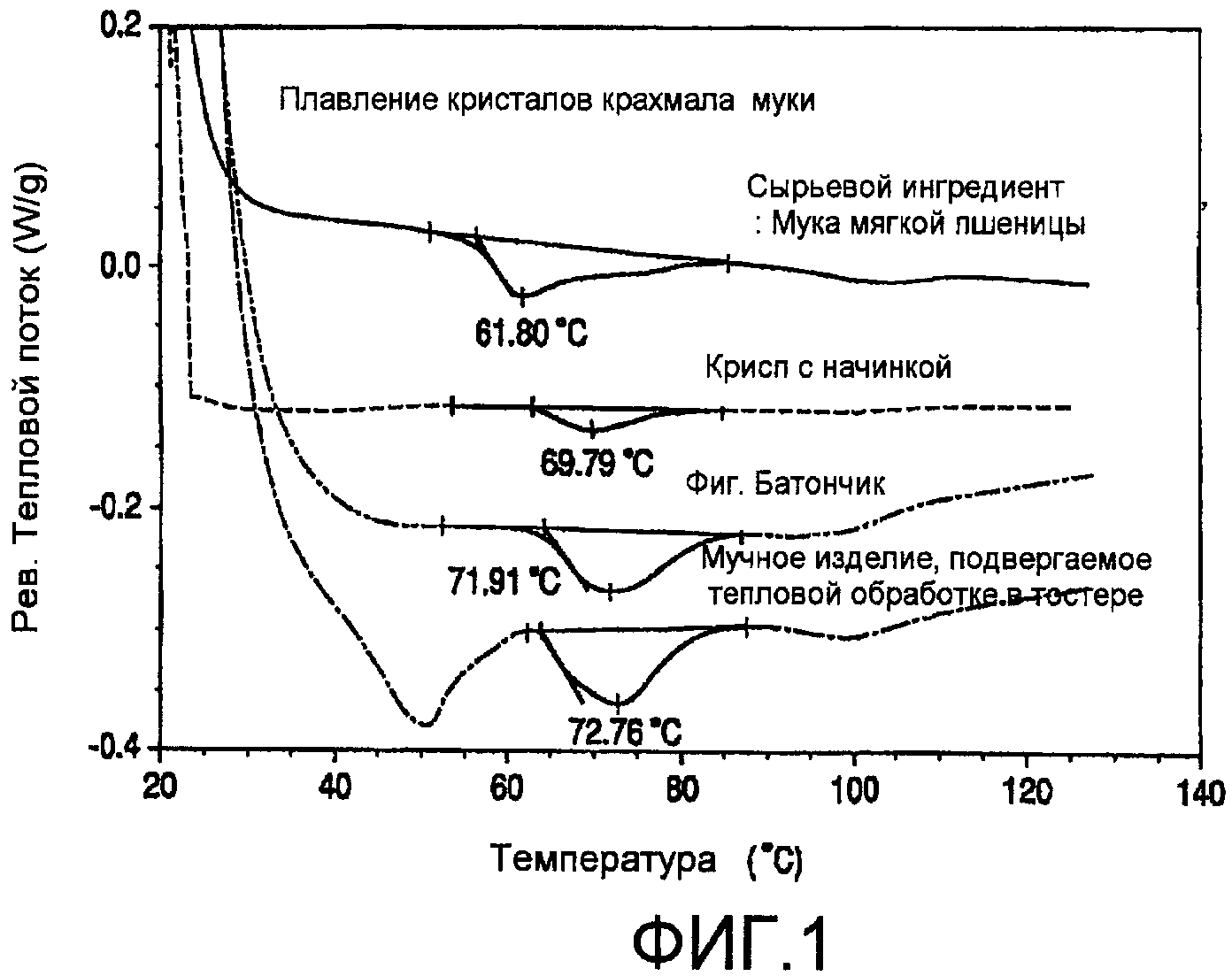
Крахмал очень чувствителен даже к весьма незначительным примесям, растворенным в воде. Это убедительно показано в исследованиях В. И. Назарова. Так, например, некоторые электролиты способны сильно понизить температуру клейстеризации крахмала. На свойства крахмала оказывают влияние и неэлектролиты, например сахар. [c.417]
Крахмал картофеля, как и крахмал других видов растений, состоит из амилозы и амилопектина. В крахмале клубней количество амилозы обычно достигает 20—25%, а амилопектина 75— 80%. Молекулярный вес амилозы составляет 180 тыс., амилопектина 1—6 млн. В крахмале найдено 50—100 мг% фосфора, небольшое количество липидов и некоторых других соединений. Фосфор в крахмале связан с амилопектином. Температура клейстеризации картофельного крахмала 55—65 °. [c.416]
В табл. 27 указана температура клейстеризации различных видов крахмала (в градусах С), обычно приводимая в литературных источниках. [c.135]
[c.135]
Крахмал — белый порошок, напоминающий пшеничную муку ( картофельная мука ) нерастворим в холодной воде. При нагревании с водой набухает и образует клейстер. Для каждого вида крахмала известна своя температура клейстеризации для картофельного она равна 59—62° для рисового 59—61° для [c.294]
Влияние щелочной среды на температуру клейстеризации крахмала [c.137]
В нерастворенных гранулах крахмала при рассмотрении под микроскопом хорошо видны канальцы и повреждения поверхности, что является результатом действия амилаз (рис. 50). Размер гранул несколько уменьшается, повышается содержание амилозы, внешние цепи амилопектина укорачиваются. Температура клейстеризации возрастает приблизительно на 4°С, а вязкость клейстера, наоборот, понижается.
На последней стадии растворимые полисахариды извлекаются водой, зерна крахмала теряют форму, становятся прозрачными и склеиваются, образуя крахмальный клейстер. Температура клейстеризации зависит от вида крахмала, Для картофельного крахмала она составляет 55—65° С, кукурузного 64— 7ГС, пшеничного 60—80°С. [c.225]
Температура клейстеризации зависит от вида крахмала, Для картофельного крахмала она составляет 55—65° С, кукурузного 64— 7ГС, пшеничного 60—80°С. [c.225]
Температура клейстеризации зависит от культуры сырья, величины зерен крахмала, концентрации его суспензии и других факторов. Поэтому клейстеризация крахмала протекает в температурном интервале, который лежит у картофельного крахмала от 55 до 65°, у ржаного — от 45 до 60°, у ячменного — от 50 до 65 , у овсяного — от 50 до 75° и у кукурузного—от 50 до 115°. Как правило, крупные зерна разрушаются раньше мелких. Температура клейстеризации крахмалов одной и той же культуры, но выделенных из различных образцов зерна, может колебаться в пределах 3—7°. Температура клейстеризации крахмала муки иа 4—6° ниже температуры клейстеризации чистого крахмала соответствующей одноименной культуры. [c.90]
Клейстеризация крахмала протекает постепенно и не имеет явно выраженных границ.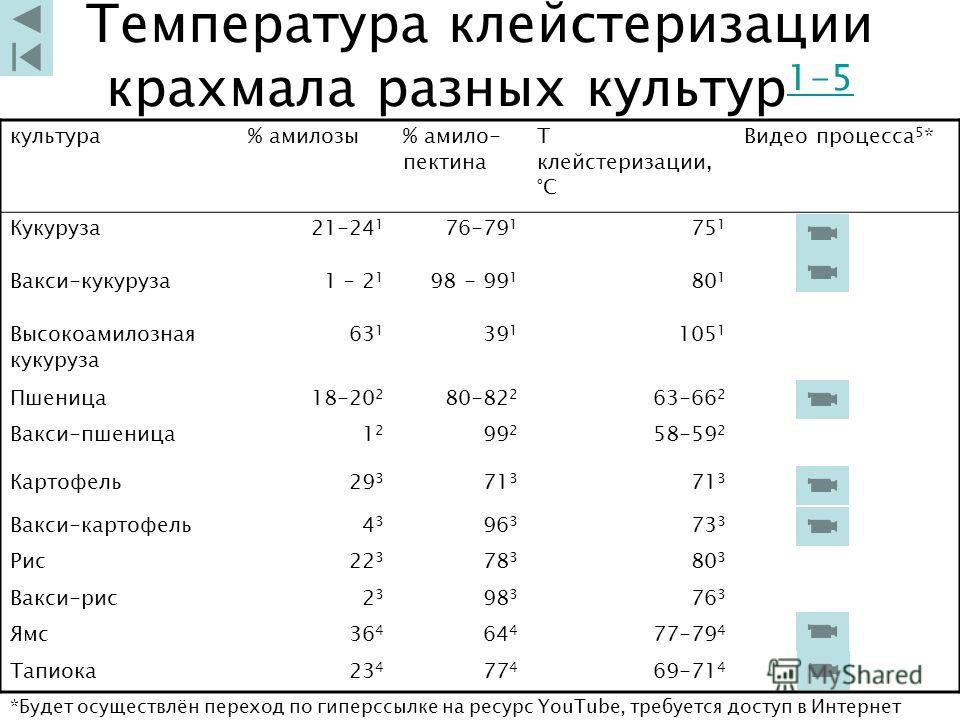 Поэтому разные исследователи по-раз-ному определяют температуру клейстеризации. [c.135]
Поэтому разные исследователи по-раз-ному определяют температуру клейстеризации. [c.135]
О температуре клейстеризации мы судили по быстроте оседания крахмала и по объему образовавшегося слоя чистой воды. [c.143]
Полученные нами при исследовании результаты влияния концентрации едкого натра на температуру клейстеризации крахмала (в градусах С) приведены в табл. 43.
Для получения крахмального клея кислотной обработки раствор соляной кислоты требуемой концентрации нагревают до температуры, которая на 5—10° С ниже температуры клейстеризации крахмала, и всыпают при энергичном помешивании крахмал. Смесь нагревают при непрерывном помешивании, пока не наступит клейстеризация крахмала и не появятся внешние признаки готовности клея. По окончании процесса заварки клей немедленно нейтрализуют едким натром до нейтральной реакции. [c.169]
Процесс обработки крахмала хлорной известью заключается в следующем.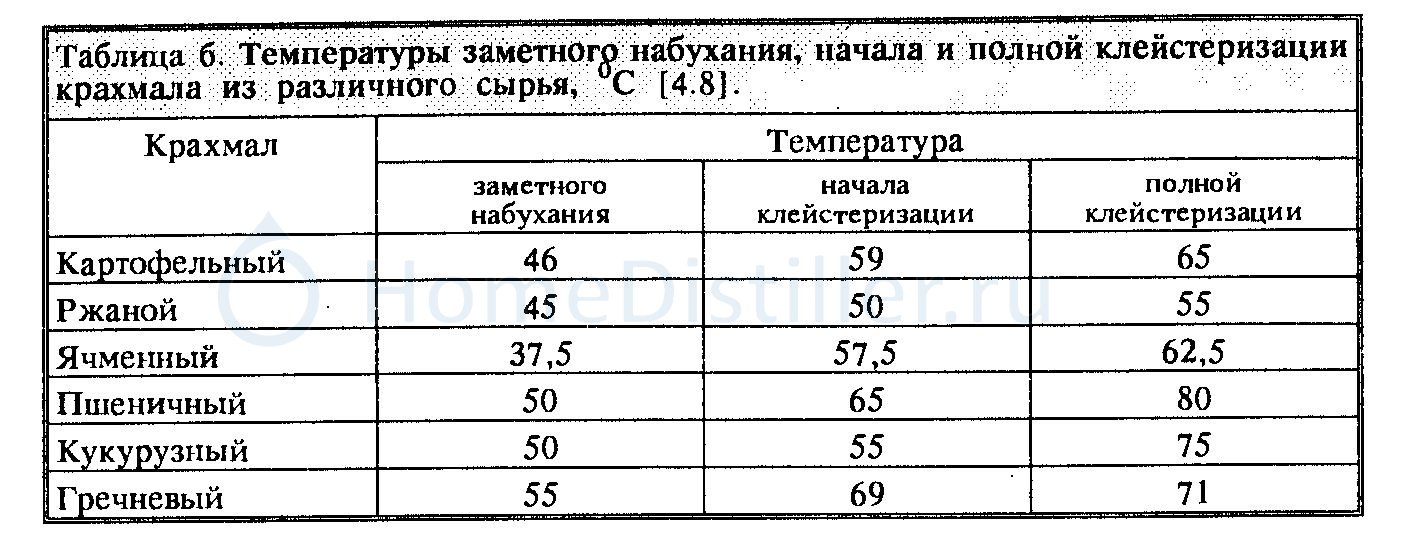 В раствор извести с рассчитанным количеством активного хлора всыпают крахмал и смесь медленно нагревают при постоянном помешивании. При температуре на 2—3° С ниже температуры клейстеризации крахмала наступает загустевание [c.180]
В раствор извести с рассчитанным количеством активного хлора всыпают крахмал и смесь медленно нагревают при постоянном помешивании. При температуре на 2—3° С ниже температуры клейстеризации крахмала наступает загустевание [c.180]
Способ производства сухого окисленного крахмала основан на том, что раствор хлорной извести окисляет крахмал при комнатной температуре, лежащей ниже температуры клейстеризации крахмала. При этом значительного набухания крахмальных зерен не происходит и окисленный крахмал легко отфильтровать и отмыть от образовавшегося в результате окисления хлористого кальция. [c.183]
В фармацевтической практике разрешено к использованию четыре вида крахмала пшеничный, кукурузный, рисовый и картофельный. Это белый нежный порошок без запаха и вкуса или куски неправильной формы, которые при растирании легко рассыпаются в порошок. Нерастворимы в холодной воде, спирте, эфире. Различные сорта крахмала имеют разную температуру клейстеризации. Наименьшая — у картофельного (55-60°С) и наибольшая — у рисового (70-80°С). [c.267]
Наименьшая — у картофельного (55-60°С) и наибольшая — у рисового (70-80°С). [c.267]
Подваривание замеса. При переработке зерна процессу подваривания предшествует смешивание крупки с водой. Оно должно вестись так, чтобы замес был однородным и не содержал комочков теста ( галушек ), которые плохо развариваются и вызывают увеличение потерь сбраживаемых веществ с нерастворенным крахмалом. Тщательность проведения этой операции определяется конструкцией смесителей, частотой вращения мешалки и температурой воды в месте смешения, которая не должна превышать 50°С (быть ниже температуры клейстеризации).
Стадия разваривания крахмалосодержащего сырья паром повышенного давления может быть заменена гидроферментативной обработкой замеса с помощью бактериальной а-амилазы при температурах клейстеризации крахмала 60…90 °С. [c.80]
Б щелочной среде температура к.1ейстернзации крахмала значительно понижается. В.лияпие нюлочной среды на температуру клейстеризации ку)ахмала (по Самецу) показано к табл.
Если воздействовать на крахмал концентрированными растворами щелочей, клейстеризация происходит уже при комнатной температуре. Клейстеризация в присутствии щелочей сопровождается расиадепием—дезагрегацией—крахмальных зерен. Нрп нагревании крахмала с водой выше температуры клейстеризации также происходит частичная дезагрегация крахмального зерна на более мелкие частицы. [c.137]
Действие щелочей на крахмал в первую очередь выражается в тол , что температура клейстеризации крахмала понижается и при достаточной концентрации щелочи крахмал клейстеризуется ужо при комнатной температуре. [c.156]
В холодной воде, так же как в спирте и эфире, ни амилоза, ни ами-лопектин не растворяются. В горячей воде крахмальные зерна набухают и разрушаются, так как происходит разрыв некоторых связей и гидратация макромолекул. Амилоза переходит в раствор, а амилопек-тин клейстеризуется, т.
В общем, из проделанных нами опытов следует, что щелочную обработку крахмала можно рекомендовать для улучшения качества крахмального клейстера. Так, кукурузный крахмал, клейстери-зующийся при относительно высокой (82—83° С) температуре, быстро загустевающий и с трудом поддающийся намазке, а также подверженный быстрому синерезису, теряет при щелочной обработке эти недостатки понижается температура клейстеризации, вязкость и скорость синерезиса, появляется возможность заваривать крахмал обычным способом, т. е. путем приливания к крахмальной суспензпи горячей воды. Это позволяет применять для переплетных работ кукурузный крахмал, которым до настоящего времени типографии почти не пользовались. [c. 158]
158]
Клей щелочной обработки из кукурузного крахмала. При испытании кукурузного крахмала оказалось, что он в силу своей химической стойкости мало пригоден для щелочной обработки. Температура клейстеризации кукурузного крахмала иод действием едкого натра значительно понижается. Дальнейшее же изменение крахмальных зерен, т. е. их распадение на части, и дальнейщая дезагрегация происходят гораздо медленнее, чем у картофельного крахмала. 15%-ный или 20%-ный клей из кукурузного крахмала при добавке 10%-ного едкого натра (от веса крахмала) после продолжительного перемешивания и нагревания при 90—100° С оставался чрезвычайно густым и не разжижался, вследствие чего кукурузный крахмал нужно признать мало пригодным для приготовления высококонцентрированного клея щелочной обработки.
Процесс получения клея из картофельного крахмала аналогичен процессу получения клея из кукурузного крахмала. С удлинением процесса приготовления клей разжижается, содер капнс декстрина повышается, клеящая сила понижается. Разница заключается только в том, что процесс приготовления клея из картофельного крахмала можно вести при более низкой температуре в связи с разницей в температуре клейстеризации кукурузного и картофельного крахмалов. [c.173]
С удлинением процесса приготовления клей разжижается, содер капнс декстрина повышается, клеящая сила понижается. Разница заключается только в том, что процесс приготовления клея из картофельного крахмала можно вести при более низкой температуре в связи с разницей в температуре клейстеризации кукурузного и картофельного крахмалов. [c.173]
Исследования этих видов клея под микроскопом показали в пробах, взятых из клея, приготовленного при 20° С, в полз зрения находятся плотные мелкие зерна в пробах из других образцов клея зерна по мере повышения температуры клейстеризации увеличиваются в объеме прп 100° С зерпа лопаются и в поле зрения появляются пустые слабо окрашенные оболочки зерен. [c.222]
Термографический метод в области коллоидной химии впервые был применен А. В. Николаевым [Н-59, 60] при определении влияния электролитов и окислителей на процесс клейстеризации крахмала и муки. Регистрация незначительных тепловых эффектов была успешно осуществлена при помощи чувствительной дифференциальной термопары и автоматического размешивания суспензий как образца, так и эталона при помощи одного механизма. В результате автору удалось наблюдать тепловые эффекты не только на дифференциальной кривой, но и на температурной. Интересно, что температура клейстеризации крахмала, определенная термографическим методом, дала полное совпадение с данными С. В. Горбачева (по началу образования адсорбционного соединения с иодом). Оствальда (по резкому увеличению вязкости), Кюнцеля и Донера (по резкому увеличению прозрачности) и А. В. Николаева и П. Осетрова (по уменьшению объема). [c.154]
В результате автору удалось наблюдать тепловые эффекты не только на дифференциальной кривой, но и на температурной. Интересно, что температура клейстеризации крахмала, определенная термографическим методом, дала полное совпадение с данными С. В. Горбачева (по началу образования адсорбционного соединения с иодом). Оствальда (по резкому увеличению вязкости), Кюнцеля и Донера (по резкому увеличению прозрачности) и А. В. Николаева и П. Осетрова (по уменьшению объема). [c.154]
Обобщение пройденного материала по теме: «Углеводы» — Статьи — Техникум — Каталог статей
Прокуда Елена Анатольевна
Преподаватель общеобразовательных дисциплин (биология, химия)
ГБОУ НПО «Новотроицкий сельскохозяйственный техникум»
Обобщение пройденного материала по теме: «Углеводы».
Игра как форма нетрадиционного урока.
Современные педагоги постоянно ищут новые формы «оживления» процесса объяснения материала и обратной связи, которые помогут активизировать всех учащихся, повысить их интерес к занятиям и вместе с тем обеспечат быстроту запоминания, понимания и усвоения учебного материала.
Нетрадиционные уроки — это занятия, которые аккумулируют методы и приемы различных форм обучения. Они строятся на совместной деятельности педагога и учащихся, на совместном поиске, на эксперименте по отработке новых приемов с целью повышения эффективности учебно-воспитательного процесса.
Признаки нетрадиционного занятия:
присутствуют элементы нового, происходит изменение внешних рамок;
кроме программного, используется и внепрограммный материал;
организуется коллективная деятельность обучающихся в сочетании с индивидуальной;
занятие проводится в нетрадиционном месте или с использованием оригинального оформления;
в процессе занятия используется музыка, видео, информационные компьютерные технологии, мультимедийное оборудование;
дает возможность обучающимся раскрыться с новых сторон, помогает ориентироваться в атмосфере творческого поиска;
требует серьезной предварительной подготовки.
Конечно, весь учебный процесс переводить на «нетрадиционные рельсы» не нужно. Именно традиционный урок должен быть основной формой обучения и воспитания, но разнообразить учебный процесс нестандартными занятиями необходимо, т. к. они помогут активизировать мыслительную деятельность учащихся, развить их творческие способности, повысить мотивированность к учению. А при проведении педагогами открытых уроков нетрадиционная форма занятий всегда будет являться выигрышной, т. к. в нее можно включить и игровые моменты, и оригинальную подачу материала, и различные виды коллективной и групповой работы учащихся.
Именно традиционный урок должен быть основной формой обучения и воспитания, но разнообразить учебный процесс нестандартными занятиями необходимо, т. к. они помогут активизировать мыслительную деятельность учащихся, развить их творческие способности, повысить мотивированность к учению. А при проведении педагогами открытых уроков нетрадиционная форма занятий всегда будет являться выигрышной, т. к. в нее можно включить и игровые моменты, и оригинальную подачу материала, и различные виды коллективной и групповой работы учащихся.
Игра — это вид деятельности в ситуациях, направленных на воссоздание и усвоение общественного опыта, в котором складывается и совершенствуется самоуправление поведением. Игра дает возможность обучающемуся, включаясь в игровую ситуацию, испытать яркие эмоциональные переживания успеха или неудачи. Также дети и подростки в процессе игры развивают способности, необходимые в области деловых и социальных отношений, — проявлять инициативу, ставить и решать проблему, планировать деятельность, решать коммуникативные задачи; учатся самостоятельности, кооперативности, толерантности, чувству товарищества и партнерства, учатся вести диалог, идти на компромисс. Игра способствует также развитию личности, формируя такие качества, как уверенность в себе, инициативность, стремление к творчеству. Учебные игры дают возможность глубже познать окружающую действительность, погрузиться в профессию, ситуацию и т. д.
Игра способствует также развитию личности, формируя такие качества, как уверенность в себе, инициативность, стремление к творчеству. Учебные игры дают возможность глубже познать окружающую действительность, погрузиться в профессию, ситуацию и т. д.
Вашему вниманию предлагается разработка одного из уроков нетрадиционной формы по теме: «Обобщение углеводов по теме: «Углеводы». Урок-игра».
Тип урока: нетрадиционный.
Цель урока: обобщить сведения об углеводах, проверить уровень знаний учащихся по теме; практически подтвердить свойства углеводов; продолжить формирование навыков практической работы с веществами и оборудованием.
Задачи:
- Учебно-образовательные: повторение, обобщение и систематизация знаний учащихся об углеводах на основе сравнительной характеристики состава, строения, свойств, обеспечивающее обратную связь и оперативную корректировку учебного процесса: выявление и оценка степени овладения системой знаний и комплексом навыков и умений, готовности учащихся успешно применять полученные знания на практике; сформировать понятие об углеводах.

- Учебно-развивающие: формирование у учащихся навыков практического применения углеводов; сформировать понятие об углеводах; развитие логического мышления учащихся на основании анализа, синтеза, обобщения.
- Учебно-воспитательные: показать учащимся связь изучаемого материала с жизнью и другими науками; продолжить формирование научного мировоззрения, подводить учащихся к правильному применению знаний в жизни человека.
Методы:
- Объяснительно-иллюстративные (беседа, объяснения (словесные), рассказ, работа с рисунками).
- Исследовательский (выполнения практических опытов, реакций).
Методические приемы:
Логические: — определение цели урока, оценка результатов;
— выявление взаимосвязей и причинно-следственных связей;
— обобщение на основе анализа, синтеза и сравнения;
— формулировка выводов.
Технические: — выполнение заданий на закрепление материала;
— работа с иллюстрированным материалом;
— записи в тетради.
Организационные: — привлечение вниманий учащихся;
— постановка вопросов;
— опора на опыт и знания учащихся.
Межпредметные связи: — с биологией;
— с кулинарией.
Формы организации учебной деятельности учащихся: сочетание групповой, индивидуальной и фронтальной деятельности учащихся.
Оборудование: реактивы необходимые для практических заданий (по углеводам).
Ход урока:
- Организационный момент.
(приветствие учащихся, проверка учащихся).
- Актуализация знаний учащихся и постановка целей урока.
Вступительное слово преподавателя:
— Сегодня вам предстоит участвовать в необычном уроке химии. Химия – это самая необычная и интересная наука на свете. Она полна разных тайн и чудес. А люди, знающие химию волшебники.
Вот мы с вами сегодня на этом уроке попробуем ими стать. Итак, для начала разделимся на 3 команды (учащиеся делятся на 3 команды и рассаживаются группами вокруг своих столов). Игра начинается……
Итак, для начала разделимся на 3 команды (учащиеся делятся на 3 команды и рассаживаются группами вокруг своих столов). Игра начинается……
1-ое задание: Вам необходимо за 3 минуты придумать название и девиз своей команде, но есть одно условие! Чтобы название команд было связано с темой нашего урока (т.е. с углеводами).
2-ое задание: Кубик «Грани»! Правила простые: один человек из команды подходит, берет листик, на котором написан углевод. Затем бросает кубик (на кубике на каждой грани написаны надписи-задания), какой гранью он падает — такое и задание. Итак, все команды по очереди.
(Приложение 1)
3-е задание: Зашифрованное слово (каждой команде раздаются листы с заданиями) в течение 7 минут команды выполняют эти задания.
(Приложения 2)
4-ое задание: «Черный ящик»
1 вопрос. В «черном ящике» находится вещество, которое в 1802 г. Впервые выделил из виноградного сока французский химик Жозеф Луи Пруст. Это вещество твердое, сладкое на вкус, хорошо растворимое в воде. При растворении в воде оно образует 3 неизомерных формы. Какое вещество находится в «черном ящике»?
Это вещество твердое, сладкое на вкус, хорошо растворимое в воде. При растворении в воде оно образует 3 неизомерных формы. Какое вещество находится в «черном ящике»?
(Правильный ответ: глюкоза, существует 3 формы глюкозы (α-; ß-; альдегидная), которые отличаются своим строением).
2 вопрос: В «черном ящике» находится вещество, точнее полисахарид для которого характерны 2 вида макромолекул: линейная и разветвленная. Линейные молекулы имеют меньшую относительную молекулярную массу и составляют ту часть полисахариды, которая называется амилозой. А разветвленные структуры являются другой составной частью, называемой амилопектином. О каком полисахариде идет речь? Что находится в «черном ящике»?
(Правильный ответ: крахмал).
3 вопрос: В «черном ящике» находится углевод. Который используется в пищевой промышленности как добавка, препятствующая слеживанию и комкованию порошкообразных продуктов.
(Правильный ответ: целлюлоза).
4 вопрос: В «черном ящике» углевод, дисахарид, который представляет собой вещество находящиеся в больших количествах в соке различных растений и некоторых плодах. При получении его тщательно очищают от примесей, а затем выпаривают в вакуум-аппаратах, температура плавления его 160°С. При застывании расплавленного углевода образуется аморфная прозрачная масса.
(Правильный ответ: сахароза).
5-ое задание: Химические свойства углеводов (для этого задания необходимо по одному участнику из команды, они вытягивают задания на листочках и выполняют решение возле доски).
Задание №1. Доказать наличие альдегидной группы в глюкозе, почему ее называют еще альдегидоспиртом?
(Ответ: СН₂ОН-(СНОН)₄-С˂…………….реакция «серебряного зеркала»).
Задание №2. Каким образом глюкоза может восстановиться в соответствующий спирт (сорбит).
(Ответ: СН₂ОН-(СНОН)₄-С˂…………….).
Задание №3. Напишите важное химическое свойство глюкозы (брожение) под действием органических катализаторов-ферментов, вырабатываемых микроорганизмами.
( Ответ: 1. спиртовое брожение (под действием ферментов дрожжей):
С₆Н₁₂О₆→2С₂Н₅ОН+2СО₂↑
2.Молочнокислое брожение (под действием молочнокислых бактерий):
С₆Н₁₂О₆→2 молекулы молочной кислоты).
6-ое задание: Интересные факты…(учащиеся рассказывают доклады подготовленные ими заранее).
Доклад Глюкоза; доклад сахароза и фруктоза; доклад крахмал и целлюлоза.
7-ое задание: Практическое задание (необходимо выбрать одного человека из команды, который выполнить опыт при помощи реактивов по карточки-задания).
Даны карточки-задания:
Карточка №1. Провести качественную реакцию на крахмал.
Карточка №2. Провести качественную реакцию на глюкозу (реакция «серебряного зеркала»).
Карточка №3. Провести реакцию доказывающую, что глюкоза может выступать как многоатомный спирт, так и альдегид.
8-ое задание: Размышление. Все прекрасно знают, что углеводы играют огромную роль в жизнедеятельности организма человека. С их помощью протекают очень важные биохимические процессы в органах, крови и тканях. Углеводы — неотъемлемая часть рациона питания человека, они являются основным источником обеспечения энергетических затрат организма. Поэтому давайте немного поразмышляем о том, где применяются углеводы в пищевой промышленности (каждая команда по одному человеку перечисляет, где применяются углеводы в пищевой промышленности).
9-ое задание: Диктант по углеводам (из каждой команды вызывается учащийся к доске, для которого уже выбран углевод (глюкоза, крахмал, сахароза) им начинает преподаватель перечислять утверждения характерные для этих углеводов и то утверждение, которое соответствует их углеводу, ставит на доске «+», после последнего вопроса подсчитывают количество «+».
( Ответы: глюкоза – 8 «+»; крахмал – 5 «+»; сахароза – 6 «+»).
(Приложение 3)
10-ое задание: «Крестики-нолики» (на доске рисуется шаблон для этого задания, вызываются два учащегося к доске и по очереди задаются им вопросы):
- Является ли фруктоза моносахаридом? (да)
- Целлюлоза – это дисахарид? (нет)
- Формула глюкозы С₆Н₁₂О₆? (да)
- Сахароза растворяется в воде? (да)
- Применяют ли целлюлозу для получения пластмасс? (да)
- Крахмал имеет точку плавления? (нет)
- Фруктоза слаще сахарозы? (да)
- Сахароза дает реакцию на альдегидную группу? (нет)
- Правда, что полисахариды – это сложные углеводы? (да)
- Крахмал сладкий на вкус? (нет)
- Глюкоза является альдегидоспиртом? (да)
- Формулы у глюкозы и фруктозы разные? (нет)
- Используется ли крахмал для получения волокна? (нет)
- Целлюлоза вступает в реакцию брожения? (нет)
- Используется ли глюкоза для приготовления зеркал? (да)
- Целлюлоза используется в качестве топлива? (да)
- Сахароза образует коллоид в горячей воде? (нет)
- Рибоза относится к углеводам? (да)
- Является ли дезоксирибоза моносахаридом? (да)
- Лактоза относится к полисахаридам? (нет)
- Солодовый сахар – это лактоза? (да)
- Мальтоза – это дисахарид? (да)
- Фруктоза подвергается гидролизу? (нет)
- Подведение итогов (объявление победителя, выставление оценок в журнал).

Список используемой литературы.
- Чередов И.М. Формы учебной работы в средней школе. — М.: Просвещение, 1988.
- Онищук В.А. Урок в современной школе. – М.: Просвещение, 1986.
- Махмутов М.И. Современный урок. — М., 1985.
- Культура современного урока / Под ред. Н.Е. Щурковой. – М., 1997.
- Дайри Н.Г. Основное усвоить на уроке. – М.: Просвещение, 1987.
- Гузеев В.В. К формализации дидактики: системный классификатор организационных форм обучения (уроков) // Школьные технологии. – 2002. – № 4.
- Марри Р., Греннер Д., Мейес П., Родуэлл В. Биохимия человека. М.: 1993. 168с.
- Павлов И.Ю., Валеннко Д.В., Москвичев Д.В. Биология. Словарь-справочник. Ростов-на-Дону, 1997. – 517с.
Написаны три вещества: глюкоза, крахмал, сахароза.
Надписи – задания:
1 грань – дайте описание
2 грань – сравните с чем-нибудь
3 грань – проассоциируйте (на что похож)
4 грань – проанализируйте (из чего состоит)
5 грань – применение
6 грань – приведите примеры
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Приложение 3
Утверждения:
- Это моносахарид (глюкоза).

- Хорошо растворимое вещество (глюкоза, сахароза).
- Это дисахарид (сахароза).
- Образует коллоид в горячей воде (крахмал).
- Волокнистое вещество.
- Это полисахарид (крахмал).
- Порошкообразное вещество (крахмал).
- Дает реакцию «серебряного зеркала» (глюкоза).
- С гидроксидом меди образует ярко-синий раствор (глюкоза, сахароза).
- Подвергается гидролизу (сахароза, крахмал).
- Вступает в реакцию брожения (глюкоза).
- Легкоплавкое вещество (сахароза, глюкоза).
- Применяется в кондитерском деле (глюкоза, сахароза, крахмал).
- Используется для изготовления зеркал (глюкоза).
Контрольная работа по органической химии для 10 класса на тему «Углеводы»
Внимание! Соблюдайте технику безопасности! Выданы 4 склянки с веществами. В одной – этиловый спирт, в другой — раствор глицерина, в третьей – раствор глюкозы, в четвёртой — раствор уксусной кислоты. Определите опытным путём, в какой склянке какое вещество содержится. Составьте план решения и опишите наблюдения.
Составьте план решения и опишите наблюдения.
Разноуровневая контрольная работа по теме «Углеводы». 10класс
Вариант 2
Часть А
А1. «Белый “хрустящий” порошок, в холодной воде нерастворим, в горячей воде образует коллоидный раствор» — данное высказывание справедливо для:
а) целлюлозы; б) сахароза; в) крахмала; г) глюкозы .
А2. Фруктоза и глюкоза являются:
а) изомерами; б) гомологами; в) одним и тем же веществом; г) таутомерами.
А3. При окислении глюкозы образуется:
а) сорбит; б) сахароза; в) глюконовая кислота; г) фруктоза.
А4. Наличие пяти гидроксигрупп в молекуле глюкозы может быть доказано в результате реакции получения из неё:
а) карбоновой кислоты; б) сложного эфира; в) многоатомного спирта; г) комплекса с ионом Cu2+.
А5. Продуктами гидролиза сахарозы являются:
а) глюкоза и глицерин; б) глюкоза и фруктоза; в) α- глюкоза и β-глюкоза ; г) крахмал и целлюлоза.
А6. Полисахаридом является:
а) рибоза; б) сахароза; в) крахмал; г) глюкоза.
А7. При восстановлении глюкозы образуется многоатомный спирт, используемый в качестве заменителя сахара при заболевании сахарным диабетом. Название этого спирта:
а) сахароза ; б) глицерин; в) сорбит; г) этиленгликоль.
А8. Реакция « серебряного зеркала» характерна для каждого из двух веществ:
а) глюкозы и глицерина; б) глюкозы и формальдегида; в) сахарозы и глицерина; г) сахарозы и формальдегида.
А9. Целлюлоза не взаимодействует с :
а) O2; б) HNO3; в) Cl2 ; г) CH3COOH.
А10. α- и β – циклические формы глюкозы отличаются между собой:
А) количеством гидроксильных групп; б) количеством карбонильных групп;
в) пространственным расположением гидроксильной группы у первого атома углерода;
г) пространственным расположением гидроксильной группы у третьего атома углерода .
Часть В
В1. Верны ли следующие суждения?
А. Ферменты человека способствуют гидролизу целлюлозы.
Б. Глюкозу используют в производстве зеркал и ёлочных игрушек.
а) верно только А; б) верно только Б; в) верны оба суждения; г) оба суждения неверны.
В2. Верны ли следующие суждения?
А. Температура плавления веществ в ряду: сорбит – глицерин – этиленгликоль уменьшается.
Б. Целлюлоза взаимодействует с органическими и неорганическими кислотами с образованием сложных эфиров.
а) верно только А; б) верно только Б; в) верны оба суждения; г) оба суждения неверны.
Часть С
С1. Массовая доля крахмала в картофеле составляет 20%. Какую массу глюкозы можно получить из картофеля массой 1620 г.
С2 . Какую массу шестиатомного спирта сорбита можно получить при восстановлении глюкозы массой 1 кг? Массовая доля выхода сорбита составляет 80%.
С3. Пользуясь ниже приведённой таблицей, составьте план решения задачи. Опишите наблюдения и приведите необходимые уравнения реакций
Внимание! Соблюдайте технику безопасности!
В четырёх пробирках под номерами находятся: раствор ацетата натрия, крахмальный клейстер, этиленгликоль, раствор муравьиной кислоты. Распознайте эти вещества опытным путём. Составьте план решения и опишите наблюдения.
Ответы на задания части А
ЗаданиеВариант
1
2
3
4
5
6
7
8
9
10
1
а
б
б
г
а
а
г
г
а
а
2
в
а
в
б
б
в
в
б
в
в
Ответы на задания части Б
Ответы к заданиям части С
Вариант 1
С1.
 C6H12O6 → 2CH₃―CHOH―COOH (молочная кислота)
C6H12O6 → 2CH₃―CHOH―COOH (молочная кислота)mчистой( C6H12O6)=300-( 300г ∙0,05)=285г
ν( C6H12O6)=285/180=1,583моль
ν(CH₃―CHOH―COOH)=2ν( C6H12O6)=2∙1,583=3,166моль.
m(CH₃―CHOH―COOH)=ν∙М=3,166∙90=284,94г
С2.
Россельхознадзор — Официальный сайт — Версия для печати
Учеными Россельхознадзора на базе подведомственного Службе ФГБУ «ВНИИЗЖ» детально изучены способы фальсификации молочной продукции, практикуемые при производстве этих товаров, в том числе на территории России. С целью предотвращения обмана потребителей, Россельхознадзор считает необходимым довести до сведения общественности информацию по рассматриваемой теме.
Проблема идентификации молочных товаров приобрела особую
актуальность, в связи с обновлением ассортимента молочных продуктов за счет
введения в их состав компонентов из растительного сырья (растительных масел,
соевых белков и др. ), увеличение числа видов и разновидностей кисломолочных
продуктов.
), увеличение числа видов и разновидностей кисломолочных
продуктов.
Целью фальсификации является получение незаконной прибыли за счет снижения себестоимости продукции в результате несанкционированной замены качественного биологически ценного сырья менее ценным. Большинство современных методов фальсификации, так или иначе, сводятся к изменениям технологии, использованию дешевого сырья, и последующему доведению физико-химических показателей до установленных нормативной документацией требований. Наряду с намеренным введением потребителя в заблуждение относительно свойств и происхождения продукции, снижения пищевой и биологической ценности, производство и реализация фальсифицированной продукции способствует также недобросовестной конкуренции на продовольственном рынке, в результате чего добросовестные изготовители оказываются в невыгодном положении.
Наиболее часто для фальсификации продуктов из коровьего
молока используют добавки дешевых растительных жиров: пальмового,
пальмоядрового, кокосового и соевого. Эти жиры используют по отдельности и в
различных сочетаниях.
Эти жиры используют по отдельности и в
различных сочетаниях.
Для каждого жира характерен свой набор и соотношение жирных кислот. Для кокосового и пальмоядрового жиров характерно высокое содержание лауриновой кислоты, для соевого — линолевой, для пальмового — пальмитиновой и олеиновой кислот. В тоже время, в отличие от молочного жира, во всех растительных жирах отсутствует масляная кислота, а в жирах, за исключением кокосового, практически отсутствуют и другие низкомолекулярные кислоты, включая миристиновую.
Широкое применение нашли и так называемые заменители молочного жира, представляющие смесь растительных жиров, подвергнутых модификации. При этом температура плавления заменителей молочного жира должна быть схожей с молочным жиром, что обеспечивает им необходимые пластичные свойства и способствует расширению возможности фальсификации.
Фальсификация цельного молока. Чаще всего вместо цельного
натурального молока представляют восстановленное молоко с добавлением
растительных жиров, затем это молоко используют для изготовления кисломолочной
продукции. Подмена одного молока другим очень часто бывает при продаже козьего
молока (оно реализуется и по более высокой цене). Происходит и подмена
натурального (цельного) молока нормализованным. Поскольку в натуральном молоке
содержание жира может достигать 4,5 и даже 6,0%, то подмена его нормализованным
2,5% молоком дает солидный доход фальсификатору. Кроме воды в молоко
подмешивают крахмал, мел, мыло, соду, известь, борную или салициловую кислоты и
даже гипс. Все это делается для фальсификации или для предохранения от быстрого
скисания. В действительности, применение этих добавок не предохраняет молоко от
скисания. И, что самое главное, часто приводит к пищевым отравлениям. Приемы
фальсификации молока за последние 2–3 года практически не изменились.
Подмена одного молока другим очень часто бывает при продаже козьего
молока (оно реализуется и по более высокой цене). Происходит и подмена
натурального (цельного) молока нормализованным. Поскольку в натуральном молоке
содержание жира может достигать 4,5 и даже 6,0%, то подмена его нормализованным
2,5% молоком дает солидный доход фальсификатору. Кроме воды в молоко
подмешивают крахмал, мел, мыло, соду, известь, борную или салициловую кислоты и
даже гипс. Все это делается для фальсификации или для предохранения от быстрого
скисания. В действительности, применение этих добавок не предохраняет молоко от
скисания. И, что самое главное, часто приводит к пищевым отравлениям. Приемы
фальсификации молока за последние 2–3 года практически не изменились.
Фальсификация сметаны. Чаще всего сметану разбавляют: водой,
кефиром, обезжиренным творогом, вводят в состав растительное масло, соевый
белок, низкокачественные молочные компоненты, крахмал, стабилизаторы, вкусовые
добавки.
Фальсификация творога. Качественный нежирный творог содержит всего 0,5% жира, а вот белка в нем не менее 17%. Калорийность такого творога всего 60ккал на 100 граммов продукта. К сожалению, заявленная жирность не всегда соответствует реальной. В фальсифицированном продукте жирность бывает более 10%, причем жировая фаза содержит не только молочный жир, но и растительный, а содержание белка всего 10%.
Фальсификация сливочного масла. Замена молочного жира на растительный жир. Добавление маргарина или других гидрированных жиров.
Фальсификация сыра. Возможно повышенное содержание воды, замена молочного жира растительным, введение соевого белка, уменьшение жирности, нарушение режима созревания и др.
Как уже было отмечено, для фальсификации молочной продукции
наиболее часто используют гидрированные жиры или смеси с другими маслами,
применение которых должно быть ограничено из-за высокого содержания в них транс-изомеров
жирных кислот (ТИЖК). ТИЖК образуются в жирах в процессе гидрогенизации,
дезодорации, отбеливания и воздействия высоких температур. Транс-жиры обладают
усвояемостью, одинаковой с обычными жирами. Входя во все липидные структуры
организма, например, в клеточные мембраны, транс-жиры нарушают транспорт
веществ через них, передачу сигналов, работу рецепторов на мембранах, биохимию
вспомогательных процессов.
ТИЖК образуются в жирах в процессе гидрогенизации,
дезодорации, отбеливания и воздействия высоких температур. Транс-жиры обладают
усвояемостью, одинаковой с обычными жирами. Входя во все липидные структуры
организма, например, в клеточные мембраны, транс-жиры нарушают транспорт
веществ через них, передачу сигналов, работу рецепторов на мембранах, биохимию
вспомогательных процессов.
66048 (Изменения углеводов и белков) — документ, страница 3
Качество студня определяет природа желирующего вещества, его концентрация и температура студнеобразования. Очевидно, что чем выше концентрация желирующего вещества, тем более прочные получаются студни и выше температура их плавления.
Важное свойство студней их тиксотропия, т. е. потеря структурной вязкости при механических воздействиях, когда они способны разжижаться, а затем частично восстанавливать свои свойства.
Еще одно обстоятельство: при хранении студней может произойти их синерезис, т. е. старение, сопровождающееся отделением части водной фазы. Особенно подвержены синерезису крахмальные студни. (При хранении густых киселей происходит отделение жидкости.)
е. старение, сопровождающееся отделением части водной фазы. Особенно подвержены синерезису крахмальные студни. (При хранении густых киселей происходит отделение жидкости.)
Желатин применяют при изготовлении желе и муссов. Чтобы желе и муссы не расплавились при комнатной температуре, в их рецептуру вводят до 3% желатина. Преимущества желатина — прозрачность студней, эластичность, допускающая взбивание, и слабовыраженный вкус. А недостатки — низкая желирующая способность, медленное образование студня, снижение желирующих свойств при кипячении. Еще один недостаток: застывание желатиновых студней зависит от температуры, поэтому их приходится длительное время выдерживать в холодильнике.
Агар используют при изготовлении желе. Этот продукт получают из морской водоросли анфельции. Агар не растворяется в холодной воде, но при кипячении дат слабоконцентрированные растворы, образующие студень при охлаждении. Студни агара имеют высокую температуру плавления. Так, 1,5% -ный раствор образует студни после охлаждения до 32-39 °С. Студни агара отличаются плотностью, прозрачностью. Преимущества — высокая желирующая способность, прозрачность, высокая температура образования студня и плавления. Хотя последнее качество агара может быть и недостатком. Так, агар нельзя использовать для приготовления муссов, самбуков, так как в процессе взбивания он очень быстро застывает.
Студни агара отличаются плотностью, прозрачностью. Преимущества — высокая желирующая способность, прозрачность, высокая температура образования студня и плавления. Хотя последнее качество агара может быть и недостатком. Так, агар нельзя использовать для приготовления муссов, самбуков, так как в процессе взбивания он очень быстро застывает.
Крахмал используют для изготовления киселей. При нагреве в результате клейстеризации крахмал дает студни разной плотности. Широко распространен картофельный крахмал. Он дает прозрачные студни, плотность которых и температура образования студня зависят от концентрации крахмала. Для получения студней, сохраняющих свою форму при комнатной температуре, требуется концентрация картофельного крахмала около 8%, а для студней, не застывающих при комнатной температуре (жидкие кисели), от 3,5 до 5%. Картофельный крахмал используют для приготовления фруктово-ягодных киселей.
Кукурузный крахмал дает нежные, но непрозрачные студни, поэтому его применяют только для приготовления молочных киселей. Преимущество крахмалов как желирующих веществ — дешевизна и способность давать вязкие или застывающие растворы. Температура начала клейстеризации картофельного крахмала составляет 62 , кукурузного крахмала 64 . Сахар повышает температуру клейстеризации крахмала.
Преимущество крахмалов как желирующих веществ — дешевизна и способность давать вязкие или застывающие растворы. Температура начала клейстеризации картофельного крахмала составляет 62 , кукурузного крахмала 64 . Сахар повышает температуру клейстеризации крахмала.
Недостаток крахмалов — способность образованных клейстеров разжижаться при длительном нагревании в результате разрушения набухших крахмальных зерен. На практике этот недостаток приводит к разжижению киселей при длительном кипячении или медленном охлаждении. Крахмальный клейстер в значительной степени подвержен синерезису — иногда мутнеет при хранении и влага отделяется от густых киселей. Высокая вязкость крахмальных клейстеров затрудняет изготовление сладких блюд, вязкость настолько быстро возрастает, что нужно очень энергичное перемешивание, чтобы в киселе не образовались плотные комки.
Модифицированные крахмалы получают из природных путем их обработки, при которой крахмал приобретает различные свойства. Так, при изготовлении сладких блюд модифицированные крахмалы имеют ряд преимуществ, их клейстеризованные растворы обладают меньшей вязкостью, низкой температурой клейстеризации и желирующей способностью способностью.
На практике применяются крахмалы кислотной и комбинированной обработки. Студни картофельного крахмала кислотной модификации близки по свойствам к гелям желатина. Гели модифицированного крахмала нежнее, легко отделяются от стенок посуды. Кукурузный модифицированный крахмал отличается от картофельного по свойствам: его студни менее вязкие, во время варки киселей он пенится и пригорает, что затрудняет его использование.
Прочность студней модифицированных крахмалов зависит от их концентрации, что позволяет, получать изделия требуемой консистенции, изменяя количество крахмала.
Агароид вырабатывают из черноморской водоросли филлофлоры. Свойства этого желирующего продукта весьма своеобразны. По студнеобразующей способности превосходит желатин. 1,5%-ная концентрация агароида образует студни с высокой температурой плавления, без посторонних запахов и привкусов, более прозрачные чем гели желатина. Растворы агароида устойчивы к кипячению (кипячение в течение 20-60 мин лишь незначительно в лияет на свойство агароида. ).
).
На прочность студней агароида влияет только щавелевая кислота, на другие органические кислоты агароид не реагирует. Добавление натри. вой соли лимонной кислоты уменьшает желирующую спо собность агароида, а при введении этой соли в количеств 0,052 экв/л раствор агароида не образует студня. Но при подкислении студнеобразующая способность агароида восстанавливается.
Часто при изготовлении желе добавляют лимонную кислоту, температура смеси в этот момент не должна быть выше 60 , иначе прочность студня ослабевает. Выдерживание студней агароида около 1 ч без охлаждения при температуре студнеобразования приводит к уплотнению геля. Объясняется это тем, что в неохлажденных растворах легче возникают связи между макромолекулами, приводящие к образованию внутренней структуры студня.
Альгинат натрия как желирующее вещество применяется редко. Его вырабатывают из бурых водорослей, основой альгината натрия является растворимая натривая соль альгиновой кислоты. При добавлении солей кальция образуются нерастворимые кальциевые соли альгиновой кислоты, студнеобразующая способность которых в 4 раза больше, чем желатина.
Альгинат натрия устойчив при нагревании, студни его бесцветны, прозрачны, у них нет посторонних запахов и привкуса.
Изделия из альгината натрия не требуют охлаждения в холодильниках, так как студнеобразование протекает одинаково при любой температуре, что позволяет готовить сладкие желированные блюда по мере надобности.
Пектиновые вещества способны образовывать студни только в присутствии других веществ — сахара и кислот. При приготовлении сладких блюд обычно используют не препараты пектина, а пюре из продуктов, богатых пектином (яблочное, абрикосовое, черносмородиновое). Применяется также свекловичный пектин.
3.2 Технология приготовления и требования, предъявляемые к желированным сладким блюдам
3.2.1 Кисели
Приготовление киселя складывается их двух операций: приготовления сиропа и заваривания крахмала. При изготовлении сиропа необходимо стараться сохранить витамины, вкусовые и ароматические вещества свежих плодов и ягод, из которых готовят кисель.
Ассортимент киселей велик: их готовят из свежих плодов, ягод, ревеня, отваров шиповника, сушеных фруктов, черники, плодово-ягодных соков и сиропов, джема, варенья, повидла, ягодных экстрактов, молока, сливок, чая с вином и лимонной кислотой, кваса, сахарных отваров и т. д.
Сиропы готовят различными способами, зависящими от свойств сырья. Сочные ягоды и фрукты — вишню, клюкву, малину, клубнику, смородину, чернику — промывают, кладут в неокисляющуюся посуду и разминают, отжимают сок, который хранят на холоде (сок вливают в кисель вместе с крахмалом.) Мезгу заливают водой, кипятят, отвар процеживают. В отвар кладут сахар, растворяют его и доводят сироп до кипения.
Малосочные плоды и ягоды, к которым относятся яблоки, кизил, сливы, абрикосы, крыжовник, варят с небольшим количеством воды, протирают и добавляют сахар.
Крахмал разводят небольшим количеством воды или охлажденного отвара в соотношении 1:5, тщательно размешивают, прицеживают, вливают в кипящий сироп и, быстро помешивая, заваривают. Готовый кисель охлаждают.
Готовый кисель охлаждают.
Кисели готовят трех консистенций: жидкие, средней густоты и густые. Консистенция зависит от количества крахмала. Для киселя полужидкого на 1000 г воды берут 30 г крахмала, средней густоты — 45 г, густого — 80 г. Жидкие кисели используют главным образом как подливки к крупяным блюдам. Охлажденные кисели средней густоты разливают в вазочки или стаканы. Чтобы на поверхности киселя при охлаждении не образовалась пленка, их посыпают сахаром.
Густые кисели проваривают при слабом кипении 6-8 мин и разливают в формочки, посыпанные сахаром, охлаждают, затем выкладывают в вазочки. К густым киселям подают холодное молоко. Для производства киселей используют свежие и сушеные плоды и ягоды, плодово-ягодные консервы, молоко, реже ревень. Ягодные кисели приготовляют, как правило, на картофельном крахмале, который образует прозрачный, почти бесцветный клейстер, молочные — на кукурузном крахмале, клейстер которого непрозрачный, молочно белый, пластичный.
В зависимости от количества используемого крахмала готовят кисели полужидкие (жидкие), средней густоты и густые. Для приготовления 1 кг полужидких (жидких), средней густоты и густых киселей из различного сырья требуется соответственно 30-40, 45-50 и 75-80 г крахмала. Во многие кисели для улучшения вкуса добавляют лимонную кислоту в количестве 0,05-0,1%.
Для приготовления 1 кг полужидких (жидких), средней густоты и густых киселей из различного сырья требуется соответственно 30-40, 45-50 и 75-80 г крахмала. Во многие кисели для улучшения вкуса добавляют лимонную кислоту в количестве 0,05-0,1%.
Технологическая схема приготовления киселей из свежих ягод включает следующие операции: отделение сока, приготовление отвара из мезги, приготовление сиропа на отваре, заваривание крахмала, введение сока, охлаждение киселя. Для отделения сока используют механические соковыжималки.
Чтобы лучше сохранить естественную окраску и витамины, отжатый сок охлаждают и хранят в закрытой посуде из кислотоустойчивого материала. Мезгу отваривают в течение 10-15 мин в пяти-, шестикратном количестве воды при слабом кипении, готовый отвар процеживают. Часть отвара охлаждают и используют для разведения крахмала, а на остальном готовят сироп.
Для этого к отвару добавляют сахар, доводят до кипения и кипятят 2-3 мин. Затем в сироп вводят разведенный крахмал, вновь доводят до кипения и соединяют с отжатым соком. Готовый кисель охлаждают. Сок, не подвергшийся тепловой обработке, придает готовому киселю аромат, вкус, цвет, присущий данному виду ягод, и повышает его витаминную активность. Для киселя из фруктово-ягодного сока или сиропа берут сока или сиропа 7г нормы, разводят водой и готовят кисель так же.
Готовый кисель охлаждают. Сок, не подвергшийся тепловой обработке, придает готовому киселю аромат, вкус, цвет, присущий данному виду ягод, и повышает его витаминную активность. Для киселя из фруктово-ягодного сока или сиропа берут сока или сиропа 7г нормы, разводят водой и готовят кисель так же.
3.2.2 Желе
Желе готовят из различных соков, цитрусовых, вина, молока, миндаля, кофейных отваров и т. д.
Сиропы для желе готовят, как и для киселей. Желатин или агар замачивают в большом количестве воды. После набухания лишнюю воду сливают, а желатин или агар добавляют в сироп, растворяя желирующее вещество при нагревании сиропа. Полученный раствор разливают в формочки и охлаждают до загустения. Модифицированные крахмалы вводят в сиропы или молоко и кипятят. Смесь при проваривании не загустевает, что облегчает порционирование. После охлаждения желе с модифицированным крахмалом хорошо отделяется от стенок формы, обладает блестящей поверхностью и нежной консистенцией.
Агароид для желе заливают холодной водой в соотношение 1:2 и оставляют для набухания на полчаса, затем отжимают, при этом в воду переходят примеси, придающие агароиду посторонние привкусы, и красящие вещества. В воду добавляют агароид, лимонно-кислый натрий (от 0,15 до 0,3% массы желе в зависимости от кислотности сока и сиропа), смесь доводят до кипения, охлаждают до 70-75 °С, соединяют с соками и разливают в креманки. (Введение лимонно-кислого натрия улучшает консистенцию желе, придает ему эластичность, смягчает кислотность, снижает температуру плавления желе до 30-40 ).
В воду добавляют агароид, лимонно-кислый натрий (от 0,15 до 0,3% массы желе в зависимости от кислотности сока и сиропа), смесь доводят до кипения, охлаждают до 70-75 °С, соединяют с соками и разливают в креманки. (Введение лимонно-кислого натрия улучшает консистенцию желе, придает ему эластичность, смягчает кислотность, снижает температуру плавления желе до 30-40 ).
В желе на ягодном и виноградном соках с невысокой кислотностью 10% -ного раствора лимонно-кислого натрия добавляют 0,15-0,25% от массы желе, в желе на вишневом, черешневом и черничном соках 0,25-0,3, а на клюквенном и брусничном 0,3-0,35%.
Альгинат натрия для изготовления желе заливают водой и, периодически помешивая, дают набухнуть в течение 1 ч, затем доводят до кипения и кипятят 2-3 мин. В полученный раствор добавляют сахар и суспензию фосфата кальция, доводят до кипения, охлаждают, добавляют соки, лимонную кислоту и разливают в формы.
Готовое желе должно быть прозрачным. Если желе получается мутноватым, его осветляют. Для этого белок разводят холодной кипяченой водой (1:1) или вливают в подготовленную жидкость. Размешивают, доводят до кипения и процеживают через салфетку.
Для этого белок разводят холодной кипяченой водой (1:1) или вливают в подготовленную жидкость. Размешивают, доводят до кипения и процеживают через салфетку.
Для желе из цитрусовых в сахарном сиропе проваривают цедру или настаивают в ней сироп, процеживают его, вводят набухший желатин и доводят до кипения. Из очищенных плодов отжимают сок и соединяют его с желирующим сиропом. Смесь разливают в формы.
Желе можно приготовить с консервированными плодами и ягодами. На основе сиропа консервированного компота готовят желирующий сироп с желатином и заливают им уложенные в формы нарезанные ломтиками плоды.
В молочное желе можно ввести ванилин, какао или кофейный отвар, чтобы придать блюду определенный аромат, цвет и вкус. Желе может быть комбинированным, т. е. приготовленным с добавлением фруктов, или из чередующихся слоев нескольких цветов. Для его приготовления используют ягодное, кофейное или шоколадное, молочное желе и др. Каждый вид желе наливают слоем в форму или противень, охлаждают и только после этого наливают следующий слой.
Для мозаичного желе, подготовленное различного цвета желе разливают на противень тонким слоем. После застывания его нарезают ромбиками, треугольниками или мелко рубят, смешивают, кладут в формы, заливают бесцветным или слабоокрашенным желе и охлаждают. Такие виды желе применяют для оформления банкетного стола.
Глюкоза Сахароза Целлюлоза Крахмал Кот в мешке 10
Глюкоза Сахароза Целлюлоза Крахмал Кот в мешке 10 10 10 20 20 20 30 30 30 40 40 40 50 50 50
Как переводится с греческого языка слово ГЛЮКОЗА? Глюкоза- «Сладкий» .
Каким способом Г. З. Кирхгоф получил глюкозу? Гидролиз крахмала.
19 Сумма коэффициентов в горении глюкозы?
Глюконат. Глюкозы с Cu(OH) Взаимодействие меди (II) 2 при комнатной температуре. Укажите название вещества.
Молекулярная формула сахарозы? C H O 12 22 11
Какие вещества образуются при гидролизе сахарозы? Молекулы ГЛЮКОЗЫ и ФРУКТОЗЫ.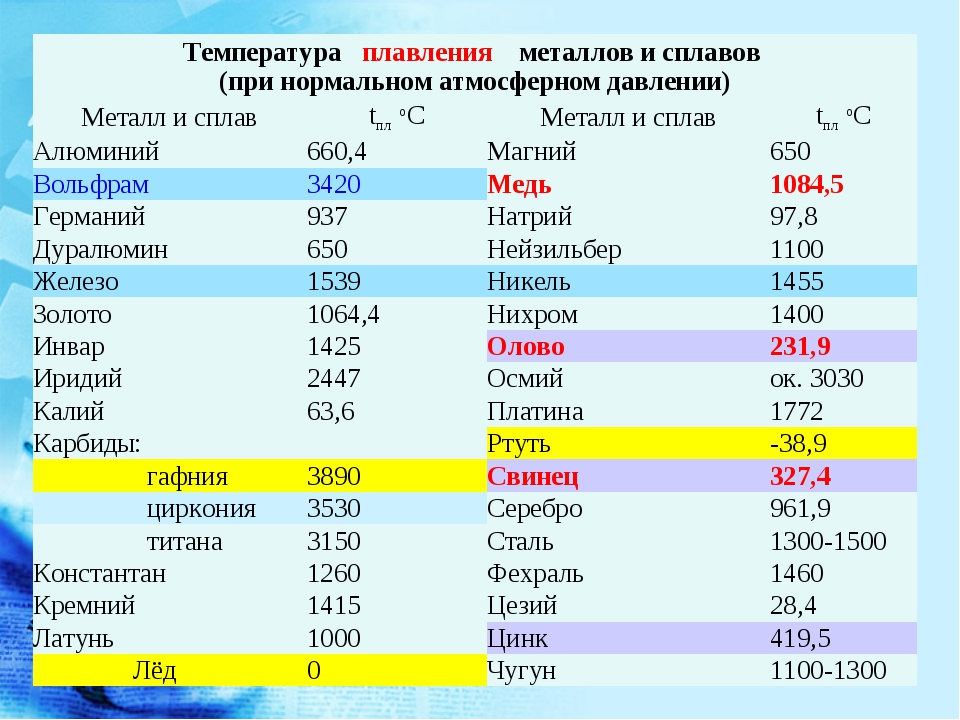
Температура плавления сахара? 160 Цельсия. Градусов
4 Сумма коэффициентов гидролиза сахарозы?
Сахарат меди (II) Как называется вещество при взаимодействии сахарозы и Cu(OH)2 (при комнатной температуре)?
Молекулярная формула целлюлозы? (С H O )n 6 10 5
Клетчатка растворяется в медноаммиачном растворе Cu(OH)2 ? ДА
Как называется эфир, который образуется при взаимодействии целлюлозы и три моль азотной кислоты? (тривиальное название) Пироксилин
Из целлюлозы, уксусного Из каких веществ можно получить триацетилцеллюлозу? ангидрида или уксусной кислоты.
Клетчатки в медно- готовят из Медно-аммиачный шелк раствора… аммиачном растворе.
Молекулярная формула крахмала? (С 6 H 10 O 5)n
Как получить из крахмала патоку? НЕПОЛНЫЙ ГИДРОЛИЗ КРАХМАЛА (присутствие неорганических кислот).
Из каких двух высокомолекулярных фракций состоит крахмал? АМИЛОЗА И АМИЛОПЕКТИН
Молекулярная масса амилозы? 30000 -40000
В чем заключается реакция КИРХГОФА? Это реакция превращения крахмала в глюкозу при каталитическом действии H 2 s. O 4.
Молекулярная формула углеводов? Cn(H 2 O)m
Раствор йода используется для обнаружения… Крахмала.
Что такое виноградный сахар? Глюкоза.
Как называется этиловый спирт, полученный из древесины? Гидролизный спирт.
Древесный уголь, H O и летучие органические вещества. Назовите вещества полученные после термического разложения целлюлозы без доступа воздуха? 2
9005-84-9 Формула, растворимая в крахмале, ЯМР, температура кипения, плотность, температура вспышки
9005-84-9 Недвижимость
- Плотность
- 1,51
- Точка кипения Разложения (Niosh, 2016)
- Точка вспышки
- 357,8 ° C
- температура плавления 256-258 ° C (дек.
 ) ( горит.)
) ( горит.) - Внешний вид бесцветные кристаллы или белый порошок
- пар 0 мм рт.652
- Растворимость Растворим в горячей воде.
- Цвет/Форма Твердый
- Стабильный Стабильный. Горючий. Несовместим с сильными окислителями.
- Код ТН ВЭД 11081100
- Температура хранения Температура хранения: без ограничений.
9005-84-9 Информация о безопасности
- Заявления о безопасности 26 26
- Заявления о риске R20 / 21/22 R20 / 21/22
- Коды опасности XI
- Безопасность
Экспериментальные тератогенные и репродуктивные эффекты.Сомнительный канцероген с экспериментальными онкогенными данными. При нагревании до разложения выделяет едкий дым и раздражающие пары.

- Токсичность
1. оральная крыса LD50:34 800 мг/кг
ЯХТЫ Якури Тирио.Фармакология и терапия. 7 (1979), 53. 2. ipr-крыса LD50:30 600 мг/кг
OYYAA2 Ойо Якури. Фармакометрия. 6 (1972), 251. 3. в/в крыса LD50:15 300 мг/кг
4. 
OYYAA2 Oyo Yakuri. Pharmacometrics. 6 (1972),251. 5. scu-mus LD50:38,600 mg/kg
YACHDS Yakuri to Chiryo.Фармакология и терапия. 7 (1979), 53. 6. в/в-мус ЛД50: 26 800 мг/кг
ЯХТЫ Якури Тирио. Фармакология и терапия. 7 (1979), 53. 7. ivn-rbt LD50:25 200 г/кг
НИИРДН «Наркотики в Японии.  Этические лекарства, 6-е издание, 1982 г.», под редакцией Японского фармацевтического информационного центра. 6 (1982), 805.
Этические лекарства, 6-е издание, 1982 г.», под редакцией Японского фармацевтического информационного центра. 6 (1982), 805. - Спецификация
Мальтоза (69-79-4), или солодовый сахар, представляет собой дисахарид, образованный из двух единиц глюкозы, соединенных связью α(1→4). Это второй член важного биохимического ряда цепей глюкозы. Добавление другой единицы глюкозы дает мальтотриозу; дальнейшие добавки будут производить декстрины и, в конечном итоге, крахмал.Он может быть расщеплен на две молекулы глюкозы путем гидролиза. В живых организмах фермент мальтаза может достичь этого очень быстро. В лаборатории нагревание с сильной кислотой в течение нескольких минут даст тот же результат. Производство мальтозы из прорастающих злаков, таких как ячмень, является важной частью процесса пивоварения. Когда ячмень соложен, его доводят до состояния, при котором концентрация амилаз, продуцирующих мальтозу, максимальна. Затирание — это процесс, посредством которого эти амилазы превращают крахмал злаков в мальтозу.
 Метаболизм мальтозы дрожжами во время ферментации приводит к образованию этанола и углекислого газа.
Метаболизм мальтозы дрожжами во время ферментации приводит к образованию этанола и углекислого газа. - Отчет
Указано в реестре EPA TSCA.
КРАХМАЛ | Камео Химикаты | НОАА
Химический паспорт
Химические идентификаторы | Опасности | Рекомендации по ответу | Физические свойства | Нормативная информация | Альтернативные химические названияХимические идентификаторы
То Поля химического идентификатора включают общие идентификационные номера, алмаз NFPA У.S. Знаки опасности Департамента транспорта и общее описание хим. Информация в CAMEO Chemicals поступает из множества источники данных.| Номер CAS | Номер ООН/НА | Знак опасности DOT | Береговая охрана США КРИС Код |
|---|---|---|---|
| никто | данные недоступны | никто | |
| Карманный справочник NIOSH | Международная карта химической безопасности | ||
| Крахмал | |||
NFPA 704
данные недоступны
Общее описание
Мелкий белый порошок без запаха. Обратите внимание, что гранулы из разных растительных источников различаются по форме, размеру и внешнему виду. Смесь углеводных полимеров амилозы и амилопектина в зависимости от источника растительного происхождения. В основном используется в пищу.
Обратите внимание, что гранулы из разных растительных источников различаются по форме, размеру и внешнему виду. Смесь углеводных полимеров амилозы и амилопектина в зависимости от источника растительного происхождения. В основном используется в пищу.
Опасности
Предупреждения о реактивности
никто
Реакции воздуха и воды
Нет быстрой реакции с воздухом Нет быстрой реакции с водой
Пожарная опасность
Нет доступной информации.
Опасность для здоровья
Пути воздействия: вдыхание, проглатывание, контакт с кожей и/или глазамиСимптомы: Раздражение глаз, кожи, слизистых оболочек; кашель, боль в груди; дерматит; ринорея (выделение жидкой слизи)
Органы-мишени: глаза, кожа, дыхательная система (NIOSH, 2016)
Профиль реактивности
КРАХМАЛ горюч. Представляет опасность взрыва пыли при рассеивании в воздухе в виде мелкой пыли в достаточных концентрациях.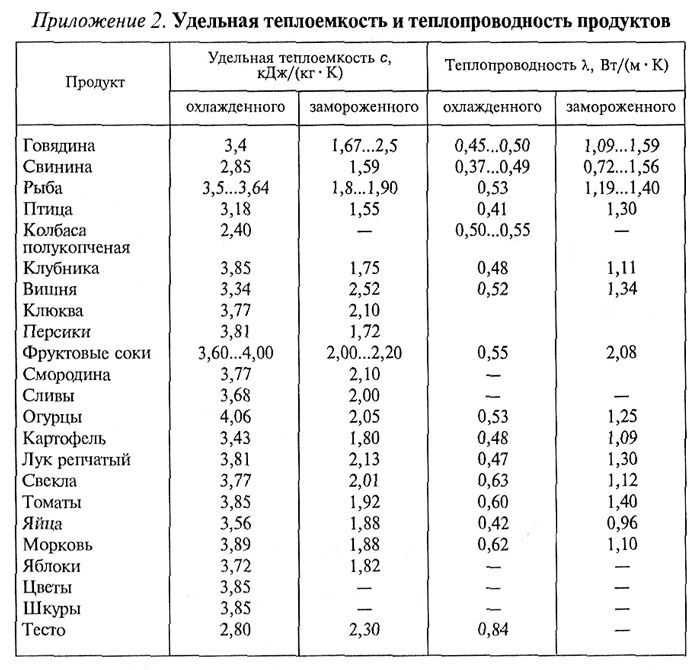 Гранулы сильно набухают в воде и образуют коллоидную суспензию.Несовместим с окислителями, кислотами, йодом, основаниями. Реагирует со смесями азотной и серной кислот с образованием нитрокрахмала, взрывчатого вещества.
Гранулы сильно набухают в воде и образуют коллоидную суспензию.Несовместим с окислителями, кислотами, йодом, основаниями. Реагирует со смесями азотной и серной кислот с образованием нитрокрахмала, взрывчатого вещества.
Принадлежит к следующей реакционной группе (группам)
Потенциально несовместимые абсорбенты
Будьте осторожны: жидкости с этой классификацией реактивной группы были Известно, что он реагирует с абсорбент перечислено ниже. Больше информации о абсорбентах, в том числе о ситуациях, на которые следует обратить внимание…
- Абсорбенты на основе целлюлозы
Рекомендации по ответу
То Поля рекомендации ответа включают в себя расстояния изоляции и эвакуации, а также рекомендации по пожаротушение, пожарное реагирование, защитная одежда и первая помощь.То информация в CAMEO Chemicals поступает из различных источники данных.Изоляция и эвакуация
Нет доступной информации.
Пожаротушение
Нет доступной информации.
Непожарный ответ
Нет доступной информации.
Защитная одежда
Кожа: Носите соответствующую защитную одежду для предотвращения контакта с кожей.Глаза: Наденьте соответствующую защиту для глаз, чтобы предотвратить попадание в глаза.
Мыть кожу: Рабочий должен мыться ежедневно в конце каждой рабочей смены.
Снять: Намокшую или сильно загрязненную рабочую одежду следует снять и заменить.
Смена: Рабочие, чья одежда могла быть заражена, должны переодеться в незагрязненную одежду, прежде чем покинуть рабочее помещение. (НИОСХ, 2016 г.)
Ткани для костюмов DuPont Tychem®
Нет доступной информации.
Первая помощь
Глаза: Если это химическое вещество попало в глаза, немедленно промойте глаза большим количеством воды, время от времени приподнимая нижние и верхние веки.Немедленно обратитесь за медицинской помощью. При работе с этим химическим веществом нельзя носить контактные линзы.
При работе с этим химическим веществом нельзя носить контактные линзы.Кожа: Если это химическое вещество попало на кожу, промойте загрязненную кожу водой с мылом.
Дыхание: Если человек вдыхает большое количество этого химического вещества, немедленно выведите пострадавшего на свежий воздух. Другие меры обычно не нужны.
Проглатывание: Если это химическое вещество было проглочено, немедленно обратитесь за медицинской помощью. (НИОСХ, 2016 г.)
Физические свойства
| Химическая формула: |
Точка воспламенения: данные недоступны
Нижний предел взрываемости (НПВ): данные недоступны
Верхний предел взрываемости (ВПВ): данные недоступны
Температура самовоспламенения: данные недоступны
Температура плавления: Разлагается (НИОСХ, 2016 г.)
Давление газа: 0 мм рт.ст. (приблизительно) (НИОСХ, 2016 г.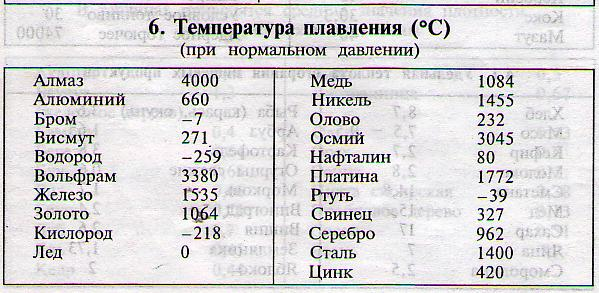 )
)
Плотность пара (относительно воздуха): данные недоступны
Удельный вес: 1.45 (НИОСХ, 2016 г.)
Точка кипения: Разлагается (НИОСХ, 2016 г.)
Молекулярная масса: варьируется (НИОСХ, 2016 г.)
Растворимость воды: Нерастворимый (НИОСХ, 2016 г.)
Потенциал ионизации: данные недоступны
ИДЛХ: данные недоступны
AEGL (нормативные уровни острого воздействия)
Информация об AEGL отсутствует.ERPG (Руководство по планированию реагирования на чрезвычайные ситуации)
Информация о ERPG отсутствует.PAC (критерии защитных действий)
Информация о PAC отсутствует.Нормативная информация
То Поля нормативной информации включить информацию из Сводный список III Агентства по охране окружающей среды США списки, Химический завод Министерства внутренней безопасности США антитеррористические стандарты, и Управление по охране труда и здоровья США Перечень стандартов по управлению безопасностью технологического процесса при работе с особо опасными химическими веществами (подробнее об этих источники данных).
Сводный перечень списков EPA
Отсутствует нормативная информация.Антитеррористические стандарты DHS Chemical Facility (CFATS)
Отсутствует нормативная информация.Список стандартов управления безопасностью процессов (PSM) OSHA
Отсутствует нормативная информация.Альтернативные химические названия
В этом разделе представлен список альтернативных названий этого химического вещества, включая торговые названия и синонимы.
Образование, структура и свойства ферменторезистентного крахмала – Laboratorium voor Levensmiddelenchemie en -biochemie
Релинде С.Эрлинген
Февраль 1994 г.
Аннотация
В данной диссертации исследованы образование, структура и свойства ферменторезистентного крахмала III типа.
Хотя в начале исследования общепризнанно считалось, что РС III типа в основном состоит из ретроградированной амилозы, было показано, что ретроградированный амилопектин также снижает чувствительность фермента. Действительно, высокие уровни РС были получены при ретроградации желатинизированных и, когда РС определяли как остаток после инкубации с панкреатической альфа-амилазой при 37°С в течение двух часов.Снижение чувствительности к ферментам может быть связано с усилением запутанности молекул и/или увеличением молекулярного порядка за счет образования двойных спиралей внешних коротких цепей амилопектина и организации этих спиралей в трехмерную (кристаллическую) структуру. . Поскольку эти короткие цепи имеют значения DP только между ок. 14 и 18 остатков глюкозы (см. 1.2.1 и 1.3.2), поэтому длина цепи устойчивых фракций также может быть ограничена. Кроме того, температура плавления ретроградного амилопектина довольно низкая (ок.65°С). Таким образом, в ретроградированном амилопектине не ожидается присутствия высокоустойчивых фракций, устойчивых к гидролизу при 100°С.
Действительно, высокие уровни РС были получены при ретроградации желатинизированных и, когда РС определяли как остаток после инкубации с панкреатической альфа-амилазой при 37°С в течение двух часов.Снижение чувствительности к ферментам может быть связано с усилением запутанности молекул и/или увеличением молекулярного порядка за счет образования двойных спиралей внешних коротких цепей амилопектина и организации этих спиралей в трехмерную (кристаллическую) структуру. . Поскольку эти короткие цепи имеют значения DP только между ок. 14 и 18 остатков глюкозы (см. 1.2.1 и 1.3.2), поэтому длина цепи устойчивых фракций также может быть ограничена. Кроме того, температура плавления ретроградного амилопектина довольно низкая (ок.65°С). Таким образом, в ретроградированном амилопектине не ожидается присутствия высокоустойчивых фракций, устойчивых к гидролизу при 100°С.
С другой стороны, RS, образованный из ретроградной амилозы, очень стабилен. Его можно выделить путем инкубации с термостабильной альфа-амилазой при 100°С и амилоглюкозидазой при 60°С. Анализ с помощью ДСК показал, что температуры плавления выделенных фракций RS были ок. 123°С. Мы показали, что в водном растворе амилозы длины цепей молекул амилозы не влияли на длины цепей (DPn между 19 и 26) и на кристаллическую структуру (тип B) полученных РС.Однако наблюдалось влияние на выход RS. В условиях эксперимента выход РС возрастал с DPn до значений плато. Мы предположили, что фракции амилозы с низкой DPn (менее 100) содержат относительно большое количество цепей, размеры которых не являются критическими для встраивания в кристаллическую структуру, что приводит к низким выходам РС. Из-за схожести длины цепи RS было предложено два возможных механизма образования RS в водных растворах амилозы: образование мицелл за счет агрегации различных молекул амилозы в определенной области цепей и образование ламеллярных структур за счет сворачивания цепей.
Анализ с помощью ДСК показал, что температуры плавления выделенных фракций RS были ок. 123°С. Мы показали, что в водном растворе амилозы длины цепей молекул амилозы не влияли на длины цепей (DPn между 19 и 26) и на кристаллическую структуру (тип B) полученных РС.Однако наблюдалось влияние на выход RS. В условиях эксперимента выход РС возрастал с DPn до значений плато. Мы предположили, что фракции амилозы с низкой DPn (менее 100) содержат относительно большое количество цепей, размеры которых не являются критическими для встраивания в кристаллическую структуру, что приводит к низким выходам РС. Из-за схожести длины цепи RS было предложено два возможных механизма образования RS в водных растворах амилозы: образование мицелл за счет агрегации различных молекул амилозы в определенной области цепей и образование ламеллярных структур за счет сворачивания цепей.
Выход РС в клейстеризованном крахмале, содержащем как амилозу (25%), так и амилопектин (75%), сильно зависел от времени хранения и температуры хранения. Действительно, мы пришли к выводу, что образование РС в клейстеризованном крахмале можно рассматривать как кристаллизацию амилозы в частично кристаллической полимерной системе. В такой полимерной системе зародышеобразование предпочтительно при температурах намного ниже температуры плавления кристаллов (около 150°C), но выше температуры стеклования (около -5°C), в то время как распространение благоприятствует условиям намного выше стеклования, но значительно ниже температуры плавления.При высокой температуре хранения (100°С) при инкубации в течение нескольких часов формировались устойчивые кристаллические структуры типа А, а при более низких температурах (0°С и 68°С) наблюдалось образование кристаллов типа В. Кристалличность устойчивых фракций повышалась со временем хранения крахмального геля.
Действительно, мы пришли к выводу, что образование РС в клейстеризованном крахмале можно рассматривать как кристаллизацию амилозы в частично кристаллической полимерной системе. В такой полимерной системе зародышеобразование предпочтительно при температурах намного ниже температуры плавления кристаллов (около 150°C), но выше температуры стеклования (около -5°C), в то время как распространение благоприятствует условиям намного выше стеклования, но значительно ниже температуры плавления.При высокой температуре хранения (100°С) при инкубации в течение нескольких часов формировались устойчивые кристаллические структуры типа А, а при более низких температурах (0°С и 68°С) наблюдалось образование кристаллов типа В. Кристалличность устойчивых фракций повышалась со временем хранения крахмального геля.
Как добавленные, так и эндогенно присутствующие липиды, хотя и присутствуют в небольших количествах (до 1,2%), снижают выход РС в крахмальных гелях. Поскольку эндогенные и добавленные липиды могут образовывать комплексы включения с амилозой, меньшее количество амилозы доступно для образования устойчивых к ферментам двойных спиралей.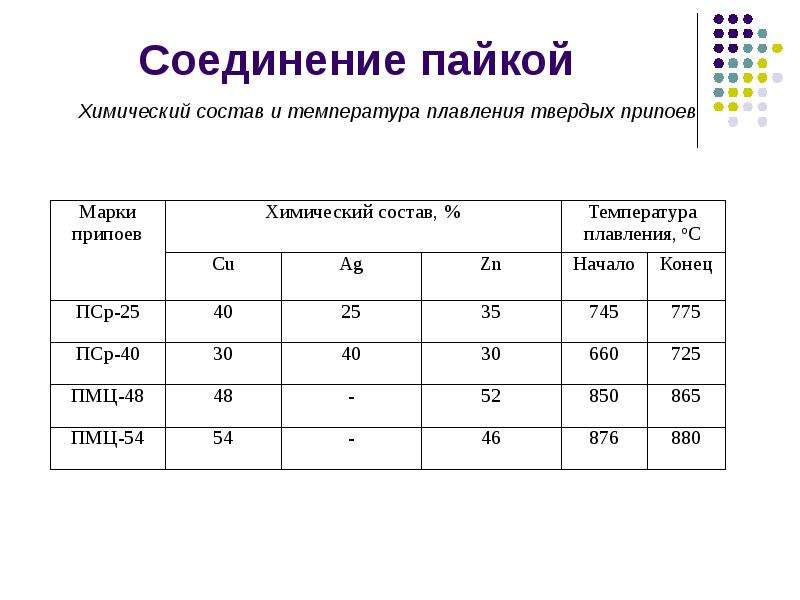 Значительные изменения выхода РС были получены даже при наличии лишь незначительных количеств липидов. Вероятно, за наблюдения ответственны комплексообразование сегментов амилозной цепи и возникающие в результате стерические препятствия для образования двойных спиралей в незакомплексованных частях цепи. При добавлении додецилсульфата натрия качество РС изменилось. Наблюдали увеличение энтальпии плавления и изменение кристаллической структуры (больше характеристик А-типа).
Значительные изменения выхода РС были получены даже при наличии лишь незначительных количеств липидов. Вероятно, за наблюдения ответственны комплексообразование сегментов амилозной цепи и возникающие в результате стерические препятствия для образования двойных спиралей в незакомплексованных частях цепи. При добавлении додецилсульфата натрия качество РС изменилось. Наблюдали увеличение энтальпии плавления и изменение кристаллической структуры (больше характеристик А-типа).
Сахара также оказывают значительное влияние на выход RS в крахмальных гелях, когда они присутствуют в высоких концентрациях.Снижение выхода RS было обнаружено в гелях пшеничного крахмала, в то время как увеличение было отмечено при использовании кукурузного крахмала с высоким содержанием амилозы. Различия в отклике выхода сахаров в гелях HA и WS при РС нельзя объяснить, хотя ясно, что разница в содержании амилозы и липидов, а также разница в температуре клейстеризации двух крахмалов не были причиной различное поведение крахмалов в присутствии сахаров. В целом влияния сахаров на рентгенографические и ДСК-характеристики выделенных РС обнаружить не удалось.
В целом влияния сахаров на рентгенографические и ДСК-характеристики выделенных РС обнаружить не удалось.
Кроме того, было показано, что могут быть получены высокие уровни RS в пищевых продуктах (хлебе). Хлеб, приготовленный из пшеничной муки (76 частей), промышленного витального пшеничного глютена (4 части) и экструдированного ретроградного высокоамиломаизированного крахмала или высокоамиломаизированного крахмала (20 частей), содержал ок. 8% RS (определено после инкубации с панкреатической альфа-амилазой при 37°C). Такие хлеба отличались отличными сроками хранения, структурой мякиша и органолептическими качествами.
В целом содержание и характеристики ферменторезистентного крахмала в пищевых продуктах зависят не только от типа крахмала (воскообразный, нормальный или с высоким содержанием амилозы), но также сильно зависят от используемых технологических условий (температуры, времени хранения) и присутствия других компонентов. компоненты.
Результаты показывают, что клейстеризованный крахмал с высокой устойчивостью к ферментам (устойчивость к термостабильной альфа-амилазе при инкубации при 100°С) может быть получен только тогда, когда кристаллизация может происходить на достаточно длинных сегментах полимерных цепей (около 25 остатков глюкозы). Таким образом, если создаются условия (время-температура и присутствие других компонентов), благоприятствующие кристаллизации, и если крахмал содержит высокие концентрации полимерных молекул с достаточно длинными цепями, способными образовать двойную спираль, высокие уровни «сильно» устойчивого крахмала могут быть ожидаемым.Поскольку ответвлениями амилопектина, доступными для кристаллизации, являются внешние короткие цепи с DP от 14 до 18 остатков глюкозы, в клейстеризованном воскообразном крахмале такие фракции не образуются. С другой стороны, в высокоамиломаизированном крахмале присутствуют высокие концентрации цепей, достаточно длинных для образования двойной спирали, и, таким образом, могут быть получены высокие уровни «сильно» устойчивого крахмала. Полученные «высокоустойчивые» фракции состоят из двойных спиралей, упорядоченных в трехмерной структуре А- или В-типа (в зависимости от температуры хранения и присутствия некоторых соединений) на определенной длине цепи.Эти фракции термостабильны и имеют температуру плавления ок.
Таким образом, если создаются условия (время-температура и присутствие других компонентов), благоприятствующие кристаллизации, и если крахмал содержит высокие концентрации полимерных молекул с достаточно длинными цепями, способными образовать двойную спираль, высокие уровни «сильно» устойчивого крахмала могут быть ожидаемым.Поскольку ответвлениями амилопектина, доступными для кристаллизации, являются внешние короткие цепи с DP от 14 до 18 остатков глюкозы, в клейстеризованном воскообразном крахмале такие фракции не образуются. С другой стороны, в высокоамиломаизированном крахмале присутствуют высокие концентрации цепей, достаточно длинных для образования двойной спирали, и, таким образом, могут быть получены высокие уровни «сильно» устойчивого крахмала. Полученные «высокоустойчивые» фракции состоят из двойных спиралей, упорядоченных в трехмерной структуре А- или В-типа (в зависимости от температуры хранения и присутствия некоторых соединений) на определенной длине цепи.Эти фракции термостабильны и имеют температуру плавления ок. 150°С.
150°С.
Как показано выше, на процесс кристаллизации влияет несколько факторов. Однако влияние некоторых из них сильно зависит от температуры, как показано на рис. 8.1. Поскольку крахмальный гель представляет собой частично кристаллическую полимерную систему, явления определяются температурой стеклования крахмальной системы и температурами плавления кристаллов, которые могут образоваться.
Кристаллизация амилозы происходит только между Tg (-5°C для крахмального геля типа B) и прибл. 150°С, температура плавления кристаллов амилозы. Поскольку амилозо-липидные комплексы диссоциируют прибл. 100°C, выше прибл. 100°С. Таким же образом предполагается, что влияние ретроградации амилопектина не происходит выше ок. 65°C из-за плавления ретроградного амилопектина при этой температуре. Как указывалось ранее, присутствие сахаров может сдвигать Tg в сторону более высоких значений.Это может иметь влияние на все явления, описанные выше (т.е. кристаллизацию амилозы, образование и кристаллизацию амилозо-липидных комплексов и ретроградацию амилопектина). Однако воздействие может быть различным для разных описываемых явлений, и поэтому нельзя построить глобальную модель, учитывающую влияние различных компонентов на формирование РС.
Однако воздействие может быть различным для разных описываемых явлений, и поэтому нельзя построить глобальную модель, учитывающую влияние различных компонентов на формирование РС.
Биоразлагаемый полимер полиэтилена низкой плотности, смешанный с крахмалом саго: синтез и характеристика
Это исследование посвящено синтезу и характеристике биоразлагаемого полимера ПЭНП, смешанного с крахмалом саго.Во-первых, было изучено влияние изменения содержания крахмала на механические свойства (удлинение при разрыве и модуль Юнга) и биоразлагаемость полимера. Для этого исследования LDPE комбинировали с 10%, 30%, 50% и 70% саго. Затем было исследовано влияние сшивания триметилолпропантриакрилатом (ТМПТА) и облучения электронным пучком (ЭП) на механические и термические свойства полимера. Во 2-м исследовании, чтобы избежать искажения данных, полимер LDPE был включен только с 50% крахмала.Содержание крахмала оказывало прямое влияние на механические свойства и биоразлагаемость полимера. Удлинение при разрыве уменьшалось с увеличением содержания крахмала, в то время как модуль Юнга и потеря массы (т.е. деградация) увеличивались с увеличением содержания крахмала. Увеличение доз сшивателя (ТМПТА) и ЭБ также приводило к увеличению модуля Юнга полимера. Однако как процессы сшивания, так и облучение ЭП привели к снижению температуры плавления полимера. Таким образом, содержание крахмала и процессы модификации играют важную роль в контроле механических, термических свойств и свойств разложения синтетического полимера ПЭНП, смешанного с крахмалом, что дает возможность модулировать свойства полимера для конкретных применений.
Удлинение при разрыве уменьшалось с увеличением содержания крахмала, в то время как модуль Юнга и потеря массы (т.е. деградация) увеличивались с увеличением содержания крахмала. Увеличение доз сшивателя (ТМПТА) и ЭБ также приводило к увеличению модуля Юнга полимера. Однако как процессы сшивания, так и облучение ЭП привели к снижению температуры плавления полимера. Таким образом, содержание крахмала и процессы модификации играют важную роль в контроле механических, термических свойств и свойств разложения синтетического полимера ПЭНП, смешанного с крахмалом, что дает возможность модулировать свойства полимера для конкретных применений.
1. Введение
Разработка инновационных биополимеров ведется уже несколько лет и продолжает вызывать интерес у современных ученых. В 1996 г. поставки канадской пластмассовой промышленности увеличились на 10,6% по сравнению с уровнем 1995 г. до 9,1 млрд долларов [1, 2]. По данным Фомина [3], в конце ХХ века мировое производство синтетических полимеров достигло 130 млн т в год, а спрос на биоразлагаемый полимер ежегодно растет на 30% [4, 5]. Между тем, в Европе расчетное среднее потребление полимера составляет 100 кг на человека в год [6]. Полиэтилен (ПЭ) широко используется в медицинских устройствах и фармацевтической упаковке [7]. Различные типы полимеров, такие как ПЭ высокой плотности (ПЭВП), ПЭ низкой плотности (ПЭНП) или линейный ПЭ низкой плотности (ЛПЭНП), предлагают различные преимущества и функциональные возможности. HDPE обеспечивает жесткость, химическую стойкость и барьерные свойства, в то время как LDPE обеспечивает устойчивость к растрескиванию под напряжением и отличные ударные свойства [8]. Кроме того, его способность к стерилизации является благоприятным и важным аспектом.Сшивание является широко используемым методом модификации свойств полимера. Этот процесс включает формирование трехмерных структур, вызывающих существенные изменения [9]. Механические свойства биоматериала так же важны, как и биосовместимость, поскольку неадекватная работа или преждевременная поломка имплантатов могут вызвать серьезные проблемы со здоровьем у пациентов [10–15].
Между тем, в Европе расчетное среднее потребление полимера составляет 100 кг на человека в год [6]. Полиэтилен (ПЭ) широко используется в медицинских устройствах и фармацевтической упаковке [7]. Различные типы полимеров, такие как ПЭ высокой плотности (ПЭВП), ПЭ низкой плотности (ПЭНП) или линейный ПЭ низкой плотности (ЛПЭНП), предлагают различные преимущества и функциональные возможности. HDPE обеспечивает жесткость, химическую стойкость и барьерные свойства, в то время как LDPE обеспечивает устойчивость к растрескиванию под напряжением и отличные ударные свойства [8]. Кроме того, его способность к стерилизации является благоприятным и важным аспектом.Сшивание является широко используемым методом модификации свойств полимера. Этот процесс включает формирование трехмерных структур, вызывающих существенные изменения [9]. Механические свойства биоматериала так же важны, как и биосовместимость, поскольку неадекватная работа или преждевременная поломка имплантатов могут вызвать серьезные проблемы со здоровьем у пациентов [10–15]. Кроме того, большая часть имплантатов тела подвергается динамической нагрузке, которая может повлиять на механическое поведение (например, сползание или расслабление) имплантатов.Имплантаты должны сохранять свою стабильность в организме в течение заданного времени по мере необходимости [16]. Таким образом, долговечность или долгосрочное механическое поведение новых биоматериалов стало главной проблемой при их внедрении в медицинские устройства.
Кроме того, большая часть имплантатов тела подвергается динамической нагрузке, которая может повлиять на механическое поведение (например, сползание или расслабление) имплантатов.Имплантаты должны сохранять свою стабильность в организме в течение заданного времени по мере необходимости [16]. Таким образом, долговечность или долгосрочное механическое поведение новых биоматериалов стало главной проблемой при их внедрении в медицинские устройства.
Крахмал представляет собой гидроколлоидный биополимер, который можно найти в различных сельскохозяйственных продуктах, таких как пшеница, кукуруза, рис, бобы и картофель [17, 18]. Крахмал состоит из одного разветвленного и линейного полимера [19] и обычно находится в виде гранул.Для модулирования свойств полимера можно использовать различные крахмалы и процентные содержания. В ряде исследований сообщается о разработке биоразлагаемого полимера путем включения крахмала в ПЭНП и о характеристиках этих синтезированных полимеров [20–27]. Эти исследования в основном были сосредоточены на изучении влияния содержания крахмала и т.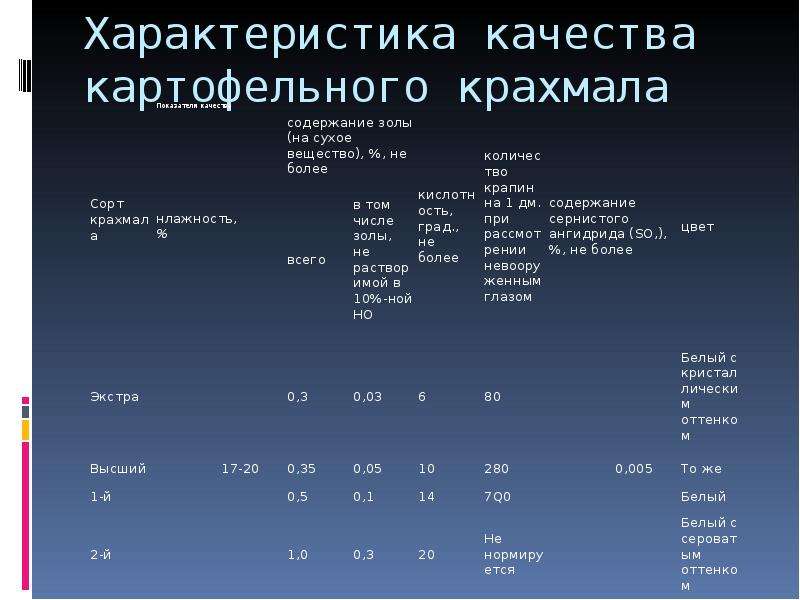 д. на механические свойства и свойства разложения полимера. Однако до сих пор слишком мало внимания уделялось оценке эффектов процессов модификации (например,г., добавление сшивающего агента и облучение электронным пучком) на механические и термические свойства полимера. В этом исследовании, помимо влияния содержания крахмала на механические характеристики и характеристики разложения крахмала саго, изучалось влияние сшивания триметилолпропантриакрилатом (ТМПТА) и облучения электронным пучком (ЭП) на механические и термические свойства полимера. включенный полимер LDPE.
д. на механические свойства и свойства разложения полимера. Однако до сих пор слишком мало внимания уделялось оценке эффектов процессов модификации (например,г., добавление сшивающего агента и облучение электронным пучком) на механические и термические свойства полимера. В этом исследовании, помимо влияния содержания крахмала на механические характеристики и характеристики разложения крахмала саго, изучалось влияние сшивания триметилолпропантриакрилатом (ТМПТА) и облучения электронным пучком (ЭП) на механические и термические свойства полимера. включенный полимер LDPE.
2. Материалы и экспериментальные методы
2.1. Синтез полимера
На 1-й фазе эксперимента были получены пять типов образцов полимера ПЭНП в сочетании с различным процентным содержанием крахмала. Полиэтилен низкой плотности (LDPE) и крахмал саго (Igan Sago Industries Sdn. Bhd.) взвешивали на весах с вертикальной загрузкой (AND, модель GF-3000) с различным процентным содержанием LDPE и крахмала, как указано в таблице 1.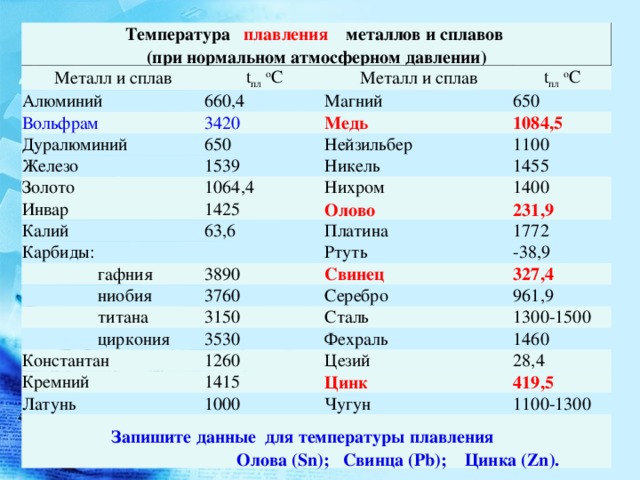 Взвешенные LDPE и крахмал предварительно смешивали и смешивали в смесителе Брабендера в течение шести минут при 135°С. Смеси, полученные из брабендера, затем переносили в гидравлическую машину (Lab Tech) для прессования.Процесс сжатия включал четыре этапа: предварительный нагрев, вентиляцию, прессование и охлаждение. Первые три этапа включали горячее прессование, а последний этап – холодное прессование. Образцы были помещены в середину квадратной стальной рамы, которая затем была зажата между двумя другими стальными пластинами. Между этими тремя слоями более толстых пластин находились две более тонкие и гладкие стальные пластины. Листы полиэтилентерефталата (ПЭТФ) использовали между поверхностью полимера и стальной пластиной, чтобы предотвратить прилипание образцов полимера к стальной пластине.Температура формования и давление составляли 150°С и 10 МПа соответственно. Процессы горячего и холодного прессования проводились на одном и том же станке, но в разных формах. При горячем прессовании, которое производилось в верхней части машины, образцы переносились в нижнюю часть для холодного прессования.
Взвешенные LDPE и крахмал предварительно смешивали и смешивали в смесителе Брабендера в течение шести минут при 135°С. Смеси, полученные из брабендера, затем переносили в гидравлическую машину (Lab Tech) для прессования.Процесс сжатия включал четыре этапа: предварительный нагрев, вентиляцию, прессование и охлаждение. Первые три этапа включали горячее прессование, а последний этап – холодное прессование. Образцы были помещены в середину квадратной стальной рамы, которая затем была зажата между двумя другими стальными пластинами. Между этими тремя слоями более толстых пластин находились две более тонкие и гладкие стальные пластины. Листы полиэтилентерефталата (ПЭТФ) использовали между поверхностью полимера и стальной пластиной, чтобы предотвратить прилипание образцов полимера к стальной пластине.Температура формования и давление составляли 150°С и 10 МПа соответственно. Процессы горячего и холодного прессования проводились на одном и том же станке, но в разных формах. При горячем прессовании, которое производилось в верхней части машины, образцы переносились в нижнюю часть для холодного прессования. Для этих образцов 1-й фазы были проведены механические испытания и испытания на биоразложение.
Для этих образцов 1-й фазы были проведены механические испытания и испытания на биоразложение.
На втором этапе исследовали влияние сшивания триметилолпропантриакрилатом (ТМПТА) и облучения электронным пучком (ЭП) на механические и термические свойства образцов полимера.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||




 C6H12O6 → 2CH₃―CHOH―COOH (молочная кислота)
C6H12O6 → 2CH₃―CHOH―COOH (молочная кислота) ) ( горит.)
) ( горит.) 

 Этические лекарства, 6-е издание, 1982 г.», под редакцией Японского фармацевтического информационного центра. 6 (1982), 805.
Этические лекарства, 6-е издание, 1982 г.», под редакцией Японского фармацевтического информационного центра. 6 (1982), 805. Метаболизм мальтозы дрожжами во время ферментации приводит к образованию этанола и углекислого газа.
Метаболизм мальтозы дрожжами во время ферментации приводит к образованию этанола и углекислого газа. Чтобы избежать перегрузки данных, образцы полимера, использованные в экспериментах второй фазы, состояли из 50% полиэтилена низкой плотности и 50% крахмала. Различные проценты ТМФТА добавляли к смесям ПЭНП-крахмал в процессе смешивания, а затем облучали соответственно различными дозами ЭБ, как показано в таблице 2. После сшивания образцы полимера прессовали под гидравлической машиной и облучали ЭБ в дозах 10 кГр, 30 кГр, 50 кГр, 70 кГр и 100 кГр. Энергия и ток были установлены на 1.5 МэВ и 30 мА соответственно.
Чтобы избежать перегрузки данных, образцы полимера, использованные в экспериментах второй фазы, состояли из 50% полиэтилена низкой плотности и 50% крахмала. Различные проценты ТМФТА добавляли к смесям ПЭНП-крахмал в процессе смешивания, а затем облучали соответственно различными дозами ЭБ, как показано в таблице 2. После сшивания образцы полимера прессовали под гидравлической машиной и облучали ЭБ в дозах 10 кГр, 30 кГр, 50 кГр, 70 кГр и 100 кГр. Энергия и ток были установлены на 1.5 МэВ и 30 мА соответственно.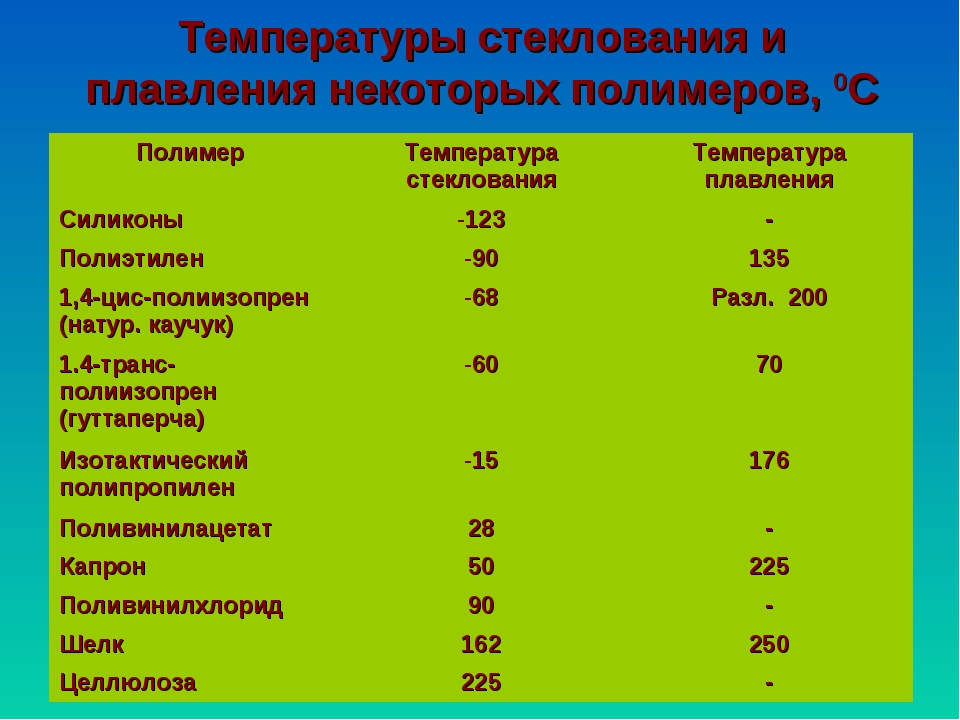 2. Подготовка образцов: резка в форме колокола
2. Подготовка образцов: резка в форме колокола Для каждого типа полимера было испытано по пять образцов. Модуль Юнга рассчитывали как отношение напряжения к деформации для оценки механических свойств образцов полимера.Тест Стьюдента t был выполнен для сравнения средних значений из всех независимых выборочных групп с использованием статистического программного обеспечения Minitab версии 12.2 (Minitab Inc., Государственный колледж, Пенсильвания, США) при уровне значимости 0,05.
Для каждого типа полимера было испытано по пять образцов. Модуль Юнга рассчитывали как отношение напряжения к деформации для оценки механических свойств образцов полимера.Тест Стьюдента t был выполнен для сравнения средних значений из всех независимых выборочных групп с использованием статистического программного обеспечения Minitab версии 12.2 (Minitab Inc., Государственный колледж, Пенсильвания, США) при уровне значимости 0,05. После одного месяца захоронения образцы выкапывали и очищали, чтобы обеспечить полное удаление почвы/ила.Затем образцы помещали в помещение с достаточной вентиляцией для естественной сушки. Высушенные деградированные образцы взвешивали на тех же электронных весах, что и перед началом деструкции. Затем процент потери массы соответствующего образца измеряли следующим образом: где — начальная масса (т. е. масса до разложения) и — конечная масса (т. е. масса после разложения).
После одного месяца захоронения образцы выкапывали и очищали, чтобы обеспечить полное удаление почвы/ила.Затем образцы помещали в помещение с достаточной вентиляцией для естественной сушки. Высушенные деградированные образцы взвешивали на тех же электронных весах, что и перед началом деструкции. Затем процент потери массы соответствующего образца измеряли следующим образом: где — начальная масса (т. е. масса до разложения) и — конечная масса (т. е. масса после разложения). Анализ ДСК дает точку плавления полимера.
Анализ ДСК дает точку плавления полимера. Кроме того, присутствие/поглощение влаги крахмалом на границе ПЭНП-крахмал ослабляет слабую межфазную адгезию. Следовательно, гранулы крахмала не удлиняются вместе с ПЭНП и, таким образом, вызывают легкое образование и/или распространение трещин, что в конечном итоге приводит к разрушению образца полимера при более низких значениях удлинения. Рисунок 1 показывает, что падение удлинения полимера при разрыве становится более заметным по мере того, как процентное содержание крахмала увеличивается.Это может быть связано с тем, что при более высоком содержании крахмала взаимодействие наполнителя с наполнителем становится более выраженным, чем взаимодействие наполнителя с матрицей, что снижает эффективную площадь поперечного сечения образца полимера, вызванное присутствием частиц крахмала. Приложенное напряжение не передается соответствующим образом от полимерной матрицы к жестким частицам крахмала, и, следовательно, эффективное напряжение, испытываемое матрицей, существенно выше [19].
Кроме того, присутствие/поглощение влаги крахмалом на границе ПЭНП-крахмал ослабляет слабую межфазную адгезию. Следовательно, гранулы крахмала не удлиняются вместе с ПЭНП и, таким образом, вызывают легкое образование и/или распространение трещин, что в конечном итоге приводит к разрушению образца полимера при более низких значениях удлинения. Рисунок 1 показывает, что падение удлинения полимера при разрыве становится более заметным по мере того, как процентное содержание крахмала увеличивается.Это может быть связано с тем, что при более высоком содержании крахмала взаимодействие наполнителя с наполнителем становится более выраженным, чем взаимодействие наполнителя с матрицей, что снижает эффективную площадь поперечного сечения образца полимера, вызванное присутствием частиц крахмала. Приложенное напряжение не передается соответствующим образом от полимерной матрицы к жестким частицам крахмала, и, следовательно, эффективное напряжение, испытываемое матрицей, существенно выше [19]. 2).Как уже упоминалось, с увеличением содержания крахмала взаимодействие наполнителя с наполнителем становится более выраженным, чем взаимодействие наполнителя с матрицей, что приводит к агломерации гранул крахмала, которые по своей природе являются более жесткими или более жесткими, чем матрица ПЭНП [28]. Общеизвестно, что жесткий наполнитель увеличивает модуль смеси даже в том случае, когда истинное армирование не происходит [24]. Поэтому считается, что увеличение модуля полимерной смеси с увеличением содержания крахмала связано с более высокой жесткостью гранул крахмала.
2).Как уже упоминалось, с увеличением содержания крахмала взаимодействие наполнителя с наполнителем становится более выраженным, чем взаимодействие наполнителя с матрицей, что приводит к агломерации гранул крахмала, которые по своей природе являются более жесткими или более жесткими, чем матрица ПЭНП [28]. Общеизвестно, что жесткий наполнитель увеличивает модуль смеси даже в том случае, когда истинное армирование не происходит [24]. Поэтому считается, что увеличение модуля полимерной смеси с увеличением содержания крахмала связано с более высокой жесткостью гранул крахмала.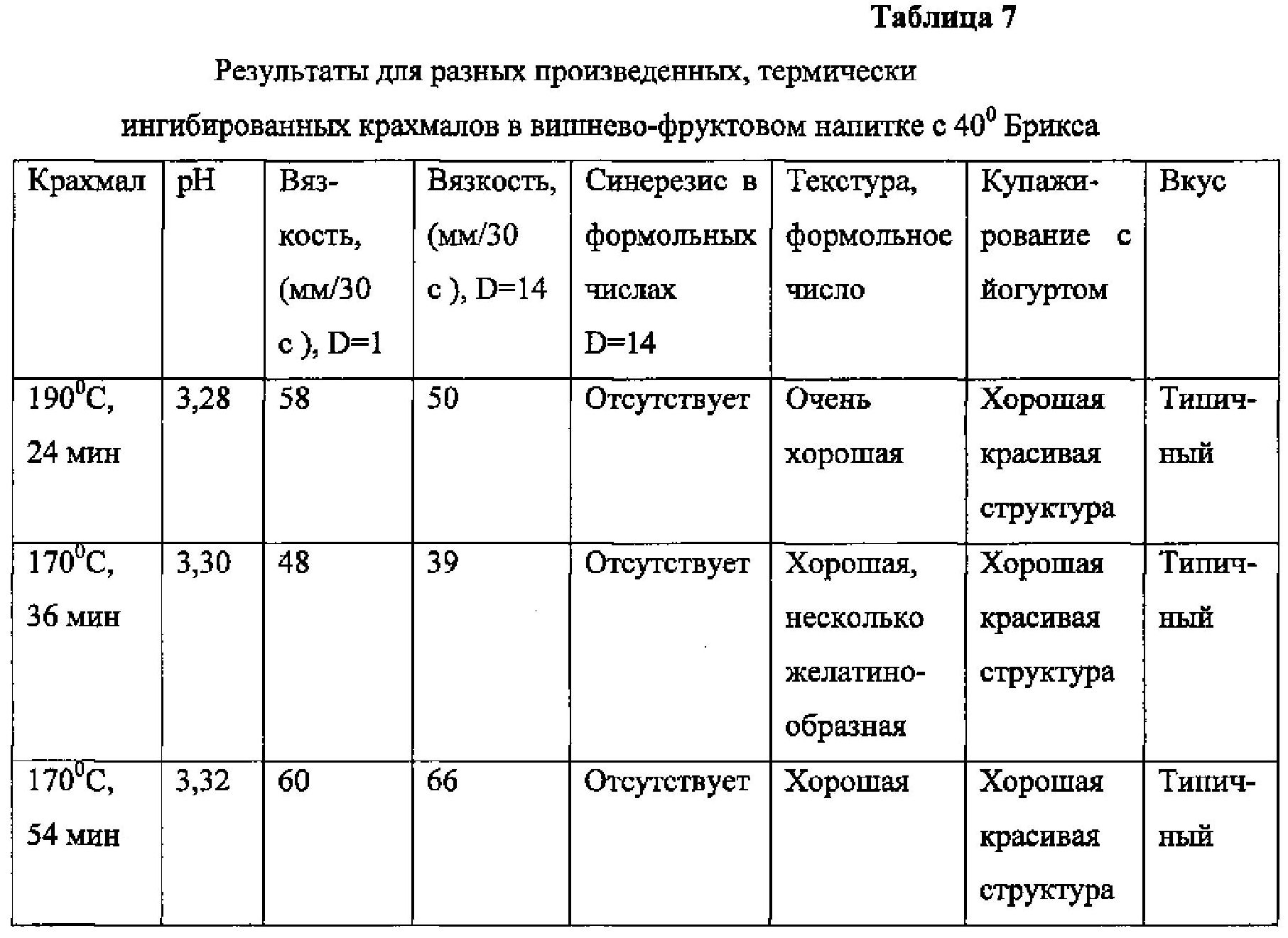 Например, удлинение стало более жестким, что привело к более высокому модулю Юнга.Однако подробное объяснение этих явлений может быть подтверждено интенсивным анализом прочности связи, который выходит за рамки данного предварительного исследования.
Например, удлинение стало более жестким, что привело к более высокому модулю Юнга.Однако подробное объяснение этих явлений может быть подтверждено интенсивным анализом прочности связи, который выходит за рамки данного предварительного исследования.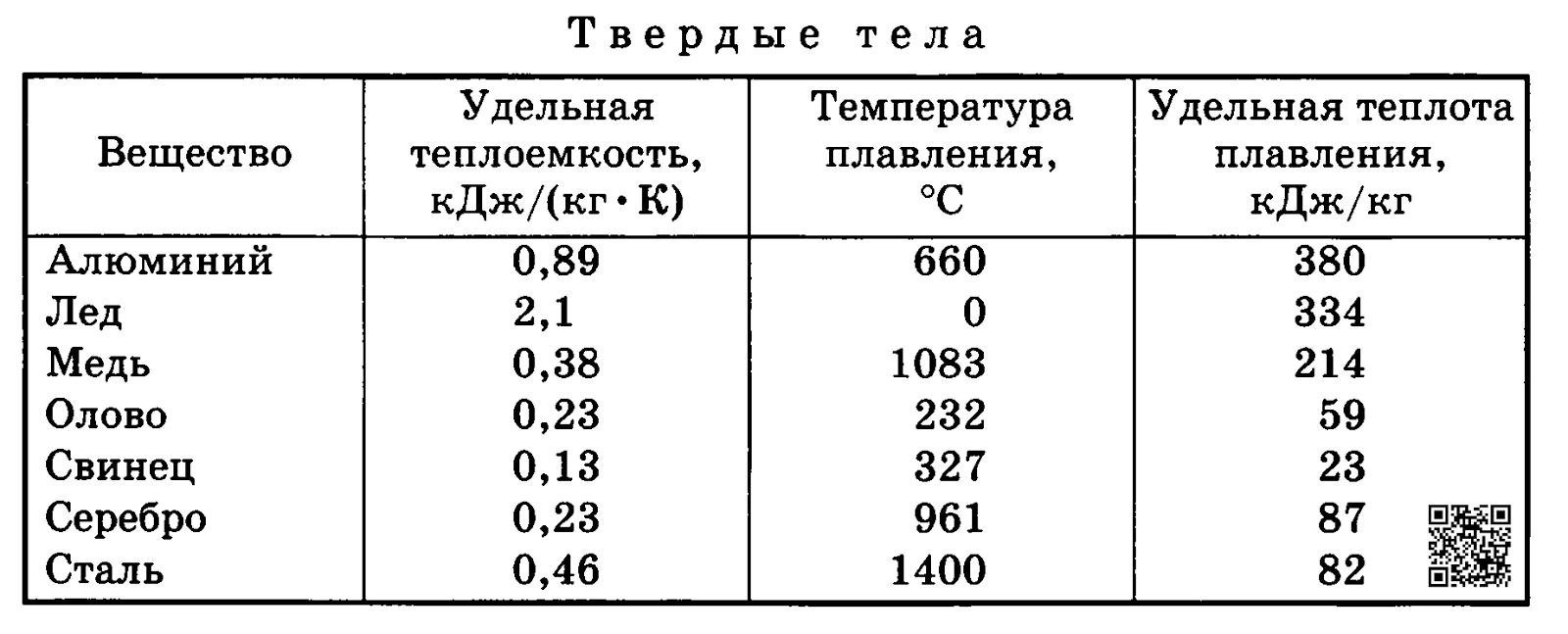 00
00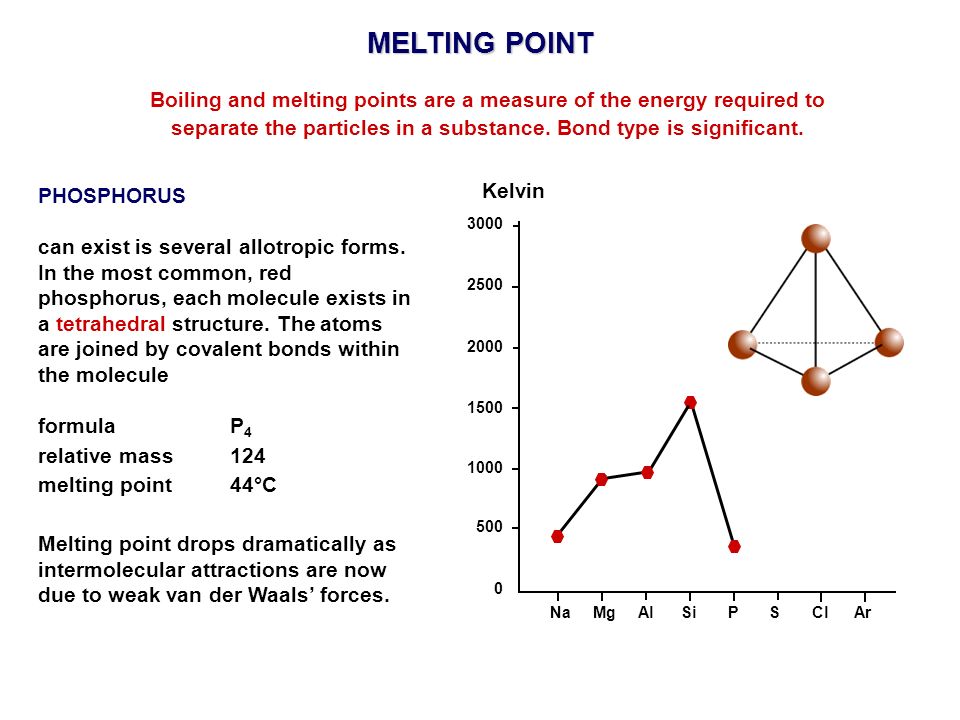 Образцы полимера ПЭНП, содержащие 30%, 50% и 70% крахмала, продемонстрировали потерю массы в 3 раза.81%, 5,37% и 11,07% соответственно. Эти результаты показывают, что более высокое содержание крахмала улучшает кинетику деградации и, таким образом, увеличивает потерю массы. Это может быть связано с гидрофильной природой крахмала, что было доказано в другом исследовании [6]. Крахмал, будучи гидрофильным по своей природе, удерживает влагу, что способствует разложению полимера. Чем выше содержание крахмала в полимере, тем выше содержание влаги, что приводит к более быстрому разложению. Наблюдалось физическое изменение общей морфологии образца полимера; например, поверхность за период деградации стала шероховатой, как показано на рисунке 6.Повышенное содержание крахмала привело к более высокой шероховатости поверхности образцов из-за повышенной деградации. Потеря веса и изменение внешнего вида (т. е. шероховатости поверхности) образца в почве можно рассматривать как свидетельство биодеградации этого полимера на свалках или в природной среде.
Образцы полимера ПЭНП, содержащие 30%, 50% и 70% крахмала, продемонстрировали потерю массы в 3 раза.81%, 5,37% и 11,07% соответственно. Эти результаты показывают, что более высокое содержание крахмала улучшает кинетику деградации и, таким образом, увеличивает потерю массы. Это может быть связано с гидрофильной природой крахмала, что было доказано в другом исследовании [6]. Крахмал, будучи гидрофильным по своей природе, удерживает влагу, что способствует разложению полимера. Чем выше содержание крахмала в полимере, тем выше содержание влаги, что приводит к более быстрому разложению. Наблюдалось физическое изменение общей морфологии образца полимера; например, поверхность за период деградации стала шероховатой, как показано на рисунке 6.Повышенное содержание крахмала привело к более высокой шероховатости поверхности образцов из-за повышенной деградации. Потеря веса и изменение внешнего вида (т. е. шероховатости поверхности) образца в почве можно рассматривать как свидетельство биодеградации этого полимера на свалках или в природной среде.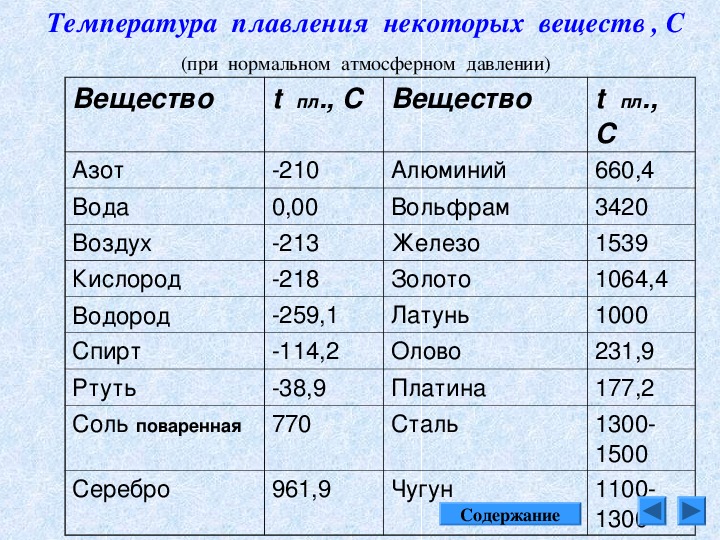 Результаты показывают, что включение гидрофильного крахмала в гидрофобный ПЭНП повышает гидрофильность и способность к разложению всего полимера. Подобные явления деградации ПЭНП, инкорпорированного крахмалом, наблюдались и в ряде других исследований [20, 25, 27].Таким образом, характеристики разложения полимера ПЭНП с примесью крахмала можно регулировать, манипулируя содержанием крахмала в полимере. Действительно, полимер должен быть разработан с по существу контролируемой характеристикой разложения при сохранении требуемой прочности полимерного объекта в течение его расчетного срока службы для конкретного применения.
Результаты показывают, что включение гидрофильного крахмала в гидрофобный ПЭНП повышает гидрофильность и способность к разложению всего полимера. Подобные явления деградации ПЭНП, инкорпорированного крахмалом, наблюдались и в ряде других исследований [20, 25, 27].Таким образом, характеристики разложения полимера ПЭНП с примесью крахмала можно регулировать, манипулируя содержанием крахмала в полимере. Действительно, полимер должен быть разработан с по существу контролируемой характеристикой разложения при сохранении требуемой прочности полимерного объекта в течение его расчетного срока службы для конкретного применения.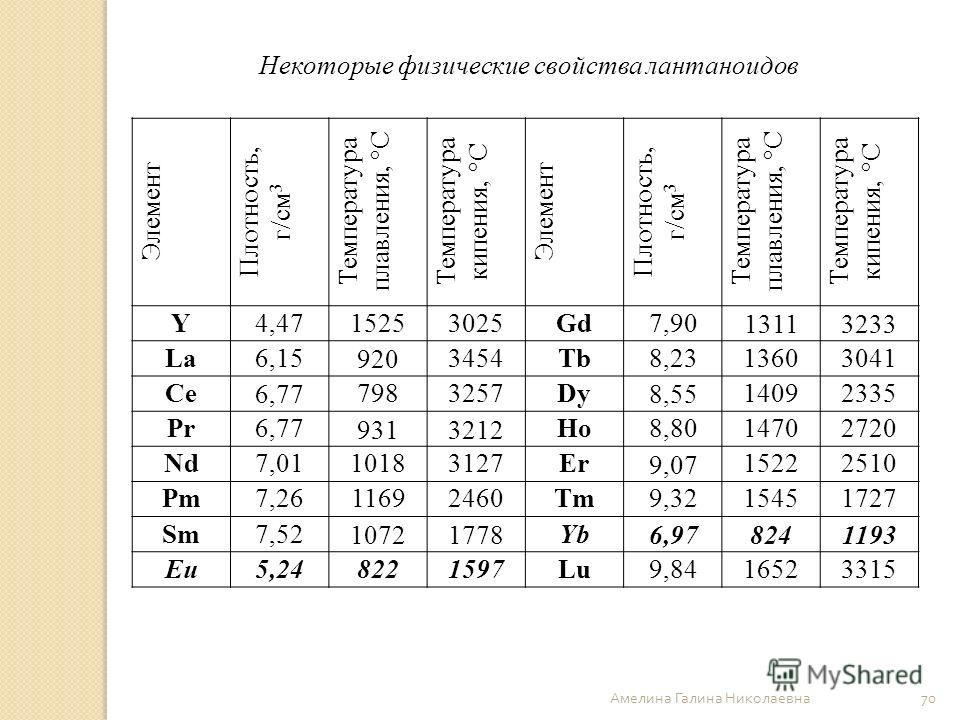 Прочность полимера (т.е. модуль Юнга) увеличивалась с увеличением содержания крахмала, процентного содержания ТМФТА и дозы облучения ЭБ, а пластичность полимера снижалась с увеличением указанных параметров.Температура плавления снижалась с увеличением процентного содержания ТМФТА и дозы облучения ЭБ. Деструкция полимера усиливалась с увеличением содержания крахмала. В заключение, свойства полимера ПЭНП с включенным крахмалом можно модулировать, манипулируя содержанием крахмала и процессами модификации (например, сшивающим агентом TMPTA и дозой облучения ЭБ) для индивидуальных применений.
Прочность полимера (т.е. модуль Юнга) увеличивалась с увеличением содержания крахмала, процентного содержания ТМФТА и дозы облучения ЭБ, а пластичность полимера снижалась с увеличением указанных параметров.Температура плавления снижалась с увеличением процентного содержания ТМФТА и дозы облучения ЭБ. Деструкция полимера усиливалась с увеличением содержания крахмала. В заключение, свойства полимера ПЭНП с включенным крахмалом можно модулировать, манипулируя содержанием крахмала и процессами модификации (например, сшивающим агентом TMPTA и дозой облучения ЭБ) для индивидуальных применений. Наша цель
заключается в проведении высококачественных исследований в максимально широком
аудитория.
Наша цель
заключается в проведении высококачественных исследований в максимально широком
аудитория. Ты
может получить личную / институциональную подписку на перечисленные
журналы непосредственно из Science Alert. В качестве альтернативы вы
возможно, вы захотите связаться с предпочитаемым агентством по подписке.Пожалуйста, направляйте заказы, платежи и запросы в службу поддержки клиентов
в службу поддержки клиентов журнала Science Alert.
Ты
может получить личную / институциональную подписку на перечисленные
журналы непосредственно из Science Alert. В качестве альтернативы вы
возможно, вы захотите связаться с предпочитаемым агентством по подписке.Пожалуйста, направляйте заказы, платежи и запросы в службу поддержки клиентов
в службу поддержки клиентов журнала Science Alert. В соответствии с характером вопросов мы разделили часто задаваемые вопросы на разные категории.
В соответствии с характером вопросов мы разделили часто задаваемые вопросы на разные категории. При диспергировании в избытке воды при комнатной температуре гранулы крахмала поглощают только около 30–40% своего сухого веса в виде влаги, заставляя их слегка набухать и оседать на дно. Однако этот процесс можно обратить вспять.
При диспергировании в избытке воды при комнатной температуре гранулы крахмала поглощают только около 30–40% своего сухого веса в виде влаги, заставляя их слегка набухать и оседать на дно. Однако этот процесс можно обратить вспять. 1,2
1,2  По этой причине рецепты для выпечки, богатые сахаром и жиром и с низким содержанием воды, такие как корочки для пирогов и печенье, никогда не достигают полной желатинизации крахмала.
По этой причине рецепты для выпечки, богатые сахаром и жиром и с низким содержанием воды, такие как корочки для пирогов и печенье, никогда не достигают полной желатинизации крахмала. Н. «Крахмалы: молекулярная и гранулярная структура и свойства». Химия углеводов для ученых-пищевиков, 3-е издание, AACCI and Elsevier Inc., 2019 г., стр. 159–182.
Н. «Крахмалы: молекулярная и гранулярная структура и свойства». Химия углеводов для ученых-пищевиков, 3-е издание, AACCI and Elsevier Inc., 2019 г., стр. 159–182.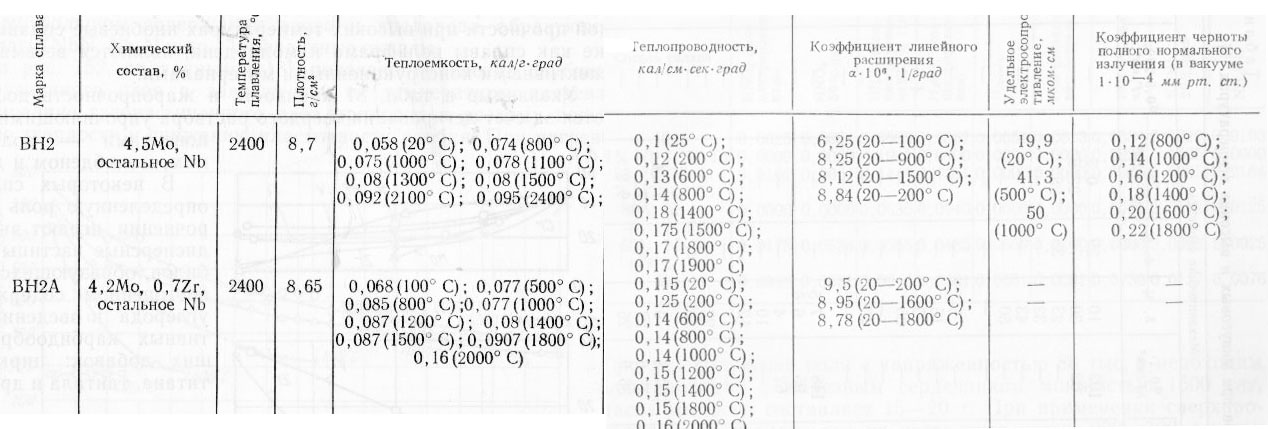 Каркасы должны обеспечивать временную поддержку и быть в состоянии выдерживать внешнюю нагрузку до того, как созреет внеклеточный матрикс клеток. PCL, обладающий хорошими механическими свойствами и способный к биорезорбции, может использоваться для некоторых из этих применений (4, 5).
Каркасы должны обеспечивать временную поддержку и быть в состоянии выдерживать внешнюю нагрузку до того, как созреет внеклеточный матрикс клеток. PCL, обладающий хорошими механическими свойствами и способный к биорезорбции, может использоваться для некоторых из этих применений (4, 5). Температура плавления полимерных строительных материалов низкая; для ПКЛ (5) она составляет 55–60°С. Свойства материала при температурах, близких к температуре его плавления, отличаются от свойств при температуре окружающей среды.Наш предыдущий отчет о PCL показал, что механические свойства гомополимера действительно значительно изменились, когда он подвергается воздействию температуры тела (9). В соответствии с этим весьма вероятно, что он ведет себя аналогичным образом при использовании в качестве матрицы и, следовательно, влияет на свойства композита. Поэтому необходимо исследование механических свойств композита ПКЛ/крахмал при различных скоростях деформации и температуре тела. В частности, учитывая, что каркасы должны выдерживать нагрузку без деформации, представляет интерес анализ упругого поведения композита ниже предела текучести.
Температура плавления полимерных строительных материалов низкая; для ПКЛ (5) она составляет 55–60°С. Свойства материала при температурах, близких к температуре его плавления, отличаются от свойств при температуре окружающей среды.Наш предыдущий отчет о PCL показал, что механические свойства гомополимера действительно значительно изменились, когда он подвергается воздействию температуры тела (9). В соответствии с этим весьма вероятно, что он ведет себя аналогичным образом при использовании в качестве матрицы и, следовательно, влияет на свойства композита. Поэтому необходимо исследование механических свойств композита ПКЛ/крахмал при различных скоростях деформации и температуре тела. В частности, учитывая, что каркасы должны выдерживать нагрузку без деформации, представляет интерес анализ упругого поведения композита ниже предела текучести. Некоторые примеры включают исследование механического поведения полиолефинов (10, 11), поликарбоната (12), полиметилметакрилата (12), полиэтилентерефталата (13) и гидрогелей (14) среди прочих. Очевидно, что в указанном широком диапазоне деформаций эластичные свойства при малых деформациях легко изменяются.Таким образом, эта работа предназначена для сообщения об упругих свойствах композита ПКЛ/крахмала при различных скоростях деформации и температурах.
Некоторые примеры включают исследование механического поведения полиолефинов (10, 11), поликарбоната (12), полиметилметакрилата (12), полиэтилентерефталата (13) и гидрогелей (14) среди прочих. Очевидно, что в указанном широком диапазоне деформаций эластичные свойства при малых деформациях легко изменяются.Таким образом, эта работа предназначена для сообщения об упругих свойствах композита ПКЛ/крахмала при различных скоростях деформации и температурах. , Easton , Пенсильвания, США) к штампам ASTM D638 тип V. Скорость сдвига устанавливали на 80 об/мин, перемешивание проводили в течение 8 мин. Для испытания на растяжение использовали H5KT (Tinius Olsen, Horsham, PA, USA) с тензодатчиком 5 кН.Были назначены скорости растяжения 5 мм/мин, 0,1 мм/мин и 0,01 мм/мин. При определении верхнего предела учитывали рекомендацию стандарта, предполагающую скорость тестирования 1–5 мм/мин. Предполагалось, что это диапазон скоростей для проведения механических испытаний твердых полимеров, а также он используется для испытаний пористых каркасных конструкций. В качестве нижнего предела был выбран предел чувствительности машины для испытаний на растяжение (0,01 мм/мин). Скорость 0,1 мм/мин представляет собой порядок между верхним и нижним пределами.Испытание на растяжение проводили при комнатной температуре 23±2°С, а также при повышенной температуре (тела человека). Для повышения температуры образца до 37 ± 2 °C использовался лучистый нагреватель, при этом гарантируя, что изоляция не оказывает прямого воздействия на тензодатчик машины для испытаний на растяжение.
, Easton , Пенсильвания, США) к штампам ASTM D638 тип V. Скорость сдвига устанавливали на 80 об/мин, перемешивание проводили в течение 8 мин. Для испытания на растяжение использовали H5KT (Tinius Olsen, Horsham, PA, USA) с тензодатчиком 5 кН.Были назначены скорости растяжения 5 мм/мин, 0,1 мм/мин и 0,01 мм/мин. При определении верхнего предела учитывали рекомендацию стандарта, предполагающую скорость тестирования 1–5 мм/мин. Предполагалось, что это диапазон скоростей для проведения механических испытаний твердых полимеров, а также он используется для испытаний пористых каркасных конструкций. В качестве нижнего предела был выбран предел чувствительности машины для испытаний на растяжение (0,01 мм/мин). Скорость 0,1 мм/мин представляет собой порядок между верхним и нижним пределами.Испытание на растяжение проводили при комнатной температуре 23±2°С, а также при повышенной температуре (тела человека). Для повышения температуры образца до 37 ± 2 °C использовался лучистый нагреватель, при этом гарантируя, что изоляция не оказывает прямого воздействия на тензодатчик машины для испытаний на растяжение. Перед испытаниями на растяжение применяли кондиционирование образцов путем предварительного нагрева при соответствующей температуре в течение не менее 4 ч. Были проанализированы кривые напряжение-деформация до точки перегиба.
Перед испытаниями на растяжение применяли кондиционирование образцов путем предварительного нагрева при соответствующей температуре в течение не менее 4 ч. Были проанализированы кривые напряжение-деформация до точки перегиба. Дисперсионный анализ (ANOVA) каждого экспериментального результата использовался для измерения значимости каждой входной переменной наряду с возможным взаимодействием между переменными. Вероятностное значение Prob > F , равное 0,05, было критерием для определения переменной как значимой. Для планирования экспериментов и расчета результатов использовали коммерчески доступный пакет программного обеспечения для статистики (Design Expert, Stat-Ease, Inc., Миннеаполис, Миннесота, США).
Дисперсионный анализ (ANOVA) каждого экспериментального результата использовался для измерения значимости каждой входной переменной наряду с возможным взаимодействием между переменными. Вероятностное значение Prob > F , равное 0,05, было критерием для определения переменной как значимой. Для планирования экспериментов и расчета результатов использовали коммерчески доступный пакет программного обеспечения для статистики (Design Expert, Stat-Ease, Inc., Миннеаполис, Миннесота, США). е. коэффициентом Пуассона и модулем Юнга. Входные данные для упругих свойств материала включали значения, связанные со скоростями деформации и температурами. После этого к модели применялась нагрузка, и наблюдались величина и распределение деформации.
е. коэффициентом Пуассона и модулем Юнга. Входные данные для упругих свойств материала включали значения, связанные со скоростями деформации и температурами. После этого к модели применялась нагрузка, и наблюдались величина и распределение деформации. 2) выявило промежутки между его составляющими, что свидетельствует о несмешиваемости. Учитывая, что PCL/S10 показал более высокую жесткость и был лишь немного слабее, чем PCL, композит PCL/S10 был выбран для дальнейшего анализа.
2) выявило промежутки между его составляющими, что свидетельствует о несмешиваемости. Учитывая, что PCL/S10 показал более высокую жесткость и был лишь немного слабее, чем PCL, композит PCL/S10 был выбран для дальнейшего анализа. Эта предельная разница возникает при любой заданной температуре. Предел текучести и модуль упругости композита PCL/крахмал прямо пропорциональны скорости деформации, но обратно пропорциональны температуре. Количественно, уменьшая скорость деформации с 5 до 0.01 мм/мин снижает прочность и модуль упругости композита до 12% и 17% соответственно. Также при повышении температуры от комнатной до температуры тела человека предел текучести и модуль упругости композита снижаются до 35% и 25% соответственно. Значения находятся в аналогичном диапазоне для гомополимера PCL (9), что означает, что добавление до 10 мас.% крахмала на самом деле не изменило механические свойства матрицы (с точки зрения прочности, жесткости и удлинения) или изменение упругое поведение матрицы при различных скоростях деформации и температурах.
Эта предельная разница возникает при любой заданной температуре. Предел текучести и модуль упругости композита PCL/крахмал прямо пропорциональны скорости деформации, но обратно пропорциональны температуре. Количественно, уменьшая скорость деформации с 5 до 0.01 мм/мин снижает прочность и модуль упругости композита до 12% и 17% соответственно. Также при повышении температуры от комнатной до температуры тела человека предел текучести и модуль упругости композита снижаются до 35% и 25% соответственно. Значения находятся в аналогичном диапазоне для гомополимера PCL (9), что означает, что добавление до 10 мас.% крахмала на самом деле не изменило механические свойства матрицы (с точки зрения прочности, жесткости и удлинения) или изменение упругое поведение матрицы при различных скоростях деформации и температурах.
 1
1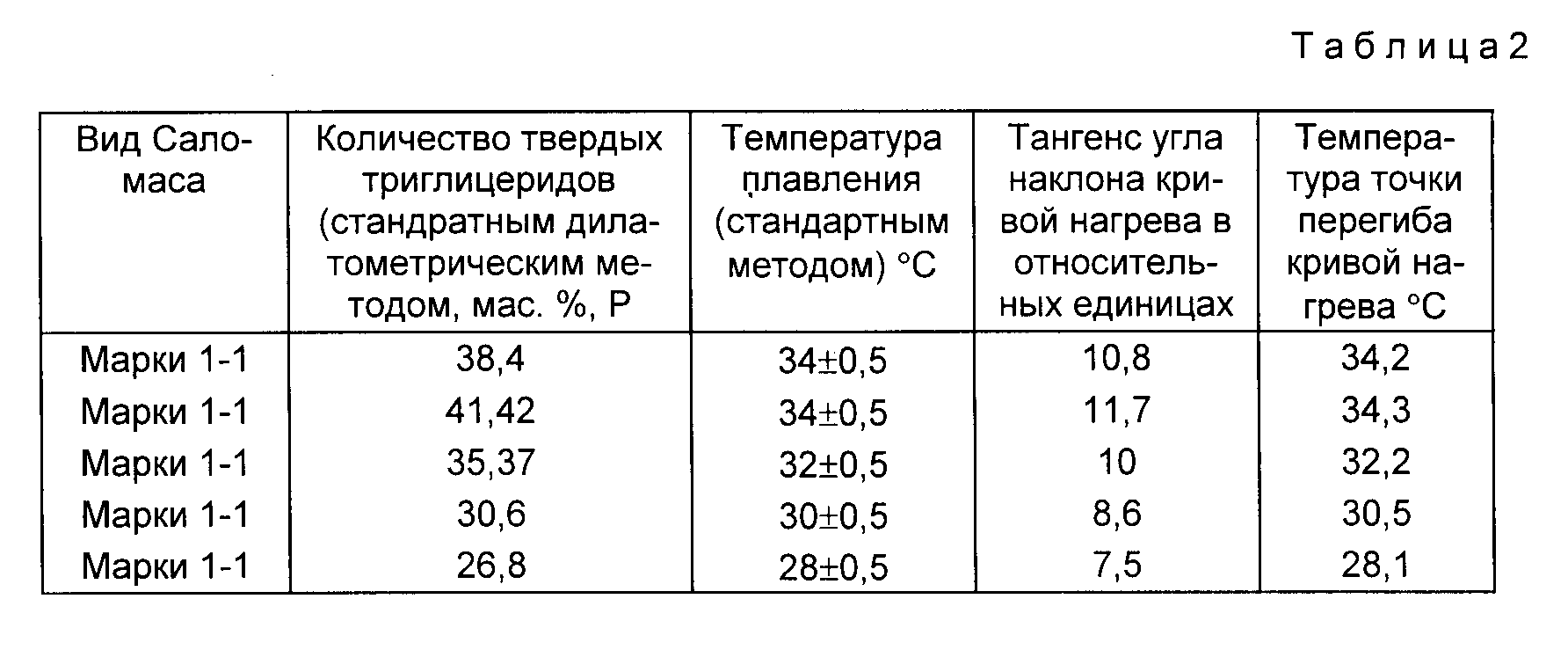 4:
4: Более высокая температура плавления и более высокая кристалличность часто означают более высокие механические свойства полукристаллических полимеров. Суммарный эффект более высокой температуры плавления и более низкой кристалличности PCL в композите, по-видимому, вызывает общее упругое поведение композита и аналогично поведению матрицы. Тенденция небольшой разницы в упругом поведении между 0.Скорость деформации 1 и 0,01 мм/мин при обеих температурах указывает на наличие уровня насыщения скорости деформации, ниже которого снижение упругих свойств незначительно.
Более высокая температура плавления и более высокая кристалличность часто означают более высокие механические свойства полукристаллических полимеров. Суммарный эффект более высокой температуры плавления и более низкой кристалличности PCL в композите, по-видимому, вызывает общее упругое поведение композита и аналогично поведению матрицы. Тенденция небольшой разницы в упругом поведении между 0.Скорость деформации 1 и 0,01 мм/мин при обеих температурах указывает на наличие уровня насыщения скорости деформации, ниже которого снижение упругих свойств незначительно. Тем не менее, в этом исследовании используется анализ конечных элементов, чтобы дополнить точки данных и одновременно проверить вывод.
Тем не менее, в этом исследовании используется анализ конечных элементов, чтобы дополнить точки данных и одновременно проверить вывод. Расчетная жесткость конкретного композита при 30°С при растяжении с нагрузкой 5, 0,1 и 0,01 мм/мин составляет 103, 89 и 88 МПа соответственно. Эти значения разумно находятся в пределах измеренного диапазона жесткости.
Расчетная жесткость конкретного композита при 30°С при растяжении с нагрузкой 5, 0,1 и 0,01 мм/мин составляет 103, 89 и 88 МПа соответственно. Эти значения разумно находятся в пределах измеренного диапазона жесткости. 43
43 Распределение деформации была не линейной, что указывает на наличие различных скоростях деформации. Это похоже на нахождение аналогичного эксперимента по PCL гомополимера (7).
Распределение деформации была не линейной, что указывает на наличие различных скоростях деформации. Это похоже на нахождение аналогичного эксперимента по PCL гомополимера (7).
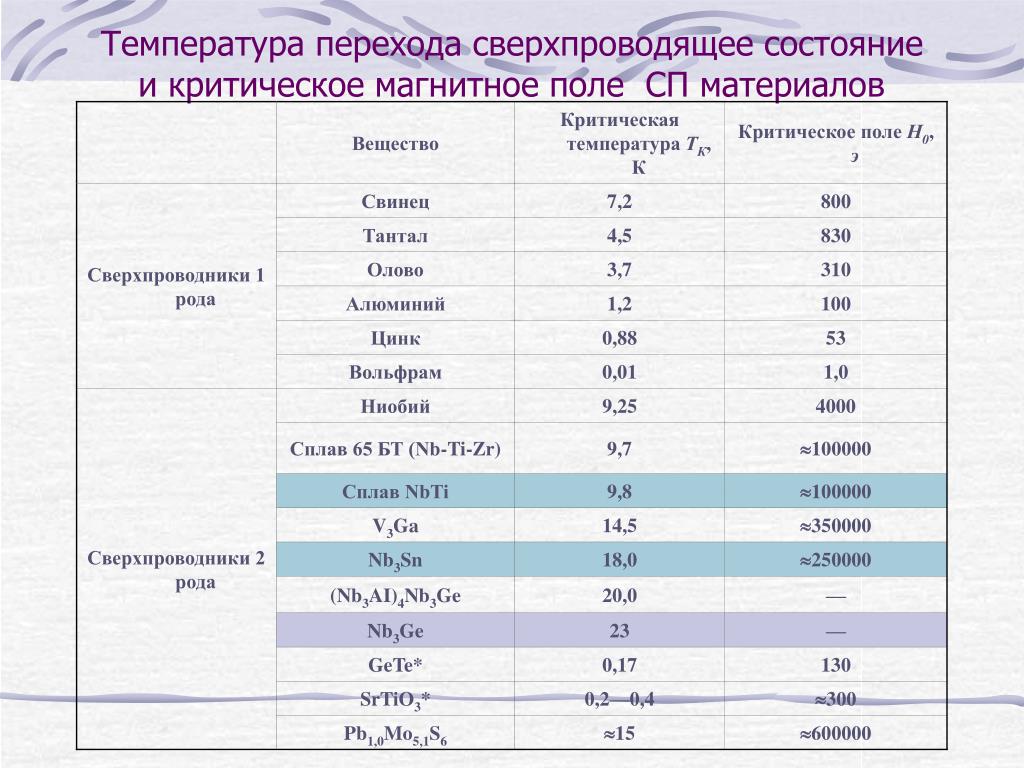 Детали анализа методом конечных элементов были ранее сообщалось (9). Следует отметить, что присвоены свойства материалов в конечно-элементной модели, включая модели с пористой архитектурой, которые получаются из их твердой формы. Модели присваиваются иметь элементарную ячейку простой кубического, которая является технологичной с использованием твердых методов в свободной форме.Упругие свойства композитов PCL/крахмал при различных температурах и скоростях деформации были заданными входными параметрами. Каркас был затем загружен на сжатие, пока напряжение не достигнет 5%. Рассчитываются распределение напряжений по помосту (рис 7) показало широкий спектр модуля упругости поперек каркаса. Разница распределения напряжений достигает почти 50%. Варьирование напряжение и деформация, которые произошли в течение каркасной конструкции во время загрузки могут быть отнесены к комбинации между эффектом пористой конструкции эшафоте и механическими свойствами композита при различных скоростях деформации (9, 22, 23).
Детали анализа методом конечных элементов были ранее сообщалось (9). Следует отметить, что присвоены свойства материалов в конечно-элементной модели, включая модели с пористой архитектурой, которые получаются из их твердой формы. Модели присваиваются иметь элементарную ячейку простой кубического, которая является технологичной с использованием твердых методов в свободной форме.Упругие свойства композитов PCL/крахмал при различных температурах и скоростях деформации были заданными входными параметрами. Каркас был затем загружен на сжатие, пока напряжение не достигнет 5%. Рассчитываются распределение напряжений по помосту (рис 7) показало широкий спектр модуля упругости поперек каркаса. Разница распределения напряжений достигает почти 50%. Варьирование напряжение и деформация, которые произошли в течение каркасной конструкции во время загрузки могут быть отнесены к комбинации между эффектом пористой конструкции эшафоте и механическими свойствами композита при различных скоростях деформации (9, 22, 23). Связанный с этим конкретным анализом конечного элемента, различие в 25% в упругости модуля измеренной в качестве эффекта скорости деформации и температуры, преобразует 4% разности жесткости жесткости в конструкции леса.
Связанный с этим конкретным анализом конечного элемента, различие в 25% в упругости модуля измеренной в качестве эффекта скорости деформации и температуры, преобразует 4% разности жесткости жесткости в конструкции леса.
 Инженерия костной ткани с использованием каркасов из поликапролактона Изготовлен методом селективного лазерного спекания.Biomaterials 2005;26:4817–27.Search in Google Scholar
Инженерия костной ткани с использованием каркасов из поликапролактона Изготовлен методом селективного лазерного спекания.Biomaterials 2005;26:4817–27.Search in Google Scholar Упругие свойства поликапролактона при малых деформациях существенно зависят от скорости деформации и температуры.Proc Inst Mecha Eng H J Eng Med. 2011;225:1015–20.Search in Google Scholar
Упругие свойства поликапролактона при малых деформациях существенно зависят от скорости деформации и температуры.Proc Inst Mecha Eng H J Eng Med. 2011;225:1015–20.Search in Google Scholar Полимер 2000;41:2183–2201.Поиск в Google Scholar
Полимер 2000;41:2183–2201.Поиск в Google Scholar