Л цистеин: L-Цистеин купить в Москве и регионах по низкой цене — VitaminOnline.ru
L-цистин
Общие сведения
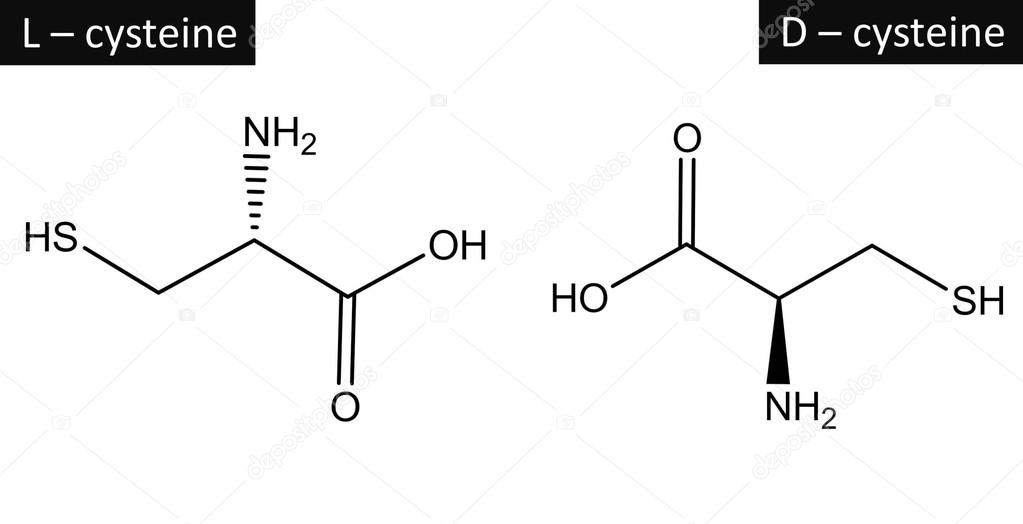
Цистин (3,3′-дитио-бис-2-аминопропионовая кислота, дицистеин). Каждая молекула цистина состоит из двух молекул цистеина.
L-Цистин — заменимая некодируемая аминокислота, не включается в пептидную цепь при ее биосинтезе, а образуется в результате ферментативного окисления остатков двух молекул цистеина (в т. ч. из разных полипептидных цепей).
Цистин – представляет собой бесцветные кристаллы, растворимые в воде. Образуется при окислении цистеина кислородом воздуха в щелочных растворах.
Аминокислоты метионин, цистеин и цистин метаболически тесно связаны друг с другом. Благодаря наличию в составе цистеина высокореактивной SH-группы в тканях легко осуществляется ферментативная окислительно-восстановительная реакция между цистеином и цистином. Цистеин образует с цистином окислительно-восстановительную пару, причем цистин играет роль восстановителя.
Основные источники
В форме кислоты входят в состав многих белков и природных пептидов. Особенно высоко содержание цистина в кератинах, которые в свою очередь явaляются производным белка ногтей, кожи и волос.
Пищевые источники цистина: рыба, овес, соя, рис, пшеница, яичный желток, лук и чеснок.
Функции в организме
-
Участвует в формировании пространственных структур ряда белков и пептидов, например инсулина, соматостатина и иммуноглобулинов.
-
Участвует в процессах формирования тканей кожи, способствует формированию коллагена и улучшает эластичность и текстуру кожи.
- Помогает обезвреживать некоторые токсические вещества и защищает организм от повреждающего действия радиации.
-
Является антиоксидантом, причем его антиоксидантное действие усиливается при одновременном приеме витамина С и селена.

-
Является предшественником глютатиона – вещества, оказывающего защитное действие на клетки печени и головного мозга от повреждения алкоголем, некоторых лекарственных препаратов и токсических веществ, содержащихся в сигаретном дыме.
Показания к применению
-
Необходимость улучшить состояние кожных покровов,
-
Ускорение регенерации волос и ногтевых пластинок,
-
Медленное заживление ран, царапин, ссадин.
В составе комплексной терапии
-
при анемиях различного происхождения,
-
болезнях дыхательной системы,
-
алкоголизме, курении,
-
белковом голодании и тяжелых инфекционных болезнях,
-
ревматоидном артрите,
-
атеросклерозе,
-
болезнях кожи, ломкости волос, алопециях.

Безопасность
Применение аминокислоты противопоказано при цистинурии. Во время беременности и в период грудного вскармливания вещество следует употреблять с осторожностью.Особенности приема и взаимодействия
Совместное применение цистина и витаминов В1 и С снижает эффективность инсулина. При сахарном диабете принимать только по назначению врача.
Финские ученые рассказали, как бороться с похмельем
Употребление продуктов с высоким содержанием аминокислоты L-цистеин может уменьшить симптомы похмелья, следует из исследования ученых Университета Хельсинки и Университета Восточной Финляндии.
L-цистеин входит в значительных количествах в состав таких продуктов, как сырое куриное яйцо, сырые семечки подсолнечника или свежие зерна гороха.
Эксперимент заключался в том, что одна группа волонтеров с признаками похмелья употребляла таблетки L-цистеина, другая — принимала плацебо. Доза алкоголя составила 1,5 грамма на один килограмм веса человека, который употреблялся в течение трех часов.
У испытуемых также измеряли содержание алкоголя в выдыхаемом воздухе и концентрацию метаболитов алкоголя в крови. В дополнение к этому участники эксперимента заполняли анкеты на следующее утро после употребления алкоголя, чтобы оценить тяжесть симптомов похмелья.
— Исследование обнаружило статистически значимую связь между L-цистеином и уменьшением симптомов похмелья. То есть L-цистеин уменьшал головную боль, тошноту, стресс и тревогу, — заверили ученые.
Это первое исследование в мире, в котором обнаружено, что простая аминокислота, такая как L-цистеин, уменьшает симптомы похмелья, сообщает «РИА Новости».
Ранее главный внештатный психиатр-нарколог Минздрава Евгений Брюн предупредил, что попытки избавиться от похмелья с помощью алкоголя смертельно опасны для человека.
— Это смертельно опасная штука, нельзя наслаивать новый алкоголь, пока не переработан старый. И нужно помнить, что алкоголь в организме человека перерабатывается от трех дней до трех недель, — сказал Евгений Брюн.
По его словам, привести организм в порядок после употребления большого количества спиртного помогут кефир, крепкие бульоны, а также капустный рассол.
Как сообщали «Кубанские новости», ученый из Брайтонского университета в Великобритании рассказал об алкогольных напитках, которые приводят к быстрому опьянению и вызывают наибольшее похмелье.
Исследователи из южнокорейского Национального университета Чеджу и Института медицинских наук назвали лучшими средствами от похмелья спаржу и газированный сок лайма и лимона.
При каком раке мне следует избегать приема N-ацетил-L-цистеина (NAC)?
Основные моменты
Пищевые добавки, такие как N-ацетил-L-цистеин (NAC), имеют много преимуществ для здоровья и широко используются онкологическими больными и людьми с генетическим риском рака.
Прием пищевых добавок N-ацетил-L-цистеина (NAC) может принести пользу онкологическим больным с карциномой эндометрия, получающим лечение анастрозолом. Но избегайте добавок N-ацетил-L-цистеина (NAC), если вы принимаете винбластин для лечения лимфомы Ходжкина. Точно так же прием пищевой добавки N-ацетил-L-цистеина (NAC) может принести пользу здоровым людям, которые подвержены генетическому риску рака из-за мутации гена MAX. Но избегайте приема пищевой добавки N-ацетил-L-цистеина (NAC), когда имеется генетический риск рака из-за мутации гена NBN.
Но избегайте приема пищевой добавки N-ацетил-L-цистеина (NAC), когда имеется генетический риск рака из-за мутации гена NBN.
Вывод — ваш индивидуальный контекст повлияет на ваше решение, безопасна ли пищевая добавка N-ацетил L-цистеин (NAC). А также то, что это решение необходимо постоянно пересматривать по мере изменения условий. Имеют значение такие состояния, как тип рака, текущее лечение и добавки, возраст, пол, вес, рост, образ жизни и любые выявленные генетические мутации. Таким образом, у вас есть законный вопрос, который вы можете задать для любой рекомендации относительно пищевых продуктов и натуральных добавок, — как они соотносятся с вашим индивидуальным контекстом.
Краткий обзор
Пищевые добавки — витамины, травы, минералы, пробиотики и другие специальные категории растут. Добавки — это высокие концентрации активных ингредиентов, которые также содержатся в различных продуктах питания. Разница в том, что продукты содержат более одного активного ингредиента при более низких концентрациях в диффузии. Помните, что каждый из этих ингредиентов имеет свой собственный научный и биологический механизм на молекулярном уровне — поэтому выбирайте правильную комбинацию добавок, таких как N-ацетил-L-цистеин (NAC), в зависимости от индивидуального контекста и условий.
Помните, что каждый из этих ингредиентов имеет свой собственный научный и биологический механизм на молекулярном уровне — поэтому выбирайте правильную комбинацию добавок, таких как N-ацетил-L-цистеин (NAC), в зависимости от индивидуального контекста и условий.
Итак, вопрос в том, следует ли вам принимать добавку N-ацетил-L-цистеина (NAC)? Стоит ли принимать его при генетическом риске рака из-за мутации гена NBN? Стоит ли принимать его при генетическом риске рака из-за мутации гена MAX? Стоит ли принимать его при диагностировании лимфомы Ходжкина? Следует ли вам принимать добавки N-ацетил-L-цистеина (NAC) при диагностировании рака эндометрия? Следует ли принимать его во время лечения винбластином? Следует ли вам продолжать принимать добавки N-ацетил-L-цистеина (NAC), если вы измените свое лечение с винбластина на анастрозол? Таким образом, общее объяснение типа «это естественно или повышает иммунитет» может быть неприемлемым и достаточным для выбора N-ацетил-L-цистеина (NAC).
рак
Рак остается нерешенной проблемой. Повышенная доступность индивидуализированного лечения и мониторинг рака с помощью крови и слюны стали важными факторами для улучшения результатов. Чем раньше будет вмешательство, тем лучше повлияет на результат. Генетическое тестирование может дать раннюю оценку риска и предрасположенности к раку. Но помимо регулярного наблюдения в большинстве случаев не существует терапевтических вариантов вмешательства. После постановки диагноза рака, такого как лимфома Ходжкина или карцинома эндометрия, лечение подбирается с учетом геномики опухоли и таких факторов, как стадия заболевания, возраст и пол. Во время ремиссии рака (после завершения цикла лечения) — мониторинг используется для оценки любого рецидива и, соответственно, принятия решения о дальнейших шагах. Подавляющее большинство онкологических больных и лиц из группы риска принимают пищевые добавки, такие как N-ацетил-L-цистеин (NAC).
Итак, вопрос в том, следует ли рассматривать все риски генетических мутаций и типы рака как единое целое при принятии решения об использовании N-ацетил-L-цистеина (NAC)? Являются ли последствия для биохимического пути генетического риска рака из-за мутации гена NBN такими же, как из-за мутации гена MAX? Являются ли последствия приема добавок N-ацетил-L-цистеина (NAC) при лимфоме Ходжкина такими же, как и при карциноме эндометрия? Это одно и то же, если вы лечитесь Винбластином или Анастрозолом?
N-ацетил L-цистеин (NAC) — пищевая добавка
N-ацетил-L-цистеин (NAC) представляет собой дополнительную форму природного цистеина аминокислоты и предшественника образования глутатиона (антиоксиданта) в организме. Ниже приведены некоторые из потенциальных преимуществ для здоровья N-ацетил-L-цистеина (NAC):
Ниже приведены некоторые из потенциальных преимуществ для здоровья N-ацетил-L-цистеина (NAC):
- Может быть полезным для уменьшения респираторных заболеваний, таких как ХОБЛ, астма, бронхит и муковисцидоз (Клаудио М. Сангинетти и др., Multidiscip Respir Med., 2016; Рабиндра Тируванциам и др., Proc Natl Acad Sci US A., 2006)
- Может помочь уменьшить повреждение почек (Вида Мохтари и др., Cell J., 2017)
- Может улучшить здоровье мозга (Майкл Коста и др., Chem Biol Interact., 2016)
- Может помочь улучшить здоровье печени (Кивиа Кейрос де Андраде и др., Int J Mol Sci., 2015; Вида Мохтари и др., Cell J., 2017)
- Может помочь уменьшить симптомы различных психических расстройств (Бриса С. Фернандес и др., J Clin Psychiatry., 2016; К. Пейдари и др., J Clin Pharm Ther., 2016)
Однако чрезмерное использование N-ацетил-L-цистеина (NAC) может привести к определенным побочным эффектам у некоторых людей, включая тошноту, рвоту, запор или диарею.
Молекулярные пути, которые регулируются N-ацетил-L-цистеином (NAC), включают репарацию ДНК, ангиогенез и передачу сигналов MYC. Эти клеточные пути прямо или косвенно регулируют определенные молекулярные конечные точки рака, такие как рост, распространение и смерть. Из-за этого биологического регулирования — для питания больных раком, правильный выбор добавок, таких как N-ацетил-L-цистеин (NAC) по отдельности или в комбинации, является важным решением. Принимая решение об использовании добавки N-ацетил-L-цистеина (NAC) для лечения рака, обязательно учитывайте все эти факторы и объяснения. Потому что, как и в случае лечения рака, использование N-ацетил-L-цистеина (NAC) не может быть универсальным решением для всех типов рака.
Эти клеточные пути прямо или косвенно регулируют определенные молекулярные конечные точки рака, такие как рост, распространение и смерть. Из-за этого биологического регулирования — для питания больных раком, правильный выбор добавок, таких как N-ацетил-L-цистеин (NAC) по отдельности или в комбинации, является важным решением. Принимая решение об использовании добавки N-ацетил-L-цистеина (NAC) для лечения рака, обязательно учитывайте все эти факторы и объяснения. Потому что, как и в случае лечения рака, использование N-ацетил-L-цистеина (NAC) не может быть универсальным решением для всех типов рака.
Выбор добавок N-ацетил-L-цистеина (NAC) для лечения рака
Причина, по которой нет простого способа ответить на вопрос «Когда мне следует избегать применения N-ацетил-L-цистеина (NAC) при раке», заключается в том, что «это зависит от обстоятельств!». Точно так же, как одно и то же лечение не работает для каждого больного раком, в зависимости от вашего индивидуального контекста N-ацетил L-цистеин (NAC) может быть вредным или безопасным. Наряду с тем, какой рак и связанная с ним генетика — текущее лечение, добавки, образ жизни, ИМТ и аллергия — все это факторы, определяющие, следует ли избегать N-ацетил-L-цистеина (NAC) и почему.
Наряду с тем, какой рак и связанная с ним генетика — текущее лечение, добавки, образ жизни, ИМТ и аллергия — все это факторы, определяющие, следует ли избегать N-ацетил-L-цистеина (NAC) и почему.
1. Будет ли добавка N-ацетил-L-цистеина (NAC) приносить пользу онкологическим больным с лимфомой Ходжкина, проходящим лечение винбластином?
Лимфома Ходжкина характеризуется и управляется специфическими генетическими мутациями, такими как TP53 и B2M, что приводит к изменениям специфических биохимических путей. Такое лечение рака, как винбластин, работает по определенному механизму действия. Цель состоит в том, чтобы обеспечить хорошее совпадение между лечением и путями, ведущими к раку, для эффективного индивидуального подхода. В таком состоянии следует избегать любых пищевых продуктов или пищевых добавок, которые имеют противоположный эффект по сравнению с лечением или уменьшают перекрытие. Например, N-ацетил-L-цистеин (NAC) следует избегать при лимфоме Ходжкина вместе с лечением винбластином. N-ацетил-L-цистеин (NAC) влияет на определенные пути, которые либо способствуют развитию факторов заболевания, либо сводят на нет лечебный эффект. Некоторые из факторов, которые следует учитывать при выборе питания, — это тип рака, методы лечения и добавки, которые принимаются в настоящее время (если таковые имеются), возраст, пол, ИМТ, образ жизни и любая информация о генетических мутациях (если таковая имеется).
N-ацетил-L-цистеин (NAC) влияет на определенные пути, которые либо способствуют развитию факторов заболевания, либо сводят на нет лечебный эффект. Некоторые из факторов, которые следует учитывать при выборе питания, — это тип рака, методы лечения и добавки, которые принимаются в настоящее время (если таковые имеются), возраст, пол, ИМТ, образ жизни и любая информация о генетических мутациях (если таковая имеется).
2. Будет ли добавка N-ацетил-L-цистеина (NAC) приносить пользу онкологическим пациентам с карциномой эндометрия, проходящим лечение анастрозолом?
Карцинома эндометрия характеризуется и управляется специфическими генетическими мутациями, такими как PTEN и PIK3CA, что приводит к изменениям специфических биохимических путей. Такое лечение рака, как Анастрозол, работает через определенные механизмы. Цель состоит в том, чтобы обеспечить хорошее совпадение методов лечения и развития рака для индивидуального подхода. В таком состоянии следует рассматривать любую пищу или пищевую добавку, которые имеют эффект, совместимый с лечением или уменьшающие перекрытие. Например, добавки N-ацетил-L-цистеина (NAC) следует рассматривать при карциноме эндометрия наряду с лечением Анастрозолом. Добавки N-ацетил-L-цистеина (NAC) воздействуют на определенные пути, которые либо препятствуют движущим силам карциномы эндометрия, либо улучшают эффект лечения анастрозолом.
Например, добавки N-ацетил-L-цистеина (NAC) следует рассматривать при карциноме эндометрия наряду с лечением Анастрозолом. Добавки N-ацетил-L-цистеина (NAC) воздействуют на определенные пути, которые либо препятствуют движущим силам карциномы эндометрия, либо улучшают эффект лечения анастрозолом.
Продукты, которые нужно есть после диагноза рака!
Нет двух одинаковых видов рака. Выходите за рамки общих рекомендаций по питанию для всех и с уверенностью принимайте индивидуальные решения о еде и добавках.
3. Безопасны ли добавки N-ацетил-L-цистеина (NAC) для здоровых людей с генетическим риском, связанным с мутациями NBN?
Различные компании предлагают панели генов для тестирования для оценки генетического риска различных видов рака. Эти панели охватывают гены, связанные с раком груди, яичников, матки, простаты, желудочно-кишечного тракта и другие. Генетическое тестирование этих генов может подтвердить диагноз и помочь в принятии решений о лечении и лечении. Выявление варианта, вызывающего заболевание, также может служить ориентиром при тестировании и диагностике родственников из группы риска.
Выявление варианта, вызывающего заболевание, также может служить ориентиром при тестировании и диагностике родственников из группы риска.
NBN — один из генов, обычно доступных в панелях для тестирования риска рака. Мутация NBN вызывает нарушение биохимических путей / процессов, таких как восстановление ДНК, передача сигналов стволовыми клетками, контрольные точки клеточного цикла, передача сигналов эстрогена и ангиогенез. Эти пути являются прямыми или косвенными движущими силами молекулярных конечных точек рака. N-ацетил-L-цистеин (NAC) следует избегать, когда генетическая панель выявляет мутацию NBN для рака молочной железы. N-ацетил-L-цистеин (NAC) влияет на пути / процессы, такие как восстановление ДНК и передача сигналов стволовыми клетками, и оказывает неблагоприятное воздействие на NBN и связанные с ним состояния.
4. Безопасны ли добавки N-ацетил-L-цистеина (NAC) для здоровых людей с максимальным генетическим риском, связанным с мутациями?
MAX — один из генов, доступных в панелях для тестирования риска рака. Мутация MAX вызывает нарушение биохимических путей / процессов, таких как ангиогенез, передача сигналов MYC, передача сигналов стволовыми клетками, эпигенетика рака и клеточный цикл. Эти пути являются прямыми или косвенными движущими силами молекулярных конечных точек рака. Рассмотрите возможность приема добавок N-ацетил-L-цистеина (NAC), когда генетическая панель выявляет мутацию в MAX для нейроэндокринного рака. N-ацетил-L-цистеин (NAC) влияет на пути / процессы, такие как ангиогенез и передача сигналов MYC, и оказывает поддерживающий эффект у людей с мутацией MAX и связанными с ними состояниями.
Мутация MAX вызывает нарушение биохимических путей / процессов, таких как ангиогенез, передача сигналов MYC, передача сигналов стволовыми клетками, эпигенетика рака и клеточный цикл. Эти пути являются прямыми или косвенными движущими силами молекулярных конечных точек рака. Рассмотрите возможность приема добавок N-ацетил-L-цистеина (NAC), когда генетическая панель выявляет мутацию в MAX для нейроэндокринного рака. N-ацетил-L-цистеин (NAC) влияет на пути / процессы, такие как ангиогенез и передача сигналов MYC, и оказывает поддерживающий эффект у людей с мутацией MAX и связанными с ними состояниями.
* Также включены другие факторы, такие как ИМТ, виды лечения, Привычки образа жизни
В заключение
Две самые важные вещи, о которых следует помнить, — это то, что лечение рака и питание никогда не одинаковы для всех. Питание, которое включает в себя пищевые продукты и пищевые добавки, такие как N-ацетил-L-цистеин (NAC), является эффективным средством, которым вы можете управлять, даже если вы столкнулись с раком.
Продукты, которые нужно есть после диагноза рака!
Нет двух одинаковых видов рака. Выходите за рамки общих рекомендаций по питанию для всех и с уверенностью принимайте индивидуальные решения о еде и добавках.
Больным раком часто приходится иметь дело с разными побочные эффекты химиотерапии которые влияют на качество их жизни и ищут альтернативные методы лечения рака. Принимая правильное питание и добавки, основанные на научных соображениях (избегая догадок и случайного выбора) — лучшее естественное средство от рака и побочных эффектов, связанных с лечением.
L-цистеин – для волос, кожи, ногтей, иммунитета, детокса и не только
Принимаю L- цистеин (вместе с глицином, лизином и пролином) уже несколько месяцев по 1 капсуле в день. Что замечено – волосы и ногти стали расти лучше и более здоровыми, волосы гораздо лучше переносят окрашивание. Кожа тоже радует – замедлила своё увядание, как-то подтянулась.
Twinlab, L-цистеин, 60 капсул
Этот L-цистеин хорош тем, что он находится в максимально усваиваемой свободной форме.
L-цистеин – это серосодержащая аминокислота, которая входит в состав белков и пептидов.
Свойства цистеина:
— входит в состав кератина, основного белка кожи, ногтей и особенно волос, улучшает их состояние;
— способствует формированию коллагена, от которого зависит эластичность и упругость кожи;
— является мощным антиоксидантом, борющимся со свободными радикалами, вызывающими онкологические и сердечно-сосудистые заболевания; его действие усиливается в присутствии селена и витамина С;
— из него и глицина образуется глутатион — вещество, улучшающее иммунитет, защищающее клетки печени и головного мозга от повреждения токсическими веществами, алкоголем, некоторыми лекарственными препаратами, сигаретным дымом;
— важен для производства таурина — вещества, необходимого для работы нервной системы, хорошей памяти, нормализации артериального давления, здоровья глаз, улучшения метаболизма;
— входит в состав некоторых пищеварительных ферментов, чем способствует улучшению пищеварения;
— защищает организм от радиоактивного излучения;
— восстанавливает слизистый слой желудочно-кишечного тракта;
— входит в состав инсулина;
— особенно необходим при сердечно-сосудистых заболеваниях, раке, ревматоидном артрите, катаракте, заболеваниях органов дыхания, сильном стрессе и повышенной физической активности, ослабленном иммунитете и ВИЧ/СПИД, после операций, ожогов, отравлений;
— ускоряет метаболизм жиров и образование мышечной ткани.
Противопоказания:
— цистинурия;
— сахарный диабет.
С осторожностью:
— гипертензия;
— проблемы с вилочковой железой;
— беременным и кормящим матерям.
(При клике левой кнопкой мыши фото открываются в новой вкладке и увеличиваются)
Другие мои отзывы о БАДах:
Ацетил-L-Карнитин — для улучшения работы мозга, повышения выносливости и похудения со скидкой 10%
Мега-полезное маточное молочко — укрепляем иммунитет, боремся со стрессом, лечим бесплодие
Country Life, Gluten Free, Хелатный магний — здоровое сердце, сосуды, сон, волосы, ногти
Now Foods, GABA — улучшение работы мозга, натуральный успокаивающий эффект и борьба с депрессией
21st Century, Ферменты папайи со скидкой 10% — улучшение пищеварения, иммунитета и не только
California Gold Nutrition, Пробиотики — для иммунитета, против аллергии и воспалений
California Gold Nutrition, Коэнзим Q10 со скидкой 2$ — для здорового сердца, иммунитета, молодости — сейчас на 2 $ дешевле вместе с другими добавками
Экономичная упаковка гиалуроновой кислоты с хондроитином для суставов и увлажнения кожи — сейчас со скидкой 10%
Здоровые глаза, сердце, иммунитет — и всё это благодаря лютеину
Очень важные для здоровья витамины D3 и K2
Мятные жевательные таблетки Umcka — убить начинающуюся простуду без вреда для печени
Now Foods, Хлорофилл в капсулах. Огромная польза и решение одной деликатной проблемы
Огромная польза и решение одной деликатной проблемы
21st Century, Мелатонин — полезное снотворное
Natrol, Ресвератрол + кверцетин — два антиоксиданта в одной таблетке
Natrol, Питательная ягода асаи на страже здоровья и молодости
Source Naturals, Антиоксидант астаксантин
American Health, Витамин С в максимально усваиваемой форме Эстер-C
Paradise Herbs, Экстракт Годжи — поддержка организма в холодный период
Ещё больше отзывов – в моём журнале.
Мои отзывы в сообществе можно увидеть, наведя курсор на мою аватарку и нажав: «Показать записи автора в сообществе».
Благодарю всех, кто воспользовался моим кодом KBJ369!
Ацетилцистеин — описание ингредиента, инструкция по применению, показания и противопоказания
Описание ацетилцистеина
Ацетилцистеин – это форма цистеина, используемая в пищевых добавках и препаратах и оказывающая муколитическое, антиоксидантное и отхаркивающее воздействие.![]() Цистеин – полунезаменимая аминокислота. Полунезаменимая, поскольку синтезируется в организме человека из метионина и серина, однако при их недостатке в рационе, может поступать в него исключительно с пищей и добавками. Источники цистеина – индейка, яйца, сыр, бобовые, семена подсолнечника, куриное мясо.
Цистеин – полунезаменимая аминокислота. Полунезаменимая, поскольку синтезируется в организме человека из метионина и серина, однако при их недостатке в рационе, может поступать в него исключительно с пищей и добавками. Источники цистеина – индейка, яйца, сыр, бобовые, семена подсолнечника, куриное мясо.
Внимание! N-ацетил-L-цистеин (NAC) включен в список важнейших лекарственных препаратов. Он эффективно предотвращает бактериальную адгезию и растворяет матрицу зрелой биопленки. Показан при заболеваниях инфекционной природы, сопровождающихся формированием трудноотделяемой мокроты.
Фармакологические свойства
Ацетилцистеин обеспечивает восполнение в организме глутатиона – мощного антиоксиданта, который важен для здоровья иммунной системы и профилактики многих хронических заболеваний и способен существенно продлить молодость и жизнь. Это вещество защищает клетки от разрушающего воздействия свободных радикалов – молекул с одним непарным электроном, стремящихся восстановить равновесие и отобрать недостающий электрон у других соединений. Глутатион «приманивает» свободные радикалы и в процессе атаки отдает им свой электрон, с легкостью восстанавливая утрату и спасая клетки от гибели.
Глутатион «приманивает» свободные радикалы и в процессе атаки отдает им свой электрон, с легкостью восстанавливая утрату и спасая клетки от гибели.
NAC очищает организм от токсинов и ядов, в том числе при передозировке парацетамола. Благодаря антиоксидантным и противовоспалительным свойствам его используют в терапии болезней печени. Полезен ацетилцистеин и для мозга. Он способен облегчить протекание многих психических расстройств и снизить тягу к никотину и алкоголю.
Внимание! Отхаркивающий эффект NAC обусловил его применение при воспалительных процессах в дыхательных путях. Он разжижает слизь и стимулирует отхождение мокроты.
Средство может задействоваться в терапии болезней Паркинсона и Альцгеймера. Благодаря снижению окислительного стресса ацетилцистеин улучшает фертильность у мужчин и женщин.
Подавляя воспалительные процессы в жировых тканях, NAC понижает резистентность к инсулину и помогает организму контролировать уровень глюкозы в крови. N-ацетил-L-цистеин способен понизить риск сердечных заболевания и иммунных нарушений.
N-ацетил-L-цистеин способен понизить риск сердечных заболевания и иммунных нарушений.
Применение ацетилцистеина
Для производства цистеина организму нужно получать достаточное количество цианокобаламина, пиридоксина и фолата. Эти питательные вещества присутствуют в таких продуктах питания, как бобовые, сыры, куриное мясо, яйца, индейка, семена подсолнечника.
В виде добавок ацетилцистеин усваивается не полностью. Поэтому его принимают в дозировках, превышающих суточную потребность – 600–1800 мг.
Противопоказания и побочные эффекты
Ацетилцистеин может спровоцировать побочные эффекты. Самые распространенные – тошнота, рвота, изжога, сонливость, апатия, раздражение слизистой оболочки дыхательных путей, зуд, аллергический кашель.
NAC противопоказан при индивидуальной непереносимости препарата, беременности, грудном вскармливании, язвенной болезни в период обострения. Применяя средство при опухолевых болезнях надпочечников, почечных и печеночных патологиях, гипертензии, варикозном расширении вен пищевода следует соблюдать осторожность и внимательно следить за своим самочувствием.
Применяя средство при опухолевых болезнях надпочечников, почечных и печеночных патологиях, гипертензии, варикозном расширении вен пищевода следует соблюдать осторожность и внимательно следить за своим самочувствием.
ЦИСТЕИН — это… Что такое ЦИСТЕИН?
Цистеин — Цистеин … Википедия
ЦИСТЕИН — (HSCh3Ch3COOH), кристаллическая аминокислота, содержащаяся в животных белках, особенно в составе волос, копыт и кератина в коже. Благодаря наличию групп HS это вещество служит катализатором для некоторых энзимов … Научно-технический энциклопедический словарь
ЦИСТЕИН — L ? амино ? тиопропионовая к та, заменимая серусо держащая аминокислота. Входит в состав почти всех природных белков и глутатио на. Занимает центр, место в обмене серусодержащих соединений. Выполняет защитную функцию, связывая токсичные ионы… … Биологический энциклопедический словарь
цистеин — сущ. , кол во синонимов: 2 • аминокислота (36) • антиоксидант (26) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
, кол во синонимов: 2 • аминокислота (36) • антиоксидант (26) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
цистеин — Серосодержащая аминокислота [http://www.dunwoodypress.com/148/PDF/Biotech Eng Rus.pdf] Тематики биотехнологии EN cysteine … Справочник технического переводчика
цистеин — h3NCH(Ch3SH)COOH, алифатическая аминокислота. Входит в состав белков, глутатиона. Сульфгидрильные ( SH) группы цистеина важны для проявления биологической активности многих ферментов, белковых гормонов, токсинов. В организме легко превращается в… … Энциклопедический словарь
цистеин — cisteinas statusas T sritis chemija formulė HSCH₂CH(NH₂)COOH santrumpa( os) Cys, C atitikmenys: angl. cysteine rus. цистеин ryšiai: sinonimas – 2 amino 3 merkaptopropano rūgštis … Chemijos terminų aiškinamasis žodynas
цистеин — заменимая в питании человека моноаминомонокарбоновая, содержащая сульфгидрильные группы аминокислота, входящая в состав всех белков и глутатиона; в организме недоношенных детей биосинтез Ц. недостаточен … Большой медицинский словарь
недостаточен … Большой медицинский словарь
Цистеин — α амино β тиопропионовая кислота, HSCh3CH (Nh3) COOH; серусодержащая аминокислота. Существует в виде двух оптически активных L и D форм и рацемической DL формы. L Ц. входит в состав почти всех природных белков и Глутатиона. При гидролизе… … Большая советская энциклопедия
ЦИСТЕИН — (2 амино З меркаптопропионовая к та, меркаптоаланин, Cys, С) HSCh3CH(Nh3)COOH, мол. м. 121,16. L Ц. бесцв. кристаллы, т. пл. гидрохлорида 178 … Химическая энциклопедия
Now Foods L-Cysteine. L-Цистеин с витаминами В6 и С
Now Foods. L-Cysteine
L-Цистеин 500 мг + витамин В6 + витамин С, 100 таблеток.
Цистеин – заменимая серосодержащая аминокислота, важна для поддержки здоровья кожи, волос и ногтей, дает детоксикацию и защиту клеток печени и головного мозга. Он может синтезироваться в организме млекопитающих из серина с участием метионина как источника серы, а также АТФ и витамина В6.

L-цистеин для кожи:
- является важным компонентом волос, ногтей и кожи, входит в состав белков и пептидов, играет важную роль в процессах формирования тканей кожи;
- улучшает эластичность и текстуру, предохраняет от старения;
- обеспечивает структурную поддержку тканей организма;
- обладает ранозаживляющим действием;
- стабилизирует структуру белка и способствует образованию коллагена;
- необходим после операций, ожогов, отравлений.
L-цистеин – это один из самых мощных антиоксидантов, при этом его антиоксидантное действие усиливается при одновременном приеме витамина С и селена.
Важность L-цистеина для организма:
- с помощью цистеина и глицина образуется глутатион – вещество, улучшающее иммунитет, защищающее клетки печени и головного мозга от повреждения токсическими веществами, рентгеновскими лучами, радиацией, некоторыми лекарственными препаратами;
- важен для производства таурина — вещества, необходимого для работы нервной системы, хорошей памяти, нормализации артериального давления, здоровья глаз, улучшения метаболизма;
- входит в состав пищеварительных ферментов, чем способствует улучшению пищеварения;
- восстанавливает слизистый слой желудочно-кишечного тракта;
- входит в состав инсулина;
- оказывает отхаркивающее и муколитическое действие, обладает способностью разрушать слизь в дыхательных путях;
- играет важную роль в активизации лейкоцитов и лимфоцитов;
- ускоряет процессы выздоровления при заболеваниях органов дыхания.

Витамин В6 (пиридоксин) играет важную роль в обмене веществ, необходим для нормального функционирования центральной и периферической нервной системы, участвует в синтезе нейромедиаторов. Активно участвует в метаболизме аминокислот, обмене гистамина. Играет важную роль в транспортировке аминокислот через клеточную мембрану. Улучшает утилизацию ненасыщенных жирных кислот, нормализует липидный обмен при атеросклерозе (снижает уровень холестерина и липидов), улучшает сократимость миокарда, способствует превращению фолиевой кислоты в ее активную форму.
В6 (пиридоксин) незаменим для ухода за зрелой кожей, поскольку оберегает ее от дерматита, способствует ее увлажнению, устраняет отечность. Витамин В6 в целом замедляет старение организма, ну а в частности, предотвращает сухость кожи, появление перхоти. Недостаток В6 проявляется шелушением и дерматитом над бровями, в носогубных складках, трещинами в уголках губ.
Соответствует стандарту качества GMP
| Distilpure Msm | Цистеин (0,02 г / 100 г) + биотин (0,02 г / 100 г) + цистин (0,05 г / 100 г) + метионин (0,02 г / 100 г) + Хлорид тиамина (0,02 г / 100 г) | Порошок | Актуальный | Mbg Inc (Корейский институт развития науки) | 16 сентября 2017 г. | 16 сентября 2018 г. | США | |
| FREAMINE III% 10 1000 мл (SETLI) | Цистеин (0.016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | Раствор | Внутривенно | ECZACIBAŞI-BAXRİ SAN.VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FREAMINE III% 10 1000 ML (SETSIZ) | Цистеин (0.016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | Раствор | Внутривенно | ECZACIBAŞI-BAXRİ SAN.VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FREAMINE III% 10 500 мл (SETLI) | Цистеин (0. 016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) 016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | Раствор | Внутривенно | ECZACIBAŞI-BAXRİ SAN.VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FREAMINE III% 10 500 мл (SETSIZ) | Цистеин (0.016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | Раствор | Внутривенно | ECZACIBAŞI-BAXRİ SAN.VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FREAMINE III% 8.5500 мл (SETLI) | Цистеин (0,014%) + аланин (0,6%) + аргинин (0,81%) + глицин (1,19%) + гистидин (0,24%) + изолейцин (0,59%) + лейцин (0,77%) + Лизин (0,62%) + метионин (0,45%) + фенилаланин (0,48%) + пролин (0,95%) + серин (0,5%) + треонин (0,34%) + триптофан (0,13%) + валин (0,56%) | Раствор | Внутривенно | ECZACIBAŞI-BAXTER HASTANE ÜRÜNLERİ SAN. VE TİC. В КАЧЕСТВЕ. VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FREAMINE III% 8.5500 мл (SETSIZ) | Цистеин (0,014%) + аланин (0,6%) + аргинин (0,81%) + глицин (1,19%) + гистидин (0,24%) + изолейцин (0,59%) + лейцин (0,77%) + Лизин (0,62%) + метионин (0,45%) + фенилаланин (0,48%) + пролин (0,95%) + серин (0,5%) + треонин (0,34%) + триптофан (0,13%) + валин (0,56%) | Раствор | Внутривенно | ECZACIBAŞI-BAXTER HASTANE ÜRÜNLERİ SAN.VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FRESELAMIN% 10 1000 ML SETLI SISE | Цистеин (0.016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | раствор | для внутривенного введения | OSEL İLAÇ SAN. VE TİC. В КАЧЕСТВЕ. VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Неприменимо | Турция | |
| FRESELAMIN% 10 1000 ML РАЗМЕР | Цистеин (0.016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | раствор | для внутривенного введения | OSEL İLAÇ SAN. VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция | |
| FRESELAMIN% 10 500 мл SETLI SISE | Цистеин (0.016%) + аланин (0,71%) + аргинин (0,95%) + глицин (1,4%) + гистидин (0,28%) + изолейцин (0,69%) + лейцин (0,91%) + лизин (0,73%) + метионин (0,53%). ) + Фенилаланин (0,56%) + пролин (1,12%) + серин (0,59%) + треонин (0,4%) + триптофан (0,15%) + валин (0,66%) | раствор | для внутривенного введения | OSEL İLAÇ SAN. VE TİC. В КАЧЕСТВЕ. VE TİC. В КАЧЕСТВЕ. | 2020-08-14 | Не применимо | Турция |
Блог The Vegetarian Resource Group
Жанна Якубу, MS
Директор по исследованиям VRG
VRG недавно провела опрос производителей и поставщиков пищевых ингредиентов, а также производителей хлеба и рогаликов, чтобы выяснить, сохранились ли все еще животные источники обычного аминокислотного кондиционера для теста и ароматизатора реакции корма для человека и домашних животных, используемого для изготовления усилителей вкуса, L-цистеина. доминируют на рынке, как и в 2007 году, когда мы последний раз сообщали о L-цистеине.Ответом было твердое «да».
Один из ведущих поставщиков аминокислот сообщил нам в феврале 2011 года, что источником являются «утиные перья или человеческий волос», на основании официального заявления, полученного от его китайского поставщика.
Менеджер по продукту другой компании, производящей пищевые ингредиенты, сообщил VRG в августе 2010 года, что «сегодня основным источником L-цистеина являются не человеческие волосы и не утиные перья, а свиньи волосы». По его оценкам, свиной волос является источником 90% китайского L-цистеина.
По его оценкам, свиной волос является источником 90% китайского L-цистеина.
Менеджер компании, производящей L-цистеин неживотного происхождения, заявил в сентябре 2010 года, что основным животным источником L-цистеина сегодня были «в основном человеческие волосы», за которыми следовали «утиные перья или волосы свиньи, когда количество человеческих волос было низким». Согласно этому источнику, перья и свиная шерсть «неэффективны по сравнению с [человеческими] волосами [в получении большого количества L-цистеина]. Так что, если есть проблема с волосами [снабжением], то свиные волосы или перья могут быть резервное копирование.»
В сентябре 2010 года VRG спросила компании, производящие неживотные версии L-цистеина, как их продукт продается на рынке.По оценкам ведущих компаний, сегодня на долю растительного ферментационного или синтетического продукта приходится примерно 10% рынка L-цистеина. Причиной низкой доли рынка является высокая цена на L-цистеин неживотного происхождения (в два-три раза больше) по сравнению с гораздо более дешевым и более многочисленным китайским (и индийским, в меньшей, но растущей степени) предложением. .
.
Вторая причина заключается в том, что все большее число пищевых компаний требует «натуральный» продукт, а «синтетический» L-цистеин не соответствует этому критерию.Кроме того, в сентябре 2010 года крупный продавец L-цистеина сообщил нам, что политика компании заключается в том, чтобы маркировать все, что использует L-цистеин животного происхождения (например, волосы или перья), как «невегетарианские», хотя технически это все еще остается. вегетарианский »и считается« натуральным ». Их решение о маркировке было предосторожным в ответ на тех, кто предпочитает избегать всех ингредиентов животного происхождения. (Примечание: одна компания продает L-цистеин, полученный путем микробной ферментации, а другая находится в процессе разработки собственной техники ферментации.По оценкам последней компании, на то, чтобы усовершенствовать процесс в промышленных масштабах и затем вывести его на рынок, может потребоваться два-три года.)
Писатель заметил в ходе опроса многих компаний в феврале и марте 2011 года, по сравнению с 2007 годом, когда VRG последний раз обновляла L-цистеин (http://www. vrg.org/vrgnews/2007jul.htm#s2), что их число растет. компаний запрашивают или перепродают только L-цистеин неживотного происхождения для использования в пищевых продуктах.
vrg.org/vrgnews/2007jul.htm#s2), что их число растет. компаний запрашивают или перепродают только L-цистеин неживотного происхождения для использования в пищевых продуктах.
Обеспокоенным лицам, которые хотели бы, чтобы в их хлебных продуктах, а также в других продуктах питания для людей и домашних животных использовалось больше L-цистеина неживотного происхождения, предлагается вежливо высказать свое мнение компаниям, производящим продукты питания, и сетям ресторанов, которые используют животных. -содержащий L-цистеин.Точно так же пищевые компании и сети, которые используют L-цистеин неживотного происхождения, должны поблагодарить вас.
Чтобы приобрести наше руководство по пищевым ингредиентам , перейдите по адресу:
http://www.vrg.org/catalog/index.php?main_page=product_info&cPath=1&products_id=8
Чтобы поддержать исследования VRG, сделайте пожертвование по адресу:
https://www.givedirect.org/give/givefrm.asp?CID=1565
или
http://www. vrg.org/catalog/index.php?main_page = индекс & cPath = 4
vrg.org/catalog/index.php?main_page = индекс & cPath = 4
Frontiers | Нейропротекторная роль l-цистеина в ослаблении раннего повреждения мозга и повышении плотности синапсов через путь CBS / h3S после субарахноидального кровоизлияния у крыс
Введение
У пациентов с субарахноидальным кровоизлиянием (САК) ранняя черепно-мозговая травма (EBI) является основной причиной высокой смертности и заболеваемости (1).Множественные факторы, включая гибель клеток, окислительный стресс, аномальные воспалительные реакции и церебральный вазоспазм, вовлечены в механизмы, лежащие в основе EBI после SAH (2). Таким образом, срочно необходимо определение ранних нейропротективных стратегий для потенциального клинического использования.
l-цистеин — это полузаменимая аминокислота, которая важна для регуляции метаболизма человека (3). Три традиционных эндогенных источника l-цистеина включают абсорбцию из рациона, путь транссульфурации и расщепление белка.Нарушение внеклеточного соотношения l-цистеин / l-цистин может быть связано с окислительным стрессом (4, 5). Kimura et al. продемонстрировали, что в центральной нервной системе (ЦНС) l-цистеин может катализироваться цистатионин-β-синтазой (CBS), которая экспрессируется в астроцитах, а затем может продуцировать эндогенный сероводород (H 2 S) (6, 7). Более того, аминооксиуксусная кислота (AOAA), широко используемый селективный ингибитор CBS, как сообщается, блокирует CBS-опосредованную продукцию H 2 S в нескольких органах (7, 8).
Kimura et al. продемонстрировали, что в центральной нервной системе (ЦНС) l-цистеин может катализироваться цистатионин-β-синтазой (CBS), которая экспрессируется в астроцитах, а затем может продуцировать эндогенный сероводород (H 2 S) (6, 7). Более того, аминооксиуксусная кислота (AOAA), широко используемый селективный ингибитор CBS, как сообщается, блокирует CBS-опосредованную продукцию H 2 S в нескольких органах (7, 8).
H 2 S играет несколько ролей в ЦНС как в физиологических, так и в патологических условиях (9). Интересно, что накопленные данные свидетельствуют о том, что экзогенный H 2 S может действовать как мощный нейрозащитный агент. Кимура и Кимура сообщили в 2004 году, что H 2 S защищает первичные нейроны коры головного мозга крысы от повреждений, вызванных окислительным стрессом (10). H 2 S также оказывает ряд цитопротекторных антиапоптотических, антиоксидантных и противовоспалительных эффектов на ЦНС (6, 11, 12). Наши предыдущие исследования показали, что H 2 S проявляет нейропротекторный потенциал на животной модели повреждения церебральной гипоксией (13, 14). Важно отметить, что мы наблюдали, что l-цистеин способствует пролиферации и дифференцировке нейронов нервных стволовых клеток посредством системы CBS / H 2 S in vitro (15). Введение АОАА на животных моделях церебральной гипоксии может ингибировать образование H 2 S и вызывать физиологические изменения в регуляции артериального давления или ассоциативном обучении (7, 16).
Наши предыдущие исследования показали, что H 2 S проявляет нейропротекторный потенциал на животной модели повреждения церебральной гипоксией (13, 14). Важно отметить, что мы наблюдали, что l-цистеин способствует пролиферации и дифференцировке нейронов нервных стволовых клеток посредством системы CBS / H 2 S in vitro (15). Введение АОАА на животных моделях церебральной гипоксии может ингибировать образование H 2 S и вызывать физиологические изменения в регуляции артериального давления или ассоциативном обучении (7, 16).
Доступна лишь ограниченная информация о нейропротекторном действии H 2 S на SAH (17, 18). Кроме того, может ли L-цистеин безопасно оказывать защитное действие на EBI после SAH, запуская CBS для производства H 2 S, и молекулярные механизмы, лежащие в основе этих эффектов, все еще неизвестны. Таким образом, цель этого исследования — выяснить потенциальный терапевтический эффект l-цистеина на EBI после САК и определить, связан ли l-цистеин с функцией H 2 S.
Животные и методы
Животные
крыс-самцов линии Wistar (280–350 г) были приобретены в Центре лабораторных животных Университета Шаньдун. По прибытии животных поместили в стандартные лабораторные условия (температура 20 ± 2 ° C, 12 часов: 12-часовой цикл свет / темнота, свет включили в 08:00), обеспечили свободный доступ к пище и воде и дали им возможность привыкнуть к новым условиям. среда на 1 неделю.
SAH Модель
Экспериментальная САК была индуцирована у крыс с помощью двойной инъекции крови в соответствии с нашим предыдущим исследованием (18).Вкратце, эстезия вызывалась под действием 3,5% изофлурана и заменялась непрерывным наркозом изофлураном 2,5% во время операции. Катетер вводили в бедренную артерию в стерильных условиях для забора крови и измерения кровяного давления. Двести микролитров аутологичной крови были взяты из бедренной артерии и введены в большую цистерну в течение 3-минутного периода.
Экспериментальный план
Всего проведено 134 операции. Крыс случайным образом разделили на следующие пять групп: Sham ( n = 22), Sham + l-цистеин ( n = 22), SAH ( n = 30), SAH + l-цистеин ( n = 30) и SAH + 1-цистеин + AOAA ( n = 30).Через 48 ч после САК этих крыс умерщвляли, ткани префронтальной коры (ПФК) удаляли и готовили для анализа. Смертность в индивидуальной группе в течение 48 часов после операции была следующей: имитация 0% (0/22), симуляция + l-цистеин 0% (0/22), SAH 23,3% (7/30), SAH + l-цистеин 10. % (3/30) и SAH + 1-цистеин + AOAA 16,7% (5/30).
Крыс случайным образом разделили на следующие пять групп: Sham ( n = 22), Sham + l-цистеин ( n = 22), SAH ( n = 30), SAH + l-цистеин ( n = 30) и SAH + 1-цистеин + AOAA ( n = 30).Через 48 ч после САК этих крыс умерщвляли, ткани префронтальной коры (ПФК) удаляли и готовили для анализа. Смертность в индивидуальной группе в течение 48 часов после операции была следующей: имитация 0% (0/22), симуляция + l-цистеин 0% (0/22), SAH 23,3% (7/30), SAH + l-цистеин 10. % (3/30) и SAH + 1-цистеин + AOAA 16,7% (5/30).
Управление по лекарствам
l-цистеин (Sigma-Aldrich) растворяли в носителе (PBS) в рабочей концентрации 100 мМ, как определено нашим предыдущим исследованием (15), и 30 мкл раствора l-цистеина вводили интрацеребровентрикулярно через 30 мин после САК.AOAA (Sigma-Aldrich) растворяли в носителе (PBS) и внутрибрюшинно вводили дозу 5 мг / кг с l-цистеином.
Анализ активности CBS и измерение H
2 Производство S CBS-активность ткани мозга определяли с помощью набора для анализа CBS (Genmed Scientifics Inc.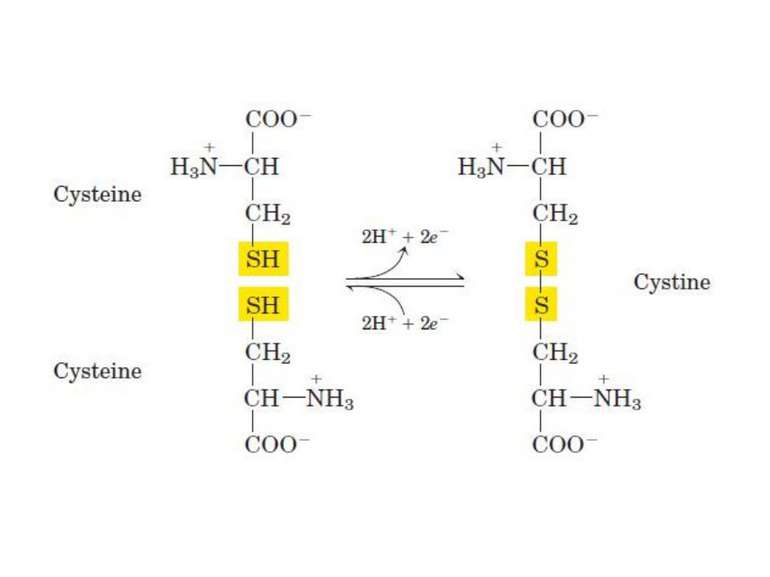 , Китай). Этот анализ косвенно измеряет активность CBS путем обнаружения метаболитов CBS, которые взаимодействуют с NADPH. Поглощение измеряли при 340 нм с использованием считывающего устройства для микропланшетов (Spectra Max 190, Molecular Devices, Саннивейл, Калифорния, США).
, Китай). Этот анализ косвенно измеряет активность CBS путем обнаружения метаболитов CBS, которые взаимодействуют с NADPH. Поглощение измеряли при 340 нм с использованием считывающего устройства для микропланшетов (Spectra Max 190, Molecular Devices, Саннивейл, Калифорния, США).
Для количественного определения H 2 S мы использовали традиционный метод метиленового синего. Вкратце, ткань PFC гомогенизировали и инкубировали с ацетатом цинка, который генерирует сульфид цинка, который впоследствии вступает в реакцию с N , N -диметил- p -фенилендиаминсульфатом (NNDPD). Величину поглощения определяли при 670 нм, и уровень H 2 S рассчитывали по калибровочной кривой NaHS.
Неврологические баллы
Через 48 часов после САК неврологическая функция оценивалась двумя «слепыми» исследователями с использованием модифицированной системы баллов Гарсиа (19, 20).Эта система включает следующие семь субтестов: спонтанная активность (0–3 балла), реакция на поглаживание (1–3 балла) и прикосновение вибрисс (1–3 балла), симметрия конечностей (0–3 балла), вытягивание передних конечностей ( 0–3 балла), скалолазание (0–3 балла) и ходьба на луче (0–4 балла). Общий балл этих субтестов отражал неврологическую функцию. Высокие баллы по Гарсиа указали на лучшую неврологическую функцию, а низкие баллы — на худшую функцию, при этом худшие показатели получили 2 балла (21).
Общий балл этих субтестов отражал неврологическую функцию. Высокие баллы по Гарсиа указали на лучшую неврологическую функцию, а низкие баллы — на худшую функцию, при этом худшие показатели получили 2 балла (21).
Содержание воды в мозге
Отек мозга определяли согласно методу «влажный / сухой», где% содержания воды в мозге = [(влажный вес — сухой вес) / влажный вес] × 100%. Вкратце, каждый образец мозга (оба полушария головного мозга) извлекали из черепа и немедленно взвешивали. Затем образец сушили при 100 ° C в течение 48 ч и взвешивали для определения сухой массы.
Окрашивание гематоксилином и эозином
Животных перфузировали под глубокой анестезией 10% хлоралгидратом, а затем 4% параформальдегидом.Затем мозг извлекали и фиксировали в формалине. После фиксации и дегидратации в градиенте этанола ткань мозга залили парафином и разрезали на коронковые срезы толщиной 4 мкм с помощью секционного ножа (Leica, Германия). Срезы (3 среза на крысу) окрашивали гематоксилином и эозином (H&E). Кроме того, по четыре крысы в каждой группе были подготовлены к окрашиванию H&E. Морфологию ПФК (коры головного мозга, покрывающей переднюю часть лобной доли) наблюдали под световым микроскопом (Olympus Corporation, Япония).
Transferase dUTP Nick End Labeling (TUNEL) Окрашивание
Четыре образца из каждой группы были приготовлены для концевого окрашивания дезоксинуклеотидилом TUNEL. Апоптоз выявляли с помощью набора TUNEL согласно протоколу производителя (DeadEnd Fluorometric kit, Promega, WI, USA). Затем предметные стекла контрастно окрашивали 4 ‘, 6-диамидино-2-фенилиндолом (DAPI), промывали, покрывали покровным стеклом на водной основе и закрывали лаком для ногтей. Были отобраны и визуализированы три поля микроскопа (20 ×), содержащих TUNEL-положительные клетки коры головного мозга.Количество TUNEL / DAPI-положительных клеток рассчитывали как среднее значение чисел, полученных из шести изображений на крысу. Подсчет производился слепым методом.
Иммунофлуоресцентная визуализация
Слайды( n = 4 образца на группу) фиксировали в 4% параформальдегиде в течение 20 минут и блокировали 10% козьей сывороткой в PBS. Затем слайды инкубировали в течение ночи в увлажненной камере при 4 ° C со следующими первичными антителами: NeuN (1: 100, Abcam, Кембридж, Массачусетс, США) и расщепленной каспазой-3 (1: 100, Cell Signaling Tech., Массачусетс, США). После инкубации первичных антител образцы промывали и инкубировали с соответствующим флуоресцентно-конъюгированным вторичным антителом (разведение 1: 500, Sigma-Aldrich) в течение 1 часа. Изображения были получены с помощью микроскопа Nikon TE2000U. Были выбраны и визуализированы три поля микроскопа (20 ×), содержащих расщепленные дважды положительные клетки каспаза-3 / NeuN в коре головного мозга. Количество активных дважды положительных клеток по каспазе-3 / NeuN рассчитывали как среднее значение чисел, полученных из шести изображений на крысу. Подсчет производился слепым методом.
Иммуногистохимия
Срезы депарафинизировали с использованием стандартной процедуры и промывали PBS, как описано ранее. Вкратце, после блокирования в течение 30 минут при комнатной температуре срезы инкубировали со следующими первичными антителами: CBS (1: 200, Santa Cruz Biotechnology, Санта-Крус, Калифорния, США) при 4 ° C в течение ночи. После инкубации первичных антител образцы промывали и инкубировали со вторичными антителами в течение 2 ч при комнатной температуре. Срезы промывали, а затем инкубировали с комплексом авидин-биотинилированный фермент в течение 1 ч при комнатной температуре.Срезы визуализировали диаминобензидином. Ядра контрастировали гематоксилином. Наконец, срезы обезвоживали в градиенте спирта и очищали ксилолом. Изображения были получены с помощью микроскопа Nikon TE2000U.
Подготовка проб для просвечивающей электронной микроскопии (ТЕМ)
Для ТЕА мы умерщвляли по три крысы на группу. Образцы ПФУ приблизительным объемом 1 мм 3 были быстро разрезаны на льду и зафиксированы в 2,5% глутаровом альдегиде в течение 2 часов при 4 ° C.После нескольких промывок в PBS образцы фиксировали в 1% тетроксиде осмия в течение 2 часов, а затем дегидратировали в серии градиентных этанолов. Затем ткани инфильтрировали пропиленоксидом 50/50 в течение ночи и заделывали. Ткани готовили для срезов на ультрамикротоме (EM UC 7, Leica, Германия) и разрезали на срезы толщиной 50 нм. После окрашивания уранилацетатом срезы исследовали под ТЕМ Hitachi H-7500.
Полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР)
Суммарную РНК экстрагировали из PFC с использованием реагента TRIzol (Gibco, Invitrogen) в соответствии с инструкциями производителя.Концентрацию РНК определяли с помощью спектрофотометра (Bio-Rad Labs) при 260 нм. Идентичные количества РНК (2 мкг) подвергали обратной транскрипции в кДНК с использованием коммерческого набора для ОТ-ПЦР (Fermentas, Вильнюс, Литва) в соответствии с инструкциями производителя. Затем кДНК амплифицировали с помощью ПЦР со специфическими праймерами (таблица 1). Продукты ПЦР, которые были разделены на геле 1,2% агарозы / TAE, визуализировали путем окрашивания бромидом этидия. Денситометрические значения были нормализованы к значениям β-актина.Интенсивность полосы определяли с помощью программного обеспечения Image-Pro Plus 6.0.
Таблица 1. Праймеры для ПЦР, использованные в этом исследовании .
Вестерн-блоттинг
Концентрацию белка в PFC определяли с использованием набора для анализа белка BCA (Pierce Biotechnology, Inc.). 30-50 мкг общих белков наносили на полиакриламидный гель с градиентом 4-20%, электрофоретически переносили на поливинилидендифторидную мембрану и зондировали следующими первичными антителами: антитело Bax (1: 1000, Santa Cruz Biotechnology, CA, США), антитело Bcl-2 (1: 1000, Santa Cruz Biotechnology), расщепленная каспаза-3 (1: 500, Cell Signaling Tech.Массачусетс, США), каспаза-3 (1: 1000, Cell Signaling), белок, связывающий элемент ответа фосфо-цАМФ (p-CREB) (1: 1000, Cell Signaling Tech., MA, США), CREB (1: 1000, Cell Signaling Tech., MA, США) и нейротрофический фактор головного мозга (BDNF) (1: 1000, Santa Cruz Biotechnology). β-актин (1: 2,000; Sigma-Aldrich) использовали в качестве внутреннего контроля. Вторичное антитело представляло собой пероксидазу хрена, конъюгированную с IgG козы / мыши против кроличьего IgG (1: 8000, Sigma-Aldrich). Мембраны были разработаны с использованием усовершенствованной системы обнаружения хемилюминесценции (Pierce, Rockford, IL, USA).
Статистический анализ
Для статистического анализа использовалсяSPSS 22.0. Неврологические баллы были проанализированы с помощью одностороннего дисперсионного анализа Краскела-Уоллиса (ANOVA) по рангам с последующим апостериорным тестом Данна . Остальные данные представлены как среднее ± стандартное отклонение; эти данные были проанализированы с помощью однофакторного дисперсионного анализа с последующим апостериорным анализом Тьюки. Различия считались достоверными при p <0,05.
Результаты
Влияние l-цистеина на активность CBS и продукцию H
2 S в ткани мозга, пораженной SAHСообщалось, что цистатионин-β-синтаза в основном локализуется в астроцитах в ЦНС и катализирует l-цистеин с образованием эндогенного H 2 S (22, 23).Здесь мы исследовали вызванные SAH изменения экспрессии CBS и активности CBS в ответ на обработку l-цистеином через 48 часов после SAH. В соответствии с предыдущими результатами наш иммуногистохимический анализ выявил многочисленные CBS-положительные клетки в ткани PFC групп Sham и Sham + l-цистеин, тогда как CBS-положительные клетки были очень редки в группе SAH (рис. 1A). Удивительно, но обработка l-цистеином значительно повысила экспрессию CBS в группе SAH (рис. 1A). Более того, экспрессия CBS в PFC была оценена через 48 часов после SAH с помощью вестерн-блоттинга и RT-PCR, и результаты показали, что l-цистеин также увеличивает уровни экспрессии белка и мРНК CBS (рис. 1B).
Фигура 1. Влияние l-цистеина на активность эндогенной цистатионин-β-синтазы (CBS). (A) Экспрессию CBS в клетках (показаны красными стрелками) определяли иммуногистохимическим методом через 48 часов после субарахноидального кровоизлияния (SAH). Масштабная линейка = 50 мкм ( n = 4). (B) CBS количественно определяли с помощью полимеразной цепной реакции с обратной транскрипцией и вестерн-блоттинга через 48 часов после SAH. Каждое значение было нормализовано по β-актину. Гистограммы, показывающие количественное определение уровней мРНК и белка CBS, были созданы с помощью Image-Pro Plus 6.0 ( n = 4). (C) Активность CBS оценивали через 48 часов после SAH ( n = 6). (D) Продукция эндогенного H 2 S оценивалась методом метиленового синего через 48 часов после SAH ( n = 8). Значения представляют собой средние значения ± стандартное отклонение. * p <0,05, ** p <0,01, *** p <0,001 SAH vs Sham, # p <0,05, ## p <0,05, ### п <0.001 SAH + l-Cys против SAH, + p <0,05, ++ p <0,01, +++ p <0,001 SAH + l-Cys + AOAA против SAH + l- Cys. AOAA, амино-оксиуксусная кислота.
Мы дополнительно оценили активность CBS, которая влияет на l-цистеин. Обе группы Sham + 1-цистеин и SAH + 1-цистеин продемонстрировали резкое повышение активности CBS, тогда как группа SAH показала низкую активность CBS (рис. 1C). Затем мы измерили продукцию H 2 S в ПФУ различных групп, поскольку продукция H 2 S является косвенным показателем активности CBS (24).Группы, обработанные l-цистеином (Sham + l-цистеин и SAH + l-цистеин) продуцировали больше H 2 S, чем группы Sham или SAH. Воздействие SAH немного снизило уровни H 2 S в PFC, но уровни в группе SAH существенно не отличались от уровней в группе Sham (рис. 1D). Совместное лечение с AOAA подавляло эффекты l-цистеина на SAH.
Введение l-цистеина уменьшило отек мозга и улучшило неврологическое поведение через 48 часов после SAH
По сравнению с группой Sham, группы SAH имели значительно более низкие неврологические показатели через 48 часов (рис. 2A).Лечение l-цистеином улучшило неврологические показатели, но этот лечебный эффект был отменен AOAA (рис. 2A).
Рис. 2. l-цистеин улучшает повреждение головного мозга, вызванное субарахноидальным кровоизлиянием (САК). (A) неврологических баллов были зарегистрированы через 48 часов после САК ( n = 6). (B) Содержание воды в коре головного мозга было измерено через 48 часов после САК ( n = 6). (C) Окрашивание H&E проводили на тканях мозга через 48 ч после САК.Патологические изменения включали очаговый отек в префронтальной коре (указаны черными стрелками) ( n = 4). Масштабная линейка = 100 мкм. Значения представляют собой среднее значение ± стандартное отклонение. ** p <0,01, *** p <0,001 SAH против Sham, # p <0,05, ## p <0,01 SAH + l-Cys против SAH, + p <0,05 SAH + l-Cys + AOAA по сравнению с SAH + l-Cys. AOAA, амино-оксиуксусная кислота.
Отек мозга (включая оба полушария головного мозга) оценивали сразу после неврологического обследования.Ткань мозга, поврежденная SAH, имела значительно более высокое содержание воды, чем ткань мозга Sham и Sham + l-цистеин. Инъекция l-цистеина после САК снизила содержание воды в головном мозге, но этот результат был отменен введением АОАА (рис. 2В).
В группах Sham и Sham + l-цистеина ткани мозга имели организованные структурные слои и корковые нейроны с четко определенными границами. Однако в группе SAH клетки были расположены редко, и очертания клеток были нечеткими.Более того, в группе SAH мы выявили значительный отек в области PFC, которая была бледной на вид, и сморщенные нейроны. Лечение l-цистеином уменьшило отек и морфологические повреждения, вызванные SAH (рис. 2C).
Кроме того, доза AOAA 5 мг / кг не вызывала дальнейшего повреждения нейронов после САК (см. Рисунок S1 в дополнительных материалах).
L-цистеин ослабляет SAH-индуцированное повреждение мозга за счет снижения апоптоза нейронов
В PFC крыс в группах Sham и Sham + l-цистеин TUNEL-положительные клетки выявлялись редко, тогда как в группе SAH было идентифицировано много TUNEL-положительных клеток.Апоптоз в ответ на SAH значительно улучшился при лечении l-цистеином, но этот эффект подавлялся введением AOAA (фиг. 3).
Рис. 3. l-цистеин ослабляет апоптоз, вызванный субарахноидальным кровоизлиянием (САК). (A) Обнаружение трансферазных dUTP nick end мечения (TUNEL) -положительных клеток в префронтальной коре выполняли через 48 часов после SAH. Масштабная линейка = 50 мкм. (B) Гистограммы, показывающие количественное определение TUNEL-положительных клеток ( n = 4).Масштабная линейка = 50 мкм. Значения представляют собой средние значения ± стандартное отклонение. *** p <0,001 SAH против Sham, ### p <0,001 SAH + l-Cys против SAH, ++ p <0,01 SAH + l-Cys + AOAA против SAH + l -Cys. AOAA, амино-оксиуксусная кислота.
l-цистеин ингибирует SAH-индуцированную активацию каспазы-3
Мы использовали двойное окрашивание расщепленной каспазой-3 / NeuN, чтобы оценить, как обработка l-цистеином ингибирует апоптоз после САК. Несколько расщепленных каспазо-3-положительных клеток были обнаружены в группах Sham и Sham + l-цистеина, тогда как многочисленные расщепленные клетки, дважды окрашенные каспазой-3 / NeuN, были обнаружены в группе SAH (Фигуры 4A, B).l-цистеин резко снижает уровни экспрессии расщепленной каспазы-3, но этот эффект блокируется AOAA. Эффект l-цистеина на SAH-индуцированную активацию каспазы-3 был подтвержден вестерн-блоттингом (фигуры 4C, D).
Рис. 4. Влияние l-цистеина на активацию каспазы-3 при субарахноидальном кровоизлиянии (САК). (A) Иммунофлуоресцентное окрашивание выявило совместную локализацию расщепленной каспазы-3 и NeuN в префронтальной коре через 48 часов после САК. Масштабная линейка = 50 мкм. (B) Гистограммы, показывающие количественное определение расщепленных каспазой-3 / NeuN-положительных клеток ( n = 4). (C) Экспрессию расщепленной каспазы-3 оценивали с помощью Вестерн-блоттинга. (D) Гистограммы, показывающие количественную оценку уровней протеина расщепленной каспазы-3 и каспазы-3, были созданы с помощью Image-Pro Plus 6.0. Результаты выражаются в виде отношения расщепленных каспаза-3 / каспаза-3 ( n = 3). Значения представляют собой среднее значение ± стандартное отклонение. * p <0,05, *** p <0,001 SAH vs Sham, # p <0,05, ### p <0.001 SAH + l-Cys против SAH, + p <0,05, +++ p <0,001 SAH + l-Cys + AOAA против SAH + l-Cys. AOAA, амино-оксиуксусная кислота.
l-цистеин восстановил уровни экспрессии Bcl-2 и Bax после SAH
Поскольку Bcl-2 и Bax являются ключевыми регуляторами пути митохондриального апоптоза в клетках, мы оценили уровни экспрессии Bcl-2 и Bax как на уровне мРНК, так и на уровне белка. Как показано на рисунке 5, SAH заметно увеличивал соотношение Bax / Bcl-2 на уровне мРНК и белка через 48 часов после травмы.Однако повышенное соотношение Bax / Bcl-2 было снижено обработкой l-цистеином. Эффект l-цистеина на вызванное SAH повышение отношения Bax / Bcl-2 было обращено AOAA (Фигуры 5A, B).
Фиг. 5. Эффекты l-цистеина на Bax и Bcl-2 на уровне мРНК и белка. (A) Относительные уровни экспрессии мРНК Bax и Bcl-2 в префронтальной коре (PFC) анализировали с помощью полуколичественной полимеразной цепной реакции с обратной транскрипцией. Плотность полос белка анализировали и нормализовали по β-актину ( n = 3). (B) Типичные вестерн-блоты, показывающие уровни Bax и Bcl-2 в PFC, и гистограммы, показывающие количественное определение уровней белков Bax и Bcl-2 ( n = 3). Уровни мРНК и белка были получены в трех независимых экспериментах. Значения представляют собой средние значения ± стандартное отклонение. ** p <0,01, *** p <0,001 субарахноидальное кровоизлияние (SAH) по сравнению с Sham, # p <0,05, ### p <0,001 SAH + l-Cys по сравнению с SAH , + п <0.05, ++ p <0,01 SAH + l-Cys + AOAA по сравнению с SAH + l-Cys. AOAA, амино-оксиуксусная кислота.
l-цистеин увеличивал экспрессию BDNF после повреждения, вызванного SAH
Чтобы определить, может ли l-цистеин влиять на выработку нейропротекторных факторов, концентрацию BDNF в PFC измеряли через 48 часов после САК. Как показано на рисунке 6A, уровень экспрессии мРНК BDNF был значительно ниже через 48 часов в группе SAH, чем в группе Sham. l-цистеин значительно увеличивал уровень экспрессии мРНК BDNF в PFC через 48 часов после воздействия SAH (фиг. 6A).В соответствии с изменениями в мРНК, SAH-индуцированное снижение уровней белка BDNF также было обращено обработкой l-цистеином, но эффект l-цистеина был обращен AOAA (фиг. 6B).
Фигура 6. Влияние l-цистеина на уровни экспрессии нейротрофического фактора головного мозга (BDNF) на уровнях мРНК и белка. (A) Уровни экспрессии BDNF на уровне мРНК в префронтальной коре оценивали с помощью полуколичественной полимеразной цепной реакции с обратной транскрипцией через 48 часов после субарахноидального кровоизлияния (SAH).Каждое значение было нормализовано по β-актину. Гистограммы, показывающие количественную оценку уровней мРНК BDNF, были созданы с помощью Image-Pro Plus 6.0 ( n = 4). (B) Уровень экспрессии белка BDNF анализировали вестерн-блоттингом через 48 часов после SAH, и β-актин использовали для оценки нагрузки белка. Гистограммы, показывающие количественное определение уровней белка BDNF, были созданы с помощью Image-Pro Plus 6.0 ( n = 3). Значения представляют собой среднее значение ± стандартное отклонение. * р <0.05, *** p <0,001 SAH против Sham, # p <0,05, ### p <0,001 SAH + l-Cys против SAH, + p <0,05, ++ p <0,01 SAH + l-Cys + AOAA по сравнению с SAH + l-Cys. AOAA, амино-оксиуксусная кислота.
Введение l-цистеина улучшает фосфорилирование CREB
In vivoФосфорилированный CREB регулирует транскрипцию нескольких генов, которые кодируют молекулы, участвующие в пластичности нейронов, включая BDNF, тирозингидроксилазу и молекулу адгезии нервных клеток; эти молекулы связаны со стрессовой реакцией.Таким образом, мы исследовали уровни фосфорилирования CREB после лечения SAH и l-цистеином. Как показано на Фигуре 7, экспрессия фосфорилированного CREB значительно снизилась через 48 часов после SAH по сравнению с таковой в группе Sham. Обработка l-цистеином значительно увеличивала уровень экспрессии фосфорилированного CREB в PFC через 48 часов после воздействия SAH. Кроме того, действие l-цистеина на уровни фосфорилирования CREB, индуцированные SAH, было обращено AOAA.
Фигура 7. Влияние l-цистеина на фосфорилирование CREB после субарахноидального кровоизлияния (SAH) .Через 48 ч после SAH экстракты цельной префронтальной коры подвергали Вестерн-блоттингу с использованием антител против белка, связывающего элемент фосфо-цАМФ (p-CREB) и CREB. Гистограммы, показывающие количественную оценку уровней экспрессии p-CREB / CREB, были созданы с помощью Image-Pro Plus 6.0 ( n = 3). Значения представляют собой средние значения ± стандартное отклонение. *** p <0,001 SAH против Sham, ### p <0,001 SAH + l-Cys против SAH, ++ p <0.001 SAH + l-Cys + AOAA против SAH + l-Cys. AOAA, амино-оксиуксусная кислота.
Влияние l-цистеина на синаптическую структуру и экспрессию синаптофизина и PSD95 после SAH
Повреждение нейронов, включая коллапс синапсов, происходит после САК; поэтому мы исследовали морфологические изменения в синапсах ПФК с помощью ПЭМ. По сравнению с группами Sham и Sham + l-цистеина (фигура 8), группа SAH показала нечеткие структурные изменения в синапсах, которые включали опухшие границы и темное окрашивание, что указывало на дегенерацию.Кроме того, количество нормальных синапсов уменьшилось в группе SAH. Обработка l-цистеином резко уменьшила синаптическое повреждение и увеличила количество синапсов в группе SAH, тогда как эффекты l-цистеина были отменены AOAA.
Рис. 8. Влияние лечения l-цистеином на синаптические изменения в префронтальной коре (ПФК) . Типичные изображения просвечивающей электронной микроскопии PFC из каждой группы. Стрелками указаны регулярные синаптические структуры.Звездочки обозначают разрушенные синапсы. Масштабная шкала = 500 нм.
Затем мы измерили уровень пресинаптического маркера синаптофизина и постсинаптического маркера PSD95. Синаптофизин был значительно снижен как на уровне мРНК, так и на уровне белка в группе SAH. Лечение l-цистеином значительно увеличивало экспрессию синаптофизина в PFC через 48 часов после воздействия SAH. Однако, по сравнению с группой Sham, уровни мРНК и белка PSD95 были значительно увеличены через 48 часов в группе SAH (Фигуры 9A, B).l-цистеин значительно снижал экспрессию PSD95 в PFC через 48 часов после воздействия SAH. АОАА обращает действие l-цистеина на уровни экспрессии синаптофизина и PSD95.
Рис. 9. Влияние лечения l-цистеином на уровни экспрессии синаптофизина и PSD95 в префронтальной коре (ПФК). (A) Уровни мРНК синаптофизина и PSD95 измеряли полуколичественной полимеразной цепной реакцией с обратной транскрипцией. Каждое значение было нормализовано по β-актину.Гистограммы, показывающие количественную оценку уровней мРНК синаптофизина и PSD95, были созданы с помощью Image-Pro Plus 6.0 ( n = 3). (B) Через 48 часов после субарахноидального кровоизлияния (SAH) цельные экстракты PFC подвергали Вестерн-блоттингу с использованием антител против синаптофизина и PSD95. Гистограммы, показывающие количественную оценку уровней мРНК синаптофизина и PSD95, были созданы с помощью Image-Pro Plus 6.0 ( n = 3). Значения представляют собой среднее значение ± стандартное отклонение трех независимых экспериментов.* p <0,05, ** p <0,01, *** p <0,001 SAH против Sham, # p <0,05, ## p <0,01 SAH + l-Cys против SAH, + p <0,05 SAH + l-Cys + AOAA против SAH + l-Cys. AOAA, амино-оксиуксусная кислота.
Обсуждение
В текущем исследовании мы продемонстрировали, что l-цистеин может повышать уровни H 2 S в мозге через взаимодействие с CBS; Кроме того, l-цистеин играет нейропротекторную роль при SAH, уменьшая отек мозга и апоптоз нейронов.Более того, l-цистеин сенсибилизировал путь CREB – BDNF и усиливал экспрессию белков, связанных с синаптической пластичностью. Положительные эффекты, инициированные l-цистеином, были значительно отменены при введении антагониста CBS AOAA.
Цистатионин-β-синтаза представляет собой пиридоксаль-5′-фосфат-зависимый фермент, который катализирует β-замену, в которой β-положение субстрата замещается нуклеофилом YH (25) и преобразует субстраты в 2-меркаптоэтанол и H 2 S (26, 27).Обнаружена тесная связь между мутациями в нескольких регионах гена CBS человека и психическими расстройствами и сосудистыми заболеваниями (28). В головном мозге крысы CBS экспрессируется более высоко, чем цистатионин-γ-лиаза, и в основном отвечает за генерацию H 2 S (7). l-цистеин, аминокислота, содержащая электроотрицательный заместитель -SH, является предпочтительным субстратом для H 2 S, на долю которого приходится 70% продукции H 2 S (29). Ли и др. продемонстрировали, что введение l-цистеина усиливает выработку H 2 S, тогда как AOAA заметно ослабляет эффекты l-цистеина дозозависимым образом (30).В исследовании Kmamt введение NaHS, a, донора H 2 S, обращало вспять снижение экспрессии CBS, фермента, метаболизирующего H 2 S (31). В нашем исследовании l-цистеин сначала вводили животным посредством интрацеребровентрикулярной инъекции через 30 минут после САК, и увеличивали активность и экспрессию CBS в PFC, что согласуется с уровнями продукции H 2 S. Мы предполагаем, что l-цистеин вызывает потенциальную петлю обратной связи для увеличения активности CBS в ответ на SAH и увеличения продукции H 2 S для оказания нейропротекторных эффектов.
Апоптоз клеток является основной характеристикой EBI, и митохондриальный путь также может быть задействован (32). Кроме того, недавно было показано, что экзогенный H 2 S защищает от глобальной и очаговой церебральной ишемии / реперфузионного повреждения (33, 34). Однако остается неизвестным, может ли H 2 S сохранять нейроны посредством метаболизма l-цистеина после САК. В нашем исследовании мы наблюдали многочисленные TUNEL-положительные клетки в ЦНС в группе САК, что согласуется с отчетом Чена (35).Введение l-цистеина может уменьшить количество апоптотических клеток, индуцированных SAH. Тем временем мы дополнительно исследовали соотношение Bax / Bcl-2. Член семейства Bcl-2, Bax, значительно усиливался после SAH, что приводило к высвобождению цитохрома c в цитозоль (32). Мы обнаружили, что индуцированная SAH повышающая регуляция соотношения Bax / Bcl-2 может быть отменена введением l-цистеина. Кроме того, мы проанализировали активацию каспазы-3; Высвобождение цитохрома c запускает расщепление белка каспазы-3, что приводит к фрагментации ДНК и апоптозу (36).Ингибирование расщепленной каспазы-3 может снизить потерю нейронов в моделях SAH (37). Наши данные показали, что обработка l-цистеином предотвращает вызванное SAH увеличение расщепленной каспазы-3 в PFC. Наши результаты показывают, что l-цистеин может защищать нейроны от апоптоза после САК. Однако, когда AOAA вводили с l-цистеином, все положительные эффекты на апоптоз были отменены. Таким образом, мы предполагаем, что нейропротекторное действие l-цистеина на SAH может быть связано с увеличением эндогенного H 2 S.
Нейротрофический фактор головного мозга является фактором роста и поддерживает выживание, пластичность и нейрогенез нейронов (38, 39). Более того, BDNF участвует в патофизиологии SAH. Например, клинические данные показали, что полиморфизм BDNF связан с плохим выздоровлением пациента от САК (40, 41). Эксперименты на животных показали, что инфузия экзогенного BDNF или усиление его экспрессии улучшает нейроповеденческие исходы после САК (42, 43). Что касается основных механизмов нейропротекторного действия BDNF на апоптоз нейронов, некоторые исследования показали, что эти эффекты зависят от активации сигнального каскада PI3K / Akt и / или ERK, который впоследствии активирует фосфорилирование CREB и способствует выживанию нейронов (44, 45).В предыдущих исследованиях сообщалось, что H 2 S способствует экспрессии BDNF, а блокирование пути BDNF-TrkB обращает H 2 S-опосредованную нейрозащиту против апоптоза и окислительного стресса в нейронах (46, 47). Более того, H 2 S может активировать сигнальный путь CREB и предотвращать ишемическое реперфузионное повреждение головного мозга (48). В нашем исследовании уровни экспрессии p-CREB и BDNF увеличивались после введения l-цистеина, что позволяет предположить, что H 2 S может активировать сигнальный путь CREB и увеличивать экспрессию расположенного ниже гена выживания, BDNF.Важно отметить, что эти открытия повышают вероятность того, что H 2 S оказывает антиапоптотические эффекты посредством активации p-CREB и BDNF в PFC. Учитывая, что AOAA блокирует CBS, катализатор l-цистеина, и снижает продукцию H 2 S, мы предполагаем, что l-цистеин моделирует экспрессию CREB-BDNF в CNS через , индуцируя H 2 S во время SAH.
Недавно Шен и др. сообщили, что повреждение нейронов, включая коллапс синапсов, происходит после САК (49).Синапсы — важные структурные единицы для передачи информации в головном мозге. Накапливающиеся данные продемонстрировали, что изменения плотности синапсов сильно коррелируют с когнитивным статусом (50, 51). Синаптофизин и PSD95 являются надежными маркерами для косвенной оценки целостности и функции синапсов (52, 53). Синаптофизин является маркером конечной плотности пресинаптического нерва, который важен для слияния везикул и высвобождения нейромедиатора (54). Снижение синаптофизина при заболеваниях ЦНС указывает на снижение синаптической пластичности (55).PSD95 — это каркасный белок, который закрепляет и организует рецепторы NMDA и контролирует количество и размер дендритных шипов (56). Мы продемонстрировали, что инъекция l-цистеина после САК значительно ослабляет синаптическое повреждение за счет уменьшения структурной дегенерации и увеличения количества здоровых синапсов. На уровнях мРНК и белка снижение синаптофизина происходит при SAH, и уровни синаптофизина улучшаются при введении l-цистеина, что указывает на потенциальную роль H 2 S в стимулировании изменений уровней синаптофизина.К нашему удивлению, мы заметили, что PSD95 активируется после SAH; Напротив, предыдущие исследования показали, что экспрессия PSD95 снижается при различных заболеваниях головного мозга (57, 58). Мы дополнительно показали, что l-цистеин может подавлять экспрессию PSD95. Мы постулируем, что взаимодействия между PSD95 и рецептором NMDA усиливаются после САК, что приводит к повреждению нейронов. Однако AOAA не блокирует действие l-цистеина на экспрессию PSD95 при SAH. Улучшение, вызванное l-цистеином, не может быть достигнуто за счет регуляции PSD95 с помощью H 2 S, как мы ожидали.
У нашего исследования есть несколько ограничений. Во-первых, мы использовали AOAA для блокирования активности CBS и функции l-цистеина, но в ЦНС есть другие ферменты, которые могут продуцировать H 2 S, такие как 3-меркаптопируват-серотрансфераза, которые необходимо изучить в будущих исследованиях (6). Во-вторых, хотя апоптоз является основным фактором EBI, другие факторы, включая церебральный вазоспазм, воспаление и окислительный стресс, также могут быть ответственны за развитие EBI при SAH (2, 59). Чтобы определить, оказывает ли l-цистеин положительное влияние на эти факторы, и изучить потенциальный механизм, лежащий в основе его эффектов, потребуются дополнительные исследования.В-третьих, не было установлено, как l-цистеин регулирует экспрессию синаптофизина и PSD95 и как эти факторы влияют на неврологическую функцию (31, 60). Наконец, необходимо дополнительно уточнить способ, время и дозировку лечения l-цистеином.
Таким образом, лечение l-цистеином может облегчить развитие EBI, индуцированного SAH, посредством нескольких механизмов, включая уменьшение апоптоза клеток, усиление экспрессии BDNF-CREB и повышение плотности синапсов за счет активации системы CBS / H 2 S.
Заявление об этике
Международные руководящие принципы исследований на животных, установленные CIOMS и принятые Центром лабораторных животных при Университете Шаньдун, в целом соблюдались при обращении с животными и уходе за ними. Исследователи, работающие с животными, систематически обучались в соответствии с руководством Институционального комитета по уходу и использованию животных (IACUC). Эвтаназию для животных моделей проводили в соответствии с инструкциями в «Руководстве AVMA по эвтаназии животных: издание 2013 года».«Все усилия были предприняты для уменьшения количества используемых животных и уменьшения их страданий в соответствии с принципами 3R. Протокол был одобрен этическим комитетом больницы Цилу.
Взносы авторов
GL и ZW участвовали в разработке исследования, интерпретации данных и написании рукописи; TL и LXW выполнили большинство экспериментов и внесли свой вклад в анализ данных; QH, SL, XMB и YKX были ответственны за модель на животных; TTZ и SSB отвечали за вестерн-блоттинг; а XQG и SHW отвечали за подготовку патологических срезов.Авторы не заявляют о конфликте интересов.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Финансирование
Эта работа была поддержана при финансовой поддержке Национального фонда естественных наук Китая (№ 81571284, 81671213), Фонда фундаментальных исследований Шаньдунского университета (2015JC008) и Плана развития науки и технологий провинции Шаньдун (2013GSF11804).
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу https://www.frontiersin.org/article/10.3389/fneur.2017.00176/full#supplementary-material.
Сокращения
AOAA, аминооксиуксусная кислота; BDNF, нейротрофический фактор головного мозга; CBS, цистатионин-β-синтаза; ЦНС, центральная нервная система; CREB, белок, связывающий элемент ответа цАМФ; p-CREB, белок, связывающий элемент ответа фосфо-цАМФ; ДАБ, диаминобензидин; DAPI, 4 ‘, 6-диамидино-2-фенилиндол дигидрохлорид; EBI — ранняя черепно-мозговая травма; H 2 S, сероводород; ИГХ — иммуногистохимическое окрашивание; NNDPD, N , N -диметил- p -фенилендиаминсульфат; САК — субарахноидальное кровоизлияние; ПЭМ, просвечивающая электронная микроскопия.
Список литературы
1. Bederson JB, Connolly ES Jr, Batjer HH, Dacey RG, Dion JE, Diringer MN, et al. Рекомендации по ведению аневризматического субарахноидального кровоизлияния: заявление для медицинских работников специальной группы авторов Совета по инсульту Американской кардиологической ассоциации. Инсульт (2009) 40: 994–1025. DOI: 10.1161 / STROKEAHA.108.1
CrossRef Полный текст | Google Scholar
3. Конрад М., Сато Х. Индуцируемый окислительным стрессом цистин / глутаматный антипортер, система x (c) (-): поставщик цистина и не только. Аминокислоты (2012) 42: 231–46. DOI: 10.1007 / s00726-011-0867-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Джонс Д.П., Гоу Ю.М., Андерсон К.Л., Зиглер Т.Р., Кинкейд Дж.М. мл., Кирлин В.Г. Пара цистеин / цистин — это недавно обнаруженный узел в схеме биологической окислительно-восстановительной передачи сигналов и контроля. FASEB J (2004) 18: 1246–8. DOI: 10.1096 / fj.03-0971fje
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Кумар П., Маурья П.К.Отток l-цистеина в эритроциты в зависимости от возраста человека: корреляция с восстановленным глутатионом и общим антиоксидантным потенциалом. Rejuvenation Res (2013) 16: 179–84. DOI: 10.1089 / rej.2012.1394
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Абэ К., Кимура Х. Возможная роль сероводорода как эндогенного нейромодулятора. J Neurosci (1996) 16: 1066–71.
PubMed Аннотация | Google Scholar
8. Asimakopoulou A, Panopoulos P, Chasapis CT, Coletta C, Zhou Z, Cirino G, et al.Селективность обычно используемых фармакологических ингибиторов цистатионин-бета-синтазы (CBS) и цистатионин-гаммалиазы (CSE). Br J Pharmacol (2013) 169: 922–32. DOI: 10.1111 / bph.12171
CrossRef Полный текст | Google Scholar
11. Ху Л.Ф., Вонг П.Т., Мур П.К., Биан Дж. С.. Сероводород ослабляет воспаление, вызванное липополисахаридом, путем ингибирования митоген-активируемой протеинкиназы p38 в микроглии. J Neurochem (2007) 100: 1121–8. DOI: 10.1111 / j.1471-4159.2006.04283.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
13. Zhang Q, Yuan L, Liu D, Wang J, Wang S, Zhang Q, et al. Сероводород снижает нейротоксичность, вызванную гипоксией, за счет ингибирования активации микроглии. Pharmacol Res (2014) 84: 32–44. DOI: 10.1016 / j.phrs.2014.04.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14. Wang Z, Zhan J, Wang X, Gu J, Xie K, Zhang Q, et al. Гидросульфид натрия предотвращает нарушение поведения новорожденных мышей, вызванное гипоксией. Brain Res (2013) 1538: 126–34. DOI: 10.1016 / j.brainres.2013.09.043
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Ван З., Лю Д. X., Ван Ф. В., Чжан Кью, Ду З. X, Чжан Дж. М. и др. l-цистеин способствует пролиферации и дифференцировке нервных стволовых клеток через путь CBS / H (2) S. Неврология (2013) 237: 106–17. DOI: 10.1016 / j.neuroscience.2012.12.057
CrossRef Полный текст | Google Scholar
16. Рой А., Хан А.Х., Ислам М.Т., Прието М.С., Маджид Д.С.Взаимозависимость цистатион-гамма-лиазы и цистатион-бета-синтазы в регуляции артериального давления у крыс, индуцированной сероводородом. Am J Hypertens (2012) 25: 74–81. DOI: 10.1038 / ajh.2011.149
CrossRef Полный текст | Google Scholar
17. Цуй И, Дуань Х, Ли Х, Данг Б., Инь Дж, Ван И и др. Сероводород улучшает раннее повреждение головного мозга после субарахноидального кровоизлияния у крыс. Мол, нейробиол (2016) 53: 3646–57. DOI: 10.1007 / s12035-015-9304-1
CrossRef Полный текст | Google Scholar
18.Ли Т., Лю Х., Сюэ Х, Чжан Дж., Хань Х, Янь С. и др. Нейропротекторные эффекты сероводорода против раннего повреждения головного мозга и вторичных когнитивных нарушений после субарахноидального кровоизлияния. Brain Pathol (2016) 27: 51–63. DOI: 10.1111 / bpa.12361
CrossRef Полный текст | Google Scholar
19. Гарсия JH, Вагнер S, Лю К.Ф., Ху XJ. Неврологический дефицит и степень нейронального некроза, связанного с окклюзией средней мозговой артерии у крыс. Статистическая проверка. Stroke (1995) 26: 627–34; Обсуждение 635.DOI: 10.1161 / 01.STR.26.4.627
CrossRef Полный текст | Google Scholar
20. Хасэгава Ю., Сузуки Х., Алтай О., Чжан Дж. Х. Сохранение передачи сигналов тропомиозин-связанной киназы B (TrkB) ортованадатом натрия ослабляет раннее повреждение головного мозга после субарахноидального кровоизлияния у крыс. Инсульт (2011) 42: 477–83. DOI: 10.1161 / STROKEAHA.110.597344
PubMed Аннотация | CrossRef Полный текст | Google Scholar
21. Fujii M, Sherchan P, Krafft PR, Rolland WB, Soejima Y, Zhang JH.Стимуляция каннабиноидного рецептора 2 типа ослабляет отек мозга за счет уменьшения инфильтрации церебральных лейкоцитов после субарахноидального кровоизлияния у крыс. J Neurol Sci (2014) 342: 101–6. DOI: 10.1016 / j.jns.2014.04.034
PubMed Аннотация | CrossRef Полный текст | Google Scholar
22. Кимура Х. Сигнализация сероводорода и полисульфидов. Антиоксидный окислительно-восстановительный сигнал (2015) 22: 347–9. DOI: 10.1089 / ars.2014.5869
CrossRef Полный текст | Google Scholar
23.Enokido Y, Suzuki E, Iwasawa K, Namekata K, Okazawa H, Kimura H. Цистатионин-бета-синтаза, ключевой фермент метаболизма гомоцистеина, предпочтительно экспрессируется в линии радиальной глии / астроцитов развивающейся ЦНС мыши. FASEB J (2005) 19: 1854–6. DOI: 10.1096 / fj.05-3724fje
PubMed Аннотация | CrossRef Полный текст | Google Scholar
24. Миямото Р., Оцугуро К., Ямагути С., Ито С. Нейрональная регуляция экспрессии производящего сероводород фермента цистатионин-бета-синтазы в астроцитах спинного мозга крыс. Neurosci Res (2015) 97: 52–9. DOI: 10.1016 / j.neures.2015.03.003
CrossRef Полный текст | Google Scholar
25. Miles EW, Kraus JP. Цистатионин-бета-синтаза: структура, функция, регуляция и расположение мутаций, вызывающих гомоцистинурию. J Biol Chem (2004) 279: 29871–4. DOI: 10.1074 / jbc.R400005200
CrossRef Полный текст | Google Scholar
26. Браунштейн А.Е., Горяченкова Е.Пиридоксаль-Р-зависимые лиазы, специфичные для b-замены. Adv Enzymol Relat Areas Mol Biol (1984) 56: 1–89.
Google Scholar
27. Хилл Р., Спенсер И. Пиридоксальфосфат: химические, биохимические и медицинские аспекты. Доктор Дельфин DNY-L . Нью-Йорк: Уайли и сыновья (1986). п. 131–222.
Google Scholar
28. Валлийский М., Рэмси Б., Аккурсо Ф., Каттинг Дж., Скрайвер С., Боде А. и др. Метаболические и молекулярные основы наследственного заболевания. 8 -е изд. McGraw-Hill Professional (2001).п. 5085–108.
Google Scholar
30. Сяо А., Ли Дж., Лю Т., Лю З., Вэй С., Сюй Х и др. l-цистеин усиливает всасывание питательных веществ через производный цистатионин-бета-синтазы путь h3 S в тощей кишке грызунов. Clin Exp Pharmacol Physiol (2016) 43: 562–8. DOI: 10.1111 / 1440-1681.12562
CrossRef Полный текст | Google Scholar
31. Камат П.К., Кайлес П., Калани А., Тьяги Н. Сероводород улучшает вызванную гомоцистеином патологию, подобную болезни Альцгеймера, нарушение гематоэнцефалического барьера и синаптическое расстройство. Мол, нейробиол (2016) 53: 2451–67. DOI: 10.1007 / s12035-015-9212-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
32. Кэхилл Дж., Калверт Дж. В., Маркантонио С., Чжан Дж. Х. p53 может играть роль организатора в апоптотической гибели клеток после экспериментального субарахноидального кровоизлияния. Нейрохирургия (2007) 60: 531–45; обсуждение 545. doi: 10.1227 / 01.NEU.0000249287.99878.9B
PubMed Аннотация | CrossRef Полный текст | Google Scholar
33.Гейби С., Обалеб Н., Хаксари М., Калалян-Могхаддам Х., Вакили А., Асади Ю. и др. Сероводород защищает мозг от ишемического реперфузионного повреждения в преходящей модели фокальной церебральной ишемии. J Mol Neurosci (2014) 54: 264–70. DOI: 10.1007 / s12031-014-0284-9
CrossRef Полный текст | Google Scholar
34. Цзян Ц., Ли К., Мануэль М.Л., Юань С., Кевил К.Г., Маккартер К.Д. и др. Роль сероводорода в раннем нарушении гематоэнцефалического барьера после преходящей очаговой ишемии головного мозга. PLoS One (2015) 10: e0117982. DOI: 10.1371 / journal.pone.0117982
PubMed Аннотация | CrossRef Полный текст | Google Scholar
35. Chen J, Wang L, Wu C, Hu Q, Gu C, Yan F, et al. Аутофагия, усиленная мелатонином, защищает от апоптоза нервов через митохондриальный путь при раннем повреждении головного мозга после субарахноидального кровоизлияния. J Pineal Res (2014) 56: 12–9. DOI: 10.1111 / jpi.12086
PubMed Аннотация | CrossRef Полный текст | Google Scholar
36.Slee EA, Harte MT, Kluck RM, Wolf BB, Casiano CA, Newmeyer DD и др. Упорядочивание каскада каспаз, инициированного цитохромом с: иерархическая активация каспаз-2, -3, -6, -7, -8 и -10 зависимым от каспазы-9 образом. J Cell Biol (1999) 144: 281–92. DOI: 10.1083 / jcb.144.2.281
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37. Парк С., Ямагути М., Чжоу С., Калверт Дж. У., Тан Дж., Чжан Дж. Х. Нейроваскулярная защита снижает вероятность раннего повреждения головного мозга после субарахноидального кровоизлияния. Инсульт (2004) 35: 2412–7. DOI: 10.1161 / 01.STR.0000141162.29864.e9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
40. Siironen J, Juvela S, Kanarek K, Vilkki J, Hernesniemi J, Lappalainen J. Аллель Met полиморфизма BDNF Val66Met предсказывает плохой исход у выживших после аневризматического субарахноидального кровоизлияния. Инсульт (2007) 38: 2858–60. DOI: 10.1161 / STROKEAHA.107.485441
PubMed Аннотация | CrossRef Полный текст | Google Scholar
41.Вилкки Дж., Лаппалайнен Дж., Ювела С., Канарек К., Хернесниеми Дж. А., Сийронен Дж. Связь аллеля Met нейротрофического фактора мозга Val66Met с памятью после аневризматического субарахноидального кровоизлияния. Нейрохирургия (2008) 63: 198–203; обсуждение 203. doi: 10.1227 / 01.NEU.0000320382.21577.8E
PubMed Аннотация | CrossRef Полный текст | Google Scholar
42. Тан Дж., Ху Ц., Чен Й, Лю Ф., Чжэн И, Тан Дж и др. Нейропротекторная роль производного N-ацетилсеротонина через активацию рецептора B тропомиозин-связанной киназы после субарахноидального кровоизлияния на модели крыс. Neurobiol Dis (2015) 78: 126–33. DOI: 10.1016 / j.nbd.2015.01.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
43. Zhang ZY, Yang MF, Wang T, Li DW, Liu YL, Zhang JH и др. Цистеамин облегчает раннее повреждение головного мозга за счет снижения окислительного стресса и апоптоза в экспериментальной модели субарахноидального кровоизлияния на крысах. Cell Mol Neurobiol (2015) 35: 543–53. DOI: 10.1007 / s10571-014-0150-x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
44.Ся Й, Ван Ч.З., Лю Дж., Анастасио Н.К., Джонсон К.М. Нейротрофический фактор головного мозга предотвращает индуцированный фенциклидином апоптоз в развивающемся головном мозге путем параллельной активации путей ERK и PI-3K / Akt. Нейрофармакология (2010) 58: 330–6. DOI: 10.1016 / j.neuropharm.2009.10.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
45. Papadia S, Hardingham GE. Дихотомия передачи сигналов рецептора NMDA. Невролог (2007) 13: 572–9. DOI: 10.1177/1073858407305833
CrossRef Полный текст | Google Scholar
46. Jiang JM, Zhou CF, Gao SL, Tian Y, Wang CY, Wang L, et al. Путь BDNF-TrkB опосредует нейрозащиту сероводорода от токсичности, вызванной формальдегидом, для клеток PC12. PLoS One (2014) 10: e0119478. DOI: 10.1371 / journal.pone.0119478
CrossRef Полный текст | Google Scholar
47. Wei HJ, Xu JH, Li MH, Tang JP, Zou W., Zhang P, et al. Сероводород подавляет индуцированный гомоцистеином стресс эндоплазматического ретикулума и апоптоз нейронов в гиппокампе крыс за счет активации пути BDNF-TrkB. Acta Pharmacol Sin (2014) 35: 707–15. DOI: 10.1038 / апс.2013.197
PubMed Аннотация | CrossRef Полный текст | Google Scholar
48. Dai HB, Ji X, Zhu SH, Hu YM, Zhang LD, Miao XL, et al. Сероводород и умеренная гипотермия активируют сигнальный путь CREB и предотвращают ишемическое реперфузионное повреждение. BMC Anesthesiol (2015) 15: 119. DOI: 10.1186 / s12871-015-0097-6
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49. Шен Х, Чен З, Ван И, Гао А, Ли Х, Цуй И и др.Роль нейрексина-1бета и нейролигина-1 в когнитивной дисфункции после субарахноидального кровоизлияния у крыс. Инсульт (2015) 46: 2607–15. DOI: 10.1161 / STROKEAHA.115.009729
CrossRef Полный текст | Google Scholar
50. Думитриу Д., Хао Дж., Хара Й., Кауфманн Дж., Янссен В.Г., Лу В. и др. Избирательные изменения плотности и морфологии тонкого позвоночника в префронтальной коре головного мозга обезьян коррелируют с когнитивными нарушениями, связанными со старением. J Neurosci (2010) 30: 7507-15. DOI: 10.1523 / JNEUROSCI.6410-09.2010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
51. Chen KS, Masliah E, Mallory M, Gage FH. Синаптическая потеря у пожилых крыс с когнитивными нарушениями улучшается за счет хронической инфузии фактора роста нервов человека. Неврология (1995) 68: 19–27. DOI: 10.1016 / 0306-4522 (95) 00099-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
52. Гланц Л.А., Гилмор Дж. Х., Хамер Р. М., Либерман Дж. А., Ярског Л. Ф.. Синаптофизин и белок постсинаптической плотности 95 в префронтальной коре головного мозга человека от середины беременности до ранней взрослой жизни. Неврология (2007) 149: 582–91. DOI: 10.1016 / j.neuroscience.2007.06.036
PubMed Аннотация | CrossRef Полный текст | Google Scholar
53. Zhang L, Luo J, Zhang M, Yao W., Ma X, Yu SY. Влияние куркумина на хроническое, непредсказуемое, легкое, вызванное стрессом депрессивное поведение и структурную пластичность боковой миндалины крыс. Int J Neuropsychopharmacol (2014) 17: 793–806. DOI: 10.1017 / S1461145713001661
PubMed Аннотация | CrossRef Полный текст | Google Scholar
55.Cunha GM, Canas PM, Oliveira CR, Cunha RA. Повышенная плотность и синаптопротекторный эффект аденозиновых рецепторов A2A при субхроническом ограничительном стрессе. Неврология (2006) 141: 1775–81. DOI: 10.1016 / j.neuroscience.2006.05.024
PubMed Аннотация | CrossRef Полный текст | Google Scholar
56. Эль-Хусейни А.Е., Шнелл Е., Четкович Д.М., Николл Р.А., Бредт Д.С. PSD-95 участвует в созревании возбуждающих синапсов. Science (2000) 290: 1364–8. DOI: 10.1126 / наука.290,5495,1364
PubMed Аннотация | CrossRef Полный текст | Google Scholar
57. Scheff SW, Price DA, Schmitt FA, Scheff MA, Mufson EJ. Синаптическая потеря в нижней височной извилине при легких когнитивных нарушениях и болезни Альцгеймера. J. Alzheimers Dis. (2011) 24: 547–57. DOI: 10.3233 / JAD-2011-101782
PubMed Аннотация | CrossRef Полный текст | Google Scholar
58. Цай Н.П., Вилкерсон Дж. Р., Го В., Максимова М. А., ДеМартино Г. Н., Коуэн К. В. и др. Множественные связанные с аутизмом гены опосредуют элиминацию синапсов через протеасомную деградацию синаптического каркаса PSD-95. Cell (2012) 151: 1581–94. DOI: 10.1016 / j.cell.2012.11.040
PubMed Аннотация | CrossRef Полный текст | Google Scholar
60. Камат П.К., Калани А., Гиввимани С., Сатнур П., Тьяги С., Тьяги Н. Сероводород ослабляет нейродегенерацию и нервно-сосудистую дисфункцию, вызванную внутримозговым введением гомоцистеина у мышей. Неврология (2013) 252: 302–19. DOI: 10.1016 / j.neuroscience.2013.07.051
PubMed Аннотация | CrossRef Полный текст | Google Scholar
L-цистеин | Восстановитель | Ингредиенты для выпечки
Происхождение
Продукты, богатые l-цистеином, известны своей пользой для здоровья со времен средневековья.Куриные мацераты, содержащие его, часто использовали для лечения астмы. Лекарства на основе производных до сих пор используются при астме и других хронических обструктивных заболеваниях легких (ХОБЛ).
Хотя l-цистеин может быть получен из источников животного и даже человеческого происхождения, таких как гусиные и утиные перья, человеческий волос, свиная щетина и копыта, существует также хорошо зарекомендовавший себя процесс ферментации с использованием растительного крахмала в качестве сырья. 1
- Химическая структура L-цистеина.
Промышленное производство
Традиционный процесс производства l-цистеина начинается с кипячения сырья (пера или волос) в концентрированной соляной кислоте и активированном угле. Затем следует электролиз. 2 Одним из недостатков такого подхода является необходимость в огромных количествах концентрированной серной кислоты и воды. Кроме того, готовый продукт не является «кошерным» или «халяльным» и не подходит для веганской диеты.
Представлен более устойчивый процесс ферментации для производства веганского l-цистеина и l-цистина (димера l-цистеина).При этом используется сырье растительного происхождения, такое как кукуруза и неорганические микроэлементы. 2 Этот метод более устойчив по сравнению с химической экстракцией, в которой используется большое количество кислоты.
Питание
L-Цистеин — это полузаменимая аминокислота. Его много во многих продуктах, таких как говяжья печень, крабовые лепешки, бобы Лимы и некоторые грибы. Он также входит в состав многих пищевых добавок.
В качестве восстанавливающего агента он может помочь предотвратить избыточное производство свободных радикалов, вызванное физическими упражнениями.Это снижает окислительный стресс.
Функция
В тесте l-цистеин действует как восстановитель, который помогает расщеплять белки глютена. Этот эффект размягчения теста особенно важен для муки с высоким содержанием белка, из которой часто образуются плотные крошки и продукты с небольшим объемом. В системах быстрого приготовления хлеба l-цистеин имеет следующие преимущества: 3
- Компенсация за высокобелковую муку
- Более короткое время смешивания
- Пониженная температура теста
- Тесто менее напряженное
- Растяжимое тесто, более гибкое для деления и округления
- Меньший износ оборудования
- Улучшенный (панорамированный) поток
- Улучшенные допуски и меньшая жесткость во время расстойки
- Товары форменные
- Повышенная громкость из-за облегченного подъема
Преимущества размягчения теста
| Мука пшеничная | Замес | Формовочная | Расстойка и выпечка | Конечный продукт |
| Компенсирует слишком крепкую муку с высоким содержанием белка |
|
|
|
|
Приложение
Добавление восстановителей, таких как этот, в хлебобулочные изделия, необходимо для продуктов, изготовленных из муки с высоким содержанием муки.А также те, которые обрабатываются в одной чаше, например, хлебопечки. 4
Хлебобулочные изделия, содержащие сорго, могут выиграть от добавления l-цистеина для улучшения их вязкоупругих свойств, снижения твердости и улучшения их усвояемости.
При использовании большого количества этого ингредиента возможно развитие сернистого вкуса и аромата.
Положения
- L-Цистеин классифицирован FDA как GRAS в соответствии с разделом 184 раздела 21.1271. 5 Он также одобрен в Канаде, Австралии, Новой Зеландии и Европе как E920 (номер правила EFSA 1129/2011). 6
- Использование в пищевых продуктах разрешено в США и Канаде для содержания до 90 частей на миллион (0,009 частей на 100 частей муки), хотя на практике используется концентрация 20-30 частей на миллион.
- Кошерная маркировка l-цистеина разрешена только в том случае, если при его производстве используются надлежащие кошерные методы, в том числе без принесения в жертву животных.
Список литературы
- Ассоциация пекарей Канады.«L-CYSTEINE», http://www.baking.ca/Food%20and%20Nutrition%20Policy%20Revised/L-cysteine.pdf
- Hiroyuki, K., et al. «Процесс производства L-лизина путем ферментации». 15 июня 1995 ..
- Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. CFR — Свод федеральных правил, раздел 21. Accessdata.fda.gov, www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfcfr/cfrsearch.cfm?fr=184.1271.
- Stoica, A., Popescu, C., Barascu, E. и Lordan, M. Влияние L-цистеина на физические свойства хлеба из муки высокой экстракции с нормальным глютеном.Annals Food Sci. Технол., 2010, том 11, № 2, с. 6-10.
- БАКЕРпедия. «Ингредиенты для кондиционирования теста» | Ингредиенты для выпечки, bakerpedia.com/ingredients/dough-conditioner-ingredients/. ПОСТАНОВЛЕНИЕ КОМИССИИ
- (ЕС) № 1129/2011 от 11 ноября 2011 г. о внесении поправок в Приложение II к Регламенту (ЕС) № 1333/2008 Европейского парламента и Совета путем установления перечня пищевых добавок Союза.
Усиление тиоредоксин / глутаредоксин-опосредованного синтеза L-цистеина из S-сульфоцистеина увеличивает продукцию L-цистеина в Escherichia coli | Фабрики микробных клеток
Штаммы и плазмиды
The E.coli и плазмиды, использованные в этом исследовании, перечислены в таблице 1. Плазмида pDES (поставляемая Ajinomoto) для сверхпродукции L-цистеина, которая несет ген устойчивости к тетрациклину, является производным pACYC184, содержащим измененный ген cysE , кодирующий нечувствительный к ингибированию L-цистеин мутант SAT (Thr167Ala), дикий -типа ydeD, ген , кодирующий транспортер L-цистеина внутренней мембраны [7], и измененный ген serA , кодирующий нечувствительный к ингибированию L-серин мутант D-3-фосфоглицератдегидрогеназы (Thr410stop).Каждый фрагмент гена находится под контролем конститутивного промотора гена ompA E. coli , кодирующего предшественник белка А внешней мембраны. Измененный ген serA ориентирован в одном направлении, измененные гены cysE и ydeD находятся в противоположном направлении ориджина репликации, как описано ранее [9, 19].
Таблица 1 Использованные бактериальные штаммы и плазмидыДля получения гена cysI или cysJ была проведена полимеразная цепная реакция (ПЦР) с набором праймеров 5′-TTC GTC GCG GCC GC G AAA TCA TAA AAA ATT -3 ‘и 5’ — AAC AAT CCA GAT GAG TTC TGA -3 ‘(подчеркивание указывает положение Not I) с плазмидой pCysI или pCysJ в качестве матрицы, соответственно.Эти продукты ПЦР расщепляли Not I и затем клонировали в pCysK или pCysI с получением pCysK-I, pCysK-J или pCysI-J. Кроме того, ген nrdH был также амплифицирован с использованием набора праймеров 5′-CGT CTT CAC CTG CGA GAA ATC ATA AAA AAT T -3 ‘и 5′-TAT CAA CTC GAG TCC AAG CTC AGC TAA TTA -3’ (подчеркивание указывает положение Xho I) с плазмидой pNrdH в качестве матрицы. Продукт ПЦР расщепляли Xho I, а затем лигировали с плазмидой pCysK-I для конструирования pCysK-I-NrdH.
Среда и культивирование
Если не указано иное, бульон Леннокса (L) [1% бакто-триптона (Difco Laboratories, Детройт, Мичиган), 0,5% экстракта бакто-дрожжей (Difco) и 0,5% NaCl], Luria-Bertani ( LB) среды (1% бакто-триптона, 0,5% экстракта бакто-дрожжей и 1% NaCl) и минимальной среды SM1 (100 мМ калий-фосфатный буфер [pH 7,0], 150 мМ NH 4 Cl, 1,7 мМ NaCl, 1,0 мМ MgCl, 0,1 мМ CaCl 2 , 7,2 мкМ FeSO 4 , 3,4 мМ тринатрийцитрат, 0,6 мкМ Na 2 MoO 4 , 40.4 мкМ H 3 BO 3 , 2,9 мкМ CoCl 2 , 1 мкМ CuSO 4 , 8,1 мкМ MnCl 2 , 1 мкМ ZnSO 4 и 3,0% глюкозы (вес / объем) как источник углерода). При необходимости добавляли хлорамфеникол (Cm; 30 мкг / мл), канамицин (Km; 50 мкг / мл) и / или тетрациклин (Tet; 10 мкг / мл). Для твердых сред добавляли 1,5% (мас. / Об.) Агара. Где указано, в SM1 добавляли бульон L (конечные 10%), 1-метионин и источники серы (сульфат: MgSO 4 или / и тиосульфат: Na 2 S 2 O 3 ).Культуры инкубировали в аэробных условиях при энергичном встряхивании при 30 ° C или 37 ° C. Рост контролировали путем измерения оптической плотности при 660 нм (OD 660 ).
В эксперименте по производству L-цистеина среду SM1 с 30 мМ тиосульфатом и 30 мМ сульфатом или только 30 мМ тиосульфатом использовали для продукции L-цистеина. Избыточные продуценты L-цистеина предварительно культивировали в LB (Tet + Cm) при 30 ° C в течение 20 часов и прекультуру вносили в 30 мл источника серы SM1 + (Tet + Cm) для установления OD 660 , равного 0.4 в каждой культуре. Культуру культивировали при 30 ° C в течение 24–48 ч. Изопропил-1-тио-β-d-галактопиранозид (IPTG; конечная концентрация 0,1 мМ) добавляли в среду после 6 часов культивирования для избыточного продуцирования целевых белков. PH доводили до 7,0, используя CaCO 3 . Рост измеряли по поглощению (OD 562 ) культурального бульона после соответствующего разбавления 0,1 н. HCl.
Экспрессия и очистка рекомбинантных белков
E. coli K-12 штамм AG1 [ recA1 endA1 gyrA96 thi-1 hsdR17 (r K — m K 16 90 sup217 K + 90 sup217 ) ] трансформировали каждой из различных плазмид на основе pCA24N, а затем трансформированные клетки выращивали при 30 ° C в 50 мл среды LB.Когда OD 660 достигала 0,6, в культуральную среду добавляли IPTG до конечной концентрации 0,1 мМ, чтобы вызвать экспрессию гена. После культивирования в течение 3 ч при 30 ° C клетки собирали, суспендировали в 5 мл ледяного буфера А (40 мМ имидазол, 0,5 М NaCl, 20 мМ фосфат натрия) и разрушали с помощью звуковых колебаний при охлаждении. После центрифугирования (20 мин при 18000 × г ) растворимую фракцию супернатанта очищали с использованием колонки с никелевой сефарозой His Trap HP (GE Healthcare, Пискатауэй, Нью-Джерси) по процедуре, рекомендованной поставщиком.Слитые белки, меченные His, наносили на колонку, уравновешенную тем же буфером, содержащим 10 мМ имидазол. Колонку промывали 80 мМ имидазолом в том же буфере, и белки элюировали 0,5 М имидазолом, 0,5 М NaCl и 20 мМ фосфатом натрия в том же буфере. Концентрации белка определяли с использованием набора для анализа белков Bio-Rad (Hercules, CA) с бычьим сывороточным альбумином в качестве стандартного белка.
Ферментный анализ
Активность Trx и Grx определяли по методикам, описанным в [14, 15].Trxs (Trx1-2) и Grx-подобные белки (Grx4 и NrdH) восстанавливаются Trx-редуктазой после восстановления субстратов. Grx (Grx1-3) также восстанавливаются глутатионом и глутатионредуктазой. Поэтому мы отдельно измерили активность Trxs и Grxs, отслеживая снижение поглощения НАДФН при 340 нм. Реакционная смесь для анализа Grx содержала следующее в конечном объеме 0,5 мл; 0,5 мМ GSH, 0,16 мМ НАДФН, 0,1 мг / мл БСА, 5,9 мкг / мл глутатионредуктазы (Sigma-Aldrich, St.Louis, MO) в 0,1 М трис-HCl (pH 8,0). К реакционной смеси добавляют дисульфидный субстрат, 50 мкМ S -сульфоцистеин (Sigma-Aldrich), что приводит к образованию смешанного дисульфида между GSH и S -сульфоцистеином в течение 1 мин. После добавления рекомбинантного Grx к реакционной смеси в течение пяти минут измеряли уменьшение НАДФН.
Реакционная смесь для анализа Trx содержала следующее в конечном объеме 0,5 мл; 0,32 мМ НАДФН, 20 мМ S -сульфоцистеин, 0.2 мкМ тиоредоксинредуктазы в 0,1 М фосфате калия / 2 мМ ЭДТА (pH 7,0). К реакционной смеси добавляли рекомбинантный Trx, чтобы начать восстановление S -сульфоцистеина.
Определение содержания L-цистеина
Количество L-цистеина в культуральных супернатантах определяли по методике Gaitonde [20]. Перед добавлением реагента Гайтонда (250 мг нингидрина, растворенного в смеси 4 мл HCl и 16 мл уксусной кислоты), L-цистин в образцах восстанавливали путем инкубации с 5 мМ дитиотреитола в 100 мМ трис-HCl буфере (pH 8 .6) на 10 мин. Продукты реакции разбавляли 99,5% (об. / Об.) Этанолом перед измерением оптической плотности при 560 нм.
N-ацетил-L-цистеин | CAS 616-91-1 | SCBT
N-ацетил-L-цистеин (CAS 616-91-1) Цитаты на продукцию
Посмотрите, как другие использовали N-ацетил-L-цистеин (CAS 616-91-1).Щелкните запись, чтобы просмотреть запись в PubMed. .
Цитирования с 1 на 10 из 28 всегоPMID: # 33544321 Караман, Э. | Эркин, Ö. | Гёль, И. | et al. 2021. J Relig Health.
PMID: # 33542321 Шарма, С.| Гуфран, С.М. | Гхош, С. | Бисвас, С. | et al. 2021. Sci Rep. 11: 3089.
PMID: # 33325610 Hsu, YK. | Chen, HY. | Wu, CC. | Huang, YC. | Hsieh, CP. | Su, PF. | Huang, YF. | et al. 2020. Environ Toxicol.
PMID: # 31273592 Wang, J. | Wu, D. | Zhang, J. | Liu, H. | Wu, J. | Dong, W. | et al. 2019. Коп. Дис. Sci.
PMID: # 30929137 Acar, T. | Kaya, E. | Yoruk, MD. | Duzenli, N. | Senturk, RS. | Can, C. | Ozturk, L. | Tomruk, C. | Uyanikgil, Y. | Rybicki , FJ. | et al. 2019. Jpn J Radiol. 37: 458-465.
PMID: # 31641109 Рашид, С. | Фрейтас, Миссури | Кукки, Д. | Бридж, Г.| Яо, З. | Гей, Л. | Уильямс, М. | Ван, Дж. | Суравира, Н. | Сильвер, А. | Макдональд, САК. | Челала, К. | Сабадкай, Г. | Мартин, С.А. | et al. 2019. Cell Death Dis. 10: 795.
PMID: # 29960166 Seervi, M. | Rani, A. | Sharma, AK. | Santhosh Kumar, TR. | et al. 2018. Biomed. Фармакотер. 106: 200-209.
PMID: # 28529590 Zhu, Q.| Го, Б. | Чен, Л. | Цзи, К. | Лян, Х. | Вэнь, Н. | Чжан, Л. | et al. 2017. Oncol Lett. 13: 3760-3766.
Цитирования с 1 на 10 из 28 всегоНовое приложение для создания электрохемилюминесцентных изображений на основе полидофаминовых наночастиц с регулируемым l-цистеином
В этой работе были синтезированы новые регулируемые цистеином L наночастицы полидофамина (НЧ PDAcp) с превосходными электрохемилюминесцентными (ECL) характеристиками.Из-за сложной полимеризации дофамина и возникающей в результате неупорядоченной внутренней структуры наночастицы полидофамина (НЧ PDA) страдали от низкой светоотдачи и плохих оптических характеристик. Поэтому мы использовали L -цистеин, чтобы уменьшить путаницу в процессе полимеризации и внутренней структуре, чтобы эффективно улучшить световые свойства НЧ КПК. С одной стороны, тиольная функциональная группа L -цистеина может реагировать с олигомером дофамина и подвергаться реакции присоединения Михаэля.С другой стороны, аминогруппа цистеина L образует основание Шиффа с карбонильной группой олигомера посредством нуклеофильного присоединения. Поверхность полученных наночастиц была дополнительно модифицирована полиэтиленимином (PEI). Приготовленные НЧ PDAcp имели в 10 раз большую интенсивность ECL, чем НЧ PDA. Для обнаружения аденозинтрифосфата (АТФ) было проведено исследование аптасенсинга ECL на основе эффекта внутреннего фильтра и анализ изображений. Результаты показали, что предлагаемый сенсор аптамера может определять АТФ с пределом обнаружения 3.79 фмоль л -1 и линейный диапазон от 10 фмоль л -1 до 100 мкмоль л -1 . ECL-изображения NP PDAcp были четко записаны с помощью смартфона. Результаты визуального анализа ECL показали, что НЧ PDAcp имеют большой потенциал для биочувствительности ECL и клинической диагностики.
У вас есть доступ к этой статье
Подождите, пока мы загрузим ваш контент… Что-то пошло не так. Попробуйте снова? .