Крахмальный клейстер формула – Урок №48. Крахмал, его строение, химические свойства, применение.
Крахмальный клейстер — Справочник химика 21
Крахмал предварительно подвергают осахариванию , т. е. превращению в более простое сахаристое вещество. Для этого картофель или зерно запаривают перегретым паром (при 140— 150° С) в результате получают массу, содержащую крахмальный клейстер. В эту массу, после того как она остынет, вводят солод (проросшие и измельченные зерна ячменя). Под каталитическим действием содержащегося в солоде фермента амилазы крахмал гидролизуется, распадаясь с образованием сахара мальтозы (стр. 251), [c.116]В холодной воде крахмал нерастворим, в горячей зерна его набухают и образуют густую жидкость — крахмальный клейстер. Гидролизуя крахмал, получают растворимый крахмал, декстрин, патоку и глюкоз-у. [c.173]
Опыт 3. Горение натрия в воздухе (в вытяжном шкафу ). На крышку тигля положить маленький кусок натрия, расплавить его, нагревая крышку снизу, затем поджечь металл пламенем горелки и сразу опустить дверцу вытяжного шкафа. Когда весь металл сгорит, охладить полученное вещество и растворить его в фарфоровой чашке в 2—3 мл воды (осторожно, может остаться несгоревший металл ). К полученному раствору добавить несколько капель раствора иодида калия, подкисленного разбавленной серной кислотой, и 1—2 капли крахмального клейстера перемешать жидкость стеклянной палочкой. Объяснить наблюдаемые явления. Какие вещества образуются при горении на воздухе натрия
Крахмал (СбНю05)х — белый (под микроскопом зернистый) порошок, нерастворимый в холодной воде в горячей — набухает, образуя коллоидный раствор крахмальный клейстер) с раствором иода дает синее окрашивание (характерная реакция). Молекулы крахмала неоднородны по величине — значение х в них колеблется от сотен до 1000—5000 и более. [c.494]
Крахмал, макромолекула которого состоит из звеньев глюкозы, представляет собой не индивидуальное вещество, а смесь полисахаридов, отличающихся не только размером макромолекул, но и строением. Крахмал является одним из важнейших продуктов фотосинтеза, образующихся в зеленых частях растений, и составляет основную часть питательного вещества хлеба, картофеля и различных круп. В воде при определенной температуре крахмал набухает и клейсте-ризуется, образуя внешне однородную густую жидкость — крахмальный клейстер, который широко применяют в технике в качестве клея, для шлихтования и отделки тканей, для проклеивания бумаги и т, д. Путем гидролиза из крахмала получают декстрин, патоку и глюкозу, [c.418]
К полученному раствору прилейте подкисленный серной кислотой раствор иодида калия и 2—3 капли крахмального клейстера. На основании результатов последнего опыта сделайте заключение о характере продуктов сгорания натрия (калия). [c.106]
Растворы воды известковой аммиачного раствора оксида серебра глюкозы с массовой долей 5 % фелинговой жидкости лактозы, сахарозы с массовой долей 1 % крахмального клейстера серной кислоты ( оч = 98 и 30 %) кислоты соляной, едкого натра эквивалентной концентрации — 2 мопь/л медно-аммиачного раствора (реактив Швейцера).
Крахмальный клейстер применяется для склеивания бум.аги. Клейстер обычной консистенции готовят из 10 в с. ч. крахмала и 100 вес. ч. воды. При этом крахмал сперва вмешивают в небольшом количестве холодной воды, а затем эту взвесь понемногу, при тщательном перемешивании вливают в кипящую воду. Чтобы клейстер долгое время оставался пригодным, добавляют в горячую жидкость I вес. ч. порошкообразных квасцов или буры». [c.1048]
Крахмальный клейстер. 2 г растворимого крахмала смешивают с 10 мл холодной воды и вливают эту кашицу в 100 мл кипящей воды. Кипятят 5—10 мин, охлаждают, дают отстояться и, если образуется хлопьевидный осадок, сливают с него раствор (или фильтруют). Для стабилизации добавляют 0,1 г гидроксида калия или салициловой кислоты (можно также 0,01 г иодида ртути). [c.191]
Если между молекулами полимера нет прочных связей, то его набухание продолжается вплоть до заполнения им всего объема взятого растворителя, т. е. до образования гомогенной системы. При достаточно большом количестве растворителя молекулы полимера окончательно разобщаются друг от друга и система приобретает текучесть — образуется жидкий раствор. Такое набухание называется неограниченным. Примером неограниченного набухания полимеров может быть растворение каучуков в углеводородах, белков в воде и т. п- На этом основано приготовление резиновых клеев, крахмального клейстера и т. п. [c.296]
Приборы и реактивы. Секундомер. Термостат (три стакана вместимостью 200— 250 мл) и крышка к нему с отверстиями для пробирок. Мензурка вместимостью 10 мл. Термометр на 50 °С. Стеклянные палочки. Пипетки капельные. Фильтровальная бумага. Шпатель. Ступка с пестиком. Сульфит натрия (кристаллический). Диоксид марганца. Карбонат кальция (мел). Нитрат ртути (И). Иодид калия. Хлорид калия. Нитрат свинца. Растворы иодата натрия (0,02 н), тиосульфата натрия (1 и., 0,5 н.), серной кислоты (2 н.), хлороводородной кислоты (плотность 1,19 г/см ), крахмального клейстера, хлорида железа (HI) (0,0025 н.,
Пероксид натрия и его свойства. 1. У лаборанта возьмите небольшое количество пероксида натрия (микрошпатель) и порциями внесите его в пробирку с 2—3 мл холодной дистиллированной воды. Полученный раствор разделите на три части. Одну часть нагрейте, тлеющей лучинкой обнаружьте выделение кислорода и определите pH раствора, ко второй — прилейте подкисленный раствор иодида калия и добавьте 1—2 капли крахмального клейстера, к третьей — по каплям прибавьте подкисленный раствор перманганата калия. Что наблюдается Напишите уравнения реакций. [c.265]
Приборы и реактивы. Асбестовая сетка. Тигель. Пинцет. Ланцет или нож. Паяльная трубка. Молоток. Цилиндр (высота 10—15 см). Чугунная или железная плита. Капиллярная пипетка. Кусок угля (не меньше 5X5 см). Оксид свинца (11). Цинк (гранулированный). Свинец. Диоксид свинца. Сурик. Припой Иодокрахмальная бумага. Крахмальный клейстер. Растворы сероводородной воды, хлороводородной кислоты (4 н., 2 н., плотность 1,19 г/см ), азотной кислоты (2 н., плотность 1,4 г/см ), серной кислоты (2 н., плотность 1,84 г/см ), едкого натра (2 и., 40%-ный), нитрата или ацетата свинца (0,5 н.), иодида калня (0,1 н.), пероксида водорода (3%-ный), карбоната натрия (0,5 и.), сульфата натрия (0,5 н.), сульфата марганца (0,5 н.), сульфата хрома (0,5 н.). [c.175]
Окислительные свойства производных меди (И). В пробирку налейте 0,5—1 мл раствора сульфата меди (II) и добавьте 0,5 мл раствора иодида калия. Наблюдайте выделение осадка и побурение смеси. Убедитесь, что побурение вызвано выделившимся иодом. Для этого отлейте часть смеси, разбавьте водой и добавьте 1—2 капли крахмального клейстера.
Вызвать рвоту. Дать 1%-ный раствор тиосульфата натрия, крахмальный клейстер, молоко [c.16]
Дать воды. Вызвать рвоту. Дать мо
www.chem21.info
Крахмальный клейстер — PharmSpravka
Как известно, нативный крахмал состоит из зерен. Крахмальные зерна представляют собой сферокристаллы — сферические скопления тончайших игольчатых кристаллов, ветвящихся из центра наружу. С этой особенностью строения крахмальных зерен связаны их пористость, гигроскопичность и способность впитывать различные жидкости. В воде на холоде крахмал нерастворим и лишь слегка набухает, поглощая 35-40% воды. Подсчет показывает, что каждая гидроксильная группа крахмала связывает при набухании одну молекулу воды. В горячей воде (50-60 °С) набухание крахмала резко усиливается. Степень набухания зависит от температуры и при 80 °С достигает 25-30% первоначального объема, причем образуется эластичный студень, а небольшая часть крахмала переходит в раствор. Это явление называется клейстеризацией. Температура клейстеризации у различных крахмалов лежит в интервале 62-72 °С. В начальных стадиях клейстеризации крахмальные зерна остаются нерастворимыми. Они разрушаются лишь при температуре выше 80 °С.
По химическому составу крахмал представляет собой неоднородное вещество. Он является смесью нескольких полисахаридов. В нем содержится 10-20% амилозы, состоящей из жестких цепеобразных макромолекул (молекулярный вес 10 000-60 000) и растворимой в горячей воде. Основная часть крахмала — амилопектин (молекулярный вес свыше 1000 000) состоит из сильно разветвленных макромолекул. В горячей воде амилопектин не растворяется, но сильно набухает, образуя очень вязкие, слизистые опалесцирующие механически непрочные студни.
Растворы амилозы очень неустойчивы и вскоре выделяют нерастворимый осадок. Это явление называется ретроградацией. Причиной ретроградации растворов амилозы является образование поперечных «сшивающих» связей между молекулами амилозы, что приводит к укреплению макромолекул и «кристаллизации» амилозы. При изготовлении клейстера из природного крахмала амилопектин препятствует ретроградации амилозы.
При неосторожной обработке горячей водой крахмал чрезвычайно легко подвергается комкованию, которое, как правило, приводит к необходимости приготовления клейстера заново. Крахмальный клейстер является питательной средой для микроорганизмов, быстро подвергается брожжению, прокисает и плесневеет. Стандартный крахмальный клейстер содержит 2% крахмала и носит название Mucilago s. Decoctum Amyli.
№ 69. Rp.: Chlorali hydrati 5,0
Mucilaginis Amyli 200 мл
MDS. 1 столовую ложку на ночь
Под названием Amylum фармакопея (ГФХ) подразумевает различные виды крахмала: пшеничный, картофельный, маисовый. По свойствам клейстера крахмалы неравноценны. Для медицинских целей наиболее целесообразно использовать клейстер из пшеничного крахмала.
4 г пшеничного крахмала растирают в небольшой ступке или фарфоровой чашке с 16 мл холодной воды (1:4). Полученную суспензию вливают в 180 мл (1:45) кипящей воды в кастрюле или колбе. Смесь нагревают до кипения и оставляют для охлаждения. Кипятить жидкость более продолжительное время не следует во избежание гидролиза крахмала. Для приготовления клейстера из картофельного крахмала необходимо 1-2-минутное кипячение. В противном случае значительное количество крахмальных зерен остается неразрушенным и быстро выделяется в осадок. Полуостывший клейстер переносят в подставку и доводят водой до 200 мл. В совершенно остывшей жидкости растворяют хлоралгидрат и микстуру процеживают в отпускную склянку сквозь марлю.
При растворении хлоралгидрата нужно иметь в виду, что он летуч при нагревании. Кроме того, горячая вода вызывает разрушение хлоралгидрата, сопровождаемое отщеплением хлористого водорода. Растворение хлоралгидрата должно производиться только в холодных растворителях. Растворы хлоралгидрата светочувствительны и должны отпускаться в склянках оранжевого стекла.
28.06.2015
www.pharmspravka.ru
Клейстер крахмальный, приготовление — Справочник химика 21
В пробирку налить немного разбавленного крахмального клейстера и прилить несколько капель приготовленного раствора иода в иодистом калии (или иодистом натрии) Что происходит [c.188]Приготовление крахмального клейстера. Крахмальный клейстер, как известно, служит наиболее распространенным реактивом на свободный иод. Для работы готовят очень разбавленный коллоидный раствор крахмала/ в воде, носящий название крахмального клейстера. [c.60]
Для приготовления крахмального клейстера растирают 1 г крахмала с 3—5 мл воды и вливают в 100 мл кипящей воды. [c.227]
Если между молекулами полимера нет прочных связей, то его набухание продолжается вплоть до заполнения им всего объема взятого растворителя, т. е. до образования гомогенной системы. При достаточно большом количестве растворителя молекулы полимера окончательно разобщаются друг от друга и система приобретает текучесть — образуется жидкий раствор. Такое набухание называется неограниченным. Примером неограниченного набухания полимеров может быть растворение каучуков в углеводородах, белков в воде и т. п- На этом основано приготовление резиновых клеев, крахмального клейстера и т. п. [c.296]
Поместите в пробирку 5 капель 0,5%-ного крахмального клейстера (33). Добавьте в нее такой же объем собственной слюны и тщательно размешайте. Через 1—2 мин возьмите пипеткой 1 каплю раствора и нанесите на предметное стекло. Добавьте 1 каплю очень разведенного раствора иода в иодиде калия (приготовление см. оп. 83). Отсутствие синей окраски укажет на то, что крахмал переварен слюной. Для контроля можно добавить вновь 1 каплю крахмального клейстера (33) — синяя окраска появится моментально. [c.90]
Назначение. Предназначена для выполнения следующих технологических процессов взвешивания исходною материала, приготовления крахмального клейстера, смешения исходной массы с крахмальным клейстером, влажного гранулирования, сушки, опудривания и транспортировки к роторным таблеточным машинам. [c.277]
Аппарат для заварки клейстера состоит из заварочной камеры и камеры приготовления крахмальной суспензии, дозатора крахмала 11, емкости горячей воды 13 и насоса-дозатора 14 для подачи крахмальной суспензии в смеситель. Заварочная камера включена в рубашку обогрева. Сквозь заварочную камеру и камеру приготовления крахмальной суспензии проходит вал. В зоне приготовления крахмальной суспензии на валу закреплена турбинка мешалки, стенки камеры имеют ребра, препятствующие образованию воронки. Камера имеет устройство для поддержания постоянного уровня суспензии, которым автоматически регулируется соотношение выдаваемого и остающегося в камере клейстера. [c.278]
В том случае, если в рецептуру крема вводят крахмал, то процесс дополняется операцией приготовления крахмального клейстера. [c.170]
Первая стадия работы — приготовление крахмального клейстера. Его помещают в круглодонную колбу, добавляют небольшое количество серной кислоты, закрывают пробкой с обратным воздушным холодильником и кипятят. Через 30 мин. после на- чала кипения отбирают пробу — 1 мл, охлаждают ее и добавляют каплю раствора йода. Такие пробы делают затем каждые 10 мин. до отрицательной реакции на крахмал. Отсутствие синей окраски с йодом говорит о том, что гидролиз закончен. [c.118]
Для приготовления иодкрахмальной бумажки применяют свежий крахмальный клейстер (см. опыт 137) его разбавляют в 4—5 раз кипящей водой, охлаждают и растворяют в этой жидкости иодистый калий (0,1—0,2 г на каждые 100 мл). Полученным раствором пропитывают фильтровальную бумагу, сушат ее и нарезают полосками, которые хранят в плотно закрытой банке. [c.269]
Хлорирование оксидов бериллия четыреххлористым углеродом было осуществлено в промышленном масштабе в Советском Союзе [29 30, с. 507]. Оксид бериллия брикетировали в шнековом прессе, используя в качестве связующего для приготовления массы 1— 3%-ный раствор крахмального клейстера или декстрина. Полученные брикеты диаметром 10 мм и длиной 40 мм сушили при 200 °С, а затем коксовали при 600 °С. Кажущаяся пористость брикетов составляла 50—60%. [c.75]
Крахмальный клейстер. Размешивают 2 г крахмала с небольшим количеством БОДЫ и смесь вливают при непрерывном перемешивании в 1 л кипящей воды. Кипятят несколько минут и фильтруют, собирая фильтрат в склянки емкостью 125 мл, снабженные притертыми пробками. Полученный раствор стерилизуют паром в стерилизаторе и заливают пробки склянок парафином. На 100 мл титруемого раствора вводят 5 мл приготовленного раствора крахмала. [c.567]
В ступке тщательно растирают 2 г крахмала, перемешивают с 10 мл дистиллированной воды до получения однородной кашицы и медленно вливают в 500 мл кипящей воды. Кипячение продолжают 1—2 мин. Раствор охлаждают и прибавляют 2 г иодида калия. Фильтровальную бумагу смачивают приготовленным раствором иодида калия в крахмальном клейстере н сушат в помещении, защищенном от действия газов, пыли и солнечных лучей. Высушенную бумагу хранят в банке из темного стекла с притертой пробкой. [c.261]
Вводные пояснения. Высокую эффективность бордоская жидкость как фунгицид широкого спектра действия достигает только при условии правильного ее приготовления и немедленного использования. Даже при непродолжительном стоянии частицы суспензии соединяются и быстро оседают на дно сосуда. Для полного или хотя бы частичного устранения такого явления к суспензии прибавляют патоку, сахар, крахмальный клейстер и другие вещества. [c.49]
Иодокрахмальная бумага представляет собой фильтровальную бумагу, пропитанную смесью растворов иодистого калия и крахмального клейстера, а затем высушенную. Приготовление иодокрахмальной бумаги см. на стр. 202. [c.191]
Гидролиз крахмала. В круглодонную колбу на 500 мл (см. рис. 44) налить 100 мл воды и 2 концентрированной серной кислоты. Нагреть раствор кислоты до кипения и к нему постепенно прилить заранее приготовленную холодную смесь, содержащую 25 г крахмала и 25 мл воды. Круглодонную колбу с образовавшимся в ней крахмальным клейстером закрыть пробкой с обратным воздушным холодильником и кипятить смесь около часа гидролиз можно считать законченным, когда проба жидкости из колбы не будет давать окраски с йодной водой. [c.197]
Поскольку избыток угля не мешает бромированию, уголь обычно берут в некотором избытке. Для приготовления исходной смеси окислы и уголь, взятый в небольшом избытке против теоретически необходимого количества, перетирают в ступке, заливают густым крахмальным клейстером, перемешивают и густую пасту помещают т
www.chem21.info
Формула крахмала в химии
Определение и формула крахмала
Химическая формула крахмала: (C6H10O5)n
Молярная масса: г/моль
Структурная формула крахмала
Крахмал содержит 10–20 % амилозы (внутренняя часть крахмального зерна) и 80–90% амилопектина (оболочка крахмального зерна). Оба полимера состоят из звеньев — глюкозы и имеют состав (C6H10O5)n.
Амилоза
Амилоза имеет неразветвленную структуру, обычно включающую 200–1000 звеньев (n = 200–1000). При образовании молекулы амилозы остатки глюкозы соединяются между собой аксиальными (14)-гликозидными связями:
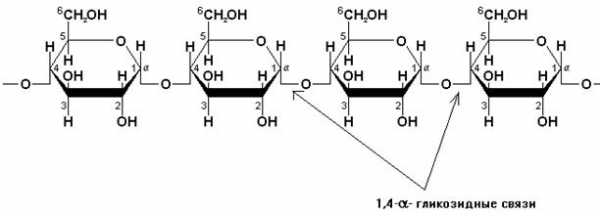
Звенья -глюкозы закручивают макромолекулу амилозы в спираль, на каждый виток которой приходится 6 остатков глюкозы:
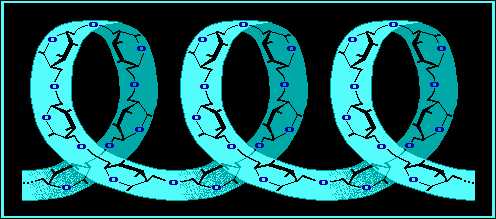
Такая структура вероятность возникновения межмолекулярных водородных связей, но увеличивает вероятность возникновения таких связей с молекулами воды. Поэтому амилоза способна растворяться в воде.
Амилопектин
Амилопектин имеет разветвленную структуру, n = 6000–40000. Полимерная цепь амилопектина также образуется за счет (14)-гликозидных связей. Разветвление цепи происходит путем образования -гликозидных связей и наблюдается через 20–25 остатков глюкозы.
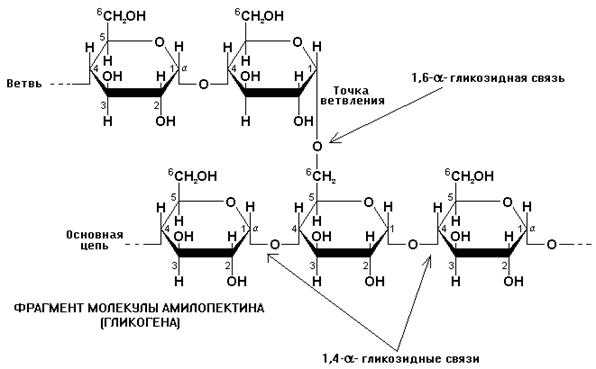
Амилопектин не растворяется в воде, а только набухает с образованием коллоидного раствора. Гликоген (животный крахмал) построен подобно амилопектину, только его макромолекулы которого отличаются еще большей разветвлённостью.
При нормальных условиях крахмал – белый безвкусный порошок, в холодной воде не растворяется, в горячей – набухает с образованием коллоидного раствора (крахмального клейстера). При растирании издает характерный скрип.
Кислотный гидролиз крахмала проходит ступенчато. Сначала крахмал превращается в полимеры с меньшей степенью полимеризации – декстрины, потом в дисахарид (мальтозу), и в конечном итоге – в глюкозу:
Суммарная реакция:
Качественная реакция на крахмал – взаимодействие с раствором йода (I2), образуется комплексное соединение включения (клатрат) синего цвета. При нагревании раствора окраска исчезает.
Примеры решения задач
ru.solverbook.com
Крахмал, свойства и все характеристики
Характеристики и физические свойства крахмала
Его молекулы состоят из линейный и разветвленных цепей, содержащих остатки α-глюкозы. Фрагмент структуры крахмала выглядит следующим образом:
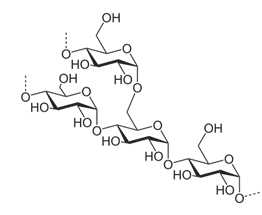
Крахмал является природным высокомолекулярным соединением и представляет собой смесь двух полисахаридов: амилозы и амилопектина. Число повторяющихся звеньев в различных молекулах амилозы и амилопектина варьируется от нескольких сотен до нескольких тысяч. Поэтому говорят только о средней молекулярной массе крахмала.
В горячей воде крахмальные зерна набухают и образуют коллоидный раствор, называемый крахмальным клейстером. Крахмал не обладает сладким вкусом.
Получение крахмала
В промышленности крахмал получают из картофеля (содержание крахмала – до 24%) или зерен кукурузы (57 – 72%).
Химические свойства крахмала
Крахмал способен гидролизоваться при нагревании в кислой среде, причем конечным продуктом гидролиза является глюкоза:
(С6Н10О5)n + nН2О → nC6H12O6.
Крахмал дает интенсивное синее окрашивание с йодом — это качественная реакция на йод.
Крахмал может образовывать эфиры за счет гидроксильных групп, однако они не имеют практического значения.
Применение крахмала
Крахмал – важнейшее пищевое вещество для человека и животных. В составе картофеля и зерновых культур (на крахмал приходится до 75% массы пшеничной муки) он потребляется в огромных количествах.
Примеры решения задач
| Понравился сайт? Расскажи друзьям! | |||
ru.solverbook.com
Крахмальный клейстер — МегаЛекции
Готовится из лучшего пшеничного крахмала, которого берут нужное количество и разводят в фаянсовой миске в небольшом количестве воды так, чтобы образовалась не очень густая кашица, причём раздавливают образовавшиеся комки и размешивают как можно лучше. Затем заваривают эту массу кипятком, подливая его понемногу, не переставая перемешивать, пока она не получится нужной степени густоты. После этого, помешав ещё некоторое время, остужают, пропускают его через плотное полотно и после используют. Его следует употреблять перед мучным.
Мучной клейстер.
Замесив в кастрюле густое тесто из чистой пшеничной муки в небольшом количестве воды, постоянно перемешивая, дать остыть.
Клейстер из картофельной муки не годится, т.к. имеет незначительную связующую силу и бывает вообще слишком водянистым.
Лабораторная работа № 8
Определение реакции среды (рН) клея.
Реакция среды клея определяется потенциометрическим методом, базирующимся на изменении цвета некоторых органических веществ (индикаторов). Каждый индикатор характеризуется определённым интервалом рН, при которых происходит изменение цвета. Индикаторы могут быть разными: в виде карандаша, буферных растворов или индикаторной бумаги.
Определение реакции среды (рН) клея индикаторной бумагой.
Определение (рН) клея в сравнении цвета индикаторной бумаги, смоченной клеем со шкалой, содержащей стандартные цвета.
Цель работы: Освоить один из методов определения среды (рН) клея.
Приборы и материалы: Универсальная индикаторная бумага ((рН) 1-12), дистиллированная вода, клей.
Методика и порядок выполнения работы:Рабочий раствор клея, разбавленный дистиллированной водой в соотношении 1:5 (клей : вода соответственно). В разведённый клей погружают индикаторную бумагу, сравнивая с контрольной средой. За результатом изменения рН клея принимается среднее значение 3х измерений. Результат исследования вносят в таблицу.
| № | Название клея | рН клея | Среднее арифметическое | ||
| Клей мучной | 5,5 | 5,5 | 5,5 | ||
| Клей крахмальный | 5,5 | ||||
| Клей КМЦ | 6,5 | 6,5 | 6,5 | 6,5 | |
| Клей ПВА | 7,5 | 7,5 | 7,5 | 7,5 |
Вывод: В этой работе мы научились определять рН клея с помощью индикаторной бумаги. Мы определили, что клей мучной (5,5 рН) имеет слабо кислую среду, так же, как и крахмальный (6) и КМЦ (6,5), а вот клей ПВА (7,5 рН) имеет щелочную среду.
Лабораторная работа № 9
«Взаимодействие бумаги с жидкостями»
В процессе полиграфической технологии бумага вступает в контакт с жидкими материалами, которые входят в состав печатных красок, клеев, лаков, и др. При использовании полиграфической продукции – воздействие разных жидкостей, воды. Особые требования к влагостойкости бумаги выдвигается при изготовлении офсетной, картографической, форзацной, обложечной, этикетной бумаги.
Особые свойства бумаги – свойства вбирать краску.
Правильный выбор бумаги с оценкой впитывания краски означает выполнение условий своевременного и полнейшего закрепления краски и получения качественного отражения.
Способность бумаги вбирать краску зависит от капиллярных свойств бумаги. Макропористые (или пористые) состоят целиком из древесной массы (газетная).
В этом случае может иметь место ещё один дефект печатания – осыпание.
Причиной этого является то, что пигмент остаётся на поверхности бумаги без достаточного количества вяжущего для образования плёнки.
В целлюлозные микропористые сорта бумаги краска почти не проникает в середину бумаги, что может послужить причиной появления чернильных пятен.
| Макропористые газетные | Микропористые немелованные | Микропористые мелованные |
| Пористость – 60% Радиус пор – 0,16 мм Плотность – 0,5 г/см2 100% древесной массы | 100% целлюлозы | Пористость – 30 % Радиус пор – 0,16 мм Плотность – 0,5 г/см2 100% целлюлозы |
Впитывающая способность бумаги по отношению к краскам определяют измерением поверхностного впитывания капельным способом. Метод состоит в определении времени, необходимого для впитывания капли воды или органического растворителя при температуре 20,0 +/- 1,0 градусов, нанесённой на поверхность бумаги. Например, впитывающая способность бумаги для глубокой печати, осуществляется 0,5% раствором гудрона в кислоте; этикеточной бумаги – 10% раствором камфоры в кислоте и т.д.
Лабораторная работа № 10
Бумага для реставрационных работ
Бумага является основным материалом для реставрационных работ. Правильный подбор её в большой мере обеспечивает успех реставрации в целом. Поэтому реставраторы должны иметь в своём распоряжении самые разнообразные виды бумаги, отличающиеся между собой цветом, толщиной, фактурой, способностью к деформации и др. Применяемые для реставрации виды бумаги в большинстве своём изготовляются промышленностью, а часть из них – полуфабрикаты, которые идут на получение той или иной продукции и поэтому носят название «основа».
Все иные используемые для реставрационных работ виды бумаги были проверены в своё время на долговечность и взаимодействие с клеем и документом.
Применяемая для реставрационных работ бумага должна иметь рН близкий к нейтральной, а именно от 8,0 до 6,0. Для реставрации пригодны виды бумаги с небольшими изменениями показателя рН в процессе термического старения. Изменение его в значительной мере зависит от типа исходного волокнистого материала и наличия канифольной проклейки, некоторые наполнители (мел) в протекающих процессах играют существенную роль. Проклейка канифольным клеем сдвигает показатель рН в кислую область, что связано с присутствием в проклеивающих веществах кислых продуктов. Наличие наполнителя, если это мел, нейтрализует кислые вещества, занесённые проклейкой, а также кислые продукты, образующиеся в результате деструкции самой целлюлозы. Для реставрационных работ следует применять бумагу, изготовленную из хлопковых и льняных волокон или из волокон сульфатной целлюлозы, как наиболее стойких к процессам старения. Менее стойкой является сульфитная целлюлоза. Бумагу, содержащую древесную массу, для целей реставрации применять не рекомендуется.
В практике реставрационных работ зачастую важно определить направление бумаги, что связано с изменением её свойств, а именно деформацией и различием механических свойств по направлениям. Направление в бумаге является результатом формирования бумажного листа на сетке бумагоделательной машины: вдоль движения сетки называется долевым направлением, а поперёк –поперечным.
Бумага ручного отлива не имеет направления. При проведении реставрационных работ применяется бумага не только как основной материал, но и для вспомогательных операций: просушки и прокладки документов, прессования и других целей.
Рекомендуемые страницы:
Воспользуйтесь поиском по сайту:
megalektsii.ru
Крахмал с йодом. Реакция невидимости
Описание:
Одно из свойств крахмала – это способность давать синюю окраску при взаимодействии с йодом. Эту окраску легко наблюдать, если поместить каплю раствора йода на срез картофеля или ломтик белого хлеба. Крахмал в качестве резервного питания накапливается в клубнях, плодах, семенах растений. Так, в клубнях картофеля содержится до 24 % крахмала, в зёрнах пшеницы — до 64 %, риса — 75 %, кукурузы — 70 %.
С помощью йода можно открыть самые незначительные количества крахмала.
йод + крахмал => соединение темно-синего цвета
I2 + (C6H10O5)n => I2*(C6H10O5)n
(желт.) (прозр.) (синий)
К разбавленному раствору крахмала добавляем немного раствора йода. Появляется синее окрашивание. Нагреваем синий раствор. Окраска постепенно исчезает, так как образующееся соединение неустойчиво. При охлаждении раствора окраска вновь появляется. Данная реакция иллюстрирует обратимость химических процессов и их зависимость от температуры.
Если более подробно, то…
Крахмал представляет собой природный полимер. Причем крахмал не индивидуальное вещество, а смесь двух полимеров состава (С6Н10О5)n –амилозы (10–20 %) и амилопектина (80–90 %), состоящих из остатков a-D-глюкозы.
В целом крахмал – это белое твердое вещество без запаха и вкуса, малорастворимое в холодной воде.
Являясь многоатомным спиртом, крахмал образует простые и сложные эфиры. Характерной качественной реакцией на крахмал является его реакция с йодом.
При взаимодействии йода с крахмалом образуется соединение включения (клатрат). Клатрат – это комплексное соединение, в котором частицы одного вещества («молекулы-гости») внедряются в кристаллическую структуру «молекул-хозяев». В роли «молекул-хозяев» выступают молекулы амилозы, а «гостями» являются молекулы йода. Попадая в спираль, молекулы йода испытывают сильное влияние со стороны своего окружения (ОН-групп), в результате чего увеличивается длина связи до 0,306 нм (в молекуле йода длина связи 0,267 нм). Данный процесс сопровождается изменением бурой окраски йода на сине-фиолетовую (lмакс 620–680 нм).
Амилопектин, в отличие от амилозы, дает с йодом красно-фиолетовое окрашивание (lмакс 520–555 нм). Хотя содержание амилопектина в зернах крахмала в несколько раз превышает количество амилозы, тем не менее синее окрашивание, возникающее при действии йода на амилозу, перекрывает красно-фиолетовую окраску амилопектина. Окраска исчезает при нагревании и восстанавливается при охлаждении крахмального клейстера.
Крахмал широко распространен в растениях и является для них резервным источником энергии. В основном он содержится в клубнях, семенах и корнях в виде зерен.
Крахмал используют как пищевой продукт, компонент лекарственных средств и для накрахмаливания белья. Его применяют для получения патоки, глюкозы и этилового спирта, а также в аналитической химии для обнаружения йода.
virtuallab.by
