Капилляротоксикоз это: Геморрагический васкулит: симптомы и лечение — Аллергическая пурпура — Болезнь Шенлейн-Геноха — Капилляротоксикоз
Капилляротоксикоз — это… Что такое Капилляротоксикоз?
- Капилляротоксикоз
1. Малая медицинская энциклопедия. — М.: Медицинская энциклопедия. 1991—96 гг. 2. Первая медицинская помощь. — М.: Большая Российская Энциклопедия. 1994 г. 3. Энциклопедический словарь медицинских терминов. — М.: Советская энциклопедия. — 1982—1984 гг.
- Капилляроскопи́я
- Капилляротоксико́з о́стрый инфекцио́нный
Смотреть что такое «Капилляротоксикоз» в других словарях:
капилляротоксикоз — капилляротоксикоз … Орфографический словарь-справочник
капилляротоксикоз — (capillarotoxicosis; капилляр + токсикоз) см. Васкулит геморрагический … Большой медицинский словарь
капилляротоксикоз — капилляротоксико/з, а … Слитно.

капилляротоксикоз острый инфекционный — (capillarotoxicosis acuta infectiosa) см. Лихорадка геморрагическая крымская … Большой медицинский словарь
ГЕМОРРАГИЧЕСКИЙ КАПИЛЛЯРОТОКСИКОЗ — (геморрагический васкулит) аллергическое заболевание сосудистой системы с нарушением проницаемости сосудистой стенки и геморрагическими высыпаниями. Поражаются кожа, суставы, желудочно кишечный тракт, почки … Большой Энциклопедический словарь
геморрагический капилляротоксикоз — (геморрагический васкулит), аллергическое заболевание сосудистой системы с нарушением проницаемости сосудистой стенки и геморрагическими высыпаниями. Поражаются кожа, суставы, желудочно кишечный тракт, почки. * * * ГЕМОРРАГИЧЕСКИЙ… … Энциклопедический словарь
ГЕМОРРАГИЧЕСКИЙ КАПИЛЛЯРОТОКСИКОЗ — (геморрагич. васкулит), аллергич. заболевание сосудистой системы с нарушением проницаемости сосудистой стенки и геморрагич.
высыпаниями. Поражаются кожа, суставы, желудочно кишечный тракт, почки … Естествознание. Энциклопедический словарь
геморрагический диатез — собирательное обозначение различных заболеваний, сопровождающихся геморрагиями, связанными с недостатком тромбоцитов (тромбоцитопеническая пурпура), дефицитом некоторых факторов свёртывания крови (гемофилия), поражением сосудистой стенки… … Энциклопедический словарь
Васкулит геморрагический — I Васкулит геморрагический (vasculitis haemorrhagica; синоним: болезнь Шенлейна Геноха, геморрагический микротромбоваскулит, капилляротоксикоз, аллергическая пурпура, абдоминальная пурпура, капилляропатическая пурпура, анафилактоидная пурпура… … Медицинская энциклопедия
ГЕМОРРАГИЧЕСКИЙ ДИАТЕЗ — собирательное обозначение различных заболеваний, сопровождающихся геморрагиями, связанными с недостатком тромбоцитов (тромбоцитопенического пурпура), дефицитом некоторых факторов свертывания крови (гемофилия), поражением сосудистой стенки… … Большой Энциклопедический словарь
васкулит геморрагический — (vasculitis haemorrhagica; син.
 : Геноха геморрагическая пурпура, капилляротоксикоз, пурпура анафилактическая, Шенлейна Геноха болезнь) аллергическая болезнь, характеризующаяся системным васкулитом и проявляющаяся симметричными, чаще… … Большой медицинский словарь
: Геноха геморрагическая пурпура, капилляротоксикоз, пурпура анафилактическая, Шенлейна Геноха болезнь) аллергическая болезнь, характеризующаяся системным васкулитом и проявляющаяся симметричными, чаще… … Большой медицинский словарь
Капилляротоксикоз: причины, симптомы и лечение
Капилляротоксикоз – это довольно распространенная патология, которая заключается в аллергическом поражении кожи и сосудистых стенок, а также резком увеличении их проницаемости. Данную болезнь еще называют геморрагическим васкулитом или болезнью Шенлейна-Геноха. Несмотря на большое распространение, болезнь является весьма серьезной и требует тщательного наблюдения и лечения.
В этой статье пойдет речь о механизме и причинах возникновения капилляротоксикоза у взрослых и в детском возрасте, а также о проявлениях этой патологии и используемых методах диагностики и лечения.
Болезнь может возникнуть в любом возрасте
О геморрагическом васкулите и его причинах
Болезнь Шенлейна-Геноха на сегодняшний день является одной из наиболее распространенных геморрагических патологий.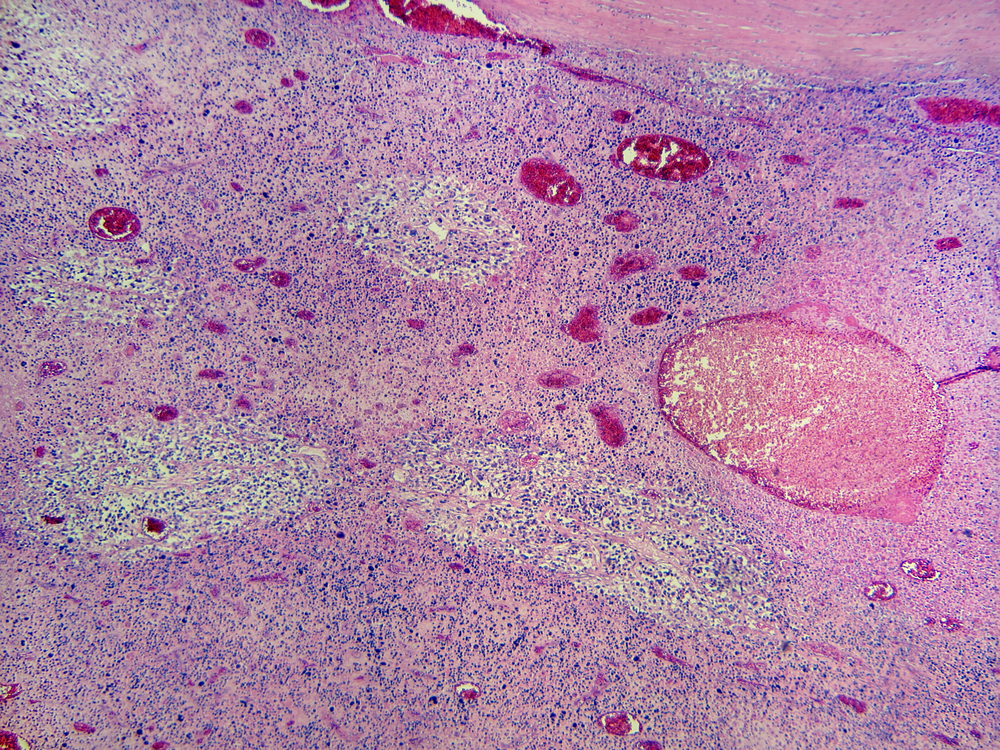 В целом она имеет аллергический характер, но с поражением капилляров, мелких венул и артериол.
В целом она имеет аллергический характер, но с поражением капилляров, мелких венул и артериол.
У детей его можно встретить в возрасте от 4 до 14 лет, а среднее количество больных детей варьируется в пределах 25 человек к 10 тыс.
К причинам, оказывающим провоцирующее влияние относят:
- вирусные заболевания;
- бактериальные заболевания;
- паразитов;
- вакцинацию;
- наличие медикаментозной или алиментарной аллергии;
- переохлаждение.
Патологию может спровоцировать даже банальный ОРВИ
Множество авторов медицинских работ подчеркивают, что развитие геморрагического васкулита под воздействием конкретных причин возможно лишь при наличии генетической предрасположенности. Механизм развития капиллярного токсикоза лежит в образовании иммунных комплексов.
Во время циркуляции в крови происходит их отложение на внутренних поверхностях стенок мелких сосудов и последующее их повреждение, сопровождающееся асептическим воспалительным процессом. Когда стенки воспаляются, у них повышается проницаемость и в просвете сосуда откладывается фибрин и тромботические массы.
Когда стенки воспаляются, у них повышается проницаемость и в просвете сосуда откладывается фибрин и тромботические массы.
Именно этими процессами геморрагический васкулит и обязан своим основным патологическим признакам – микротромбированию и геморрагическому синдрому.
Капиллярный токсикоз может иметь разный размер
Виды капилляротоксикоза
В клиническом развитии заболевания существует острая фаза (начало заболевания или обострение) и фаза стихания (период улучшения).
В зависимости от преобладающих симптомов врач может классифицировать одну из форм:
- простую;
- суставную;
- абдоминальную;
- молниеносную.
Кроме того, заболевание может протекать в острой (около 2 месяцев), затяжной (до 6 мес.) и хронической форме. Помимо форм болезнь Шенлейна-Геноха имеет определенные степени тяжести, влияющие на ход течения болезни.
- Легкая степень. В этом случае состояние пациентов удовлетворительное, сыпь не обильна, наблюдаются артралгии.

- Средняя степень. Состояние определяют как средней тяжести, сыпь имеет обильный характер, к артралгиям добавляются изменения в суставах по типу артрита, возникают периодические болезненные ощущения в животе, микрогематурия.
- Тяжелая степень. Состояние тяжелое, сыпь значительно распространена, с участками некроза. Наблюдается нефротический синдром, ангионевротические отеки, макрогематурия, кровотечения из ЖКТ, в некоторых случаях – острая почечная недостаточность.
Важно! Несмотря на то, что болезнь в детском возрасте встречается у детей от 4-5 лет и старше, бывают случаи капилляротоксикоза у более младших детей. Поэтому важно серьезно относится к любой сыпи у ребенка.
Заболевание имеет несколько степеней тяжести
Как себя проявляет капиллярный токсикоз?
Симптомы этого заболевания довольно разнообразны, и в основном происходит преобладание одного или нескольких синдромов. Болезнь всегда имеет острое начало с повышением температуры тела.
Боль в животе частый сопутствующий симптом болезни
Могут наблюдаться такие синдромы:
Кожный
– имеет место абсолютно у всех пациентов и проявляется в начальном периоде заболевания. В этом случае на коже образуются пятнисто-папулезные геморрагические элементы разного размера, которые не исчезают при надавливании. Иногда можно заметить уртикарную сыпь. Расположены высыпания симметрично, в нижней части голеней, на бедрах и ягодицах, около больших суставов, иногда – на руках и туловище. Часто обильность сыпи связывают со степенью тяжести заболевания. Если степень тяжелая – наблюдается некроз в центре элемента сыпи, с последующим образованием язвы. В период разрешения высыпания заканчиваются гиперпигментацией, которая сохраняется длительное время.
Суставной
– встречается у 65-80% пациентов. Поражения могут иметь кратковременный характер по типу небольшой артралгии, либо сохраняться на протяжении пары дней с выраженными болями, отечностью, покраснениями и нарушениями движений в пораженных суставах, характерными для артрита.

Абдоминальный
– иногда предшествует кожно-суставным проявлениям или сопровождает их. Возникают боли в животе, различные по интенсивности. Иногда пациентам не удается указать конкретную локализацию болей. Возникает тошнота и рвота, нарушение стула. Боли могут возникать несколько раз за день и проходить самостоятельно, либо исчезают в первые сутки после получаемого лечения. В более тяжелых случаях может возникнуть кровотечение из ЖКТ, рвота с кровью, диарея с примесью крови.
Почечный
– наименее распространен и наблюдается меньше чем у 30% больных. Сопровождается симптомами гломерулонефрита и гематурией различной степени, у некоторых пациентов наблюдается нефротический синдром. Несмотря на редкость, поражения почек наиболее стойкий симптом капилляротоксикоза и может вызвать почечную недостаточность.

Симптомы, связанные с поражением других органов, практически не встречаются. Однако, если они возникают, то сюда относят миокардит, геморрагический перикардит, одышку, кашель с прожилками крови, головокружение, головную боль, геморрагический инсульт.
После заживления сыпи, некоторое время на коже остаются участки гиперпигментации
Методы диагностики капиллярного токсикоза
При подозрении на геморрагический васкулит необходимо обращение за консультацией ревматолога. На приеме учитывают возраст, собирают анамнез, изучают показатели клинических и лабораторных методов исследований, а также исключают наличие других заболеваний.
В ОАК у больных геморрагическим васкулитом можно наблюдать лейкоцитоз и незначительное увеличение СОЭ, повышенное содержание тромбоцитов и эозинофилов.
Кроме ОАК назначают следующие исследования:
- ОАМ;
- коагулограмму;
- биохимический анализ мочи;
- пробу Зимницкого;
- УЗИ почек;
- гастроскопию;
- УЗИ органов брюшной полости;
- анализ кала на скрытую кровь;
- биопсию кожи.

Цена анализов крови и мочи в целом не является высокой и позволяет дать врачу точные данные, в случае своевременного обращения в медицинское учреждение. Кроме того, проводят дифференциальную диагностику с лейкозом, ревматоидным артритом, системным васкулитом, болезнью Стилла, острым гломерулонефритом и тромбоцитопенической пурпурой.
Анализы крови необходимы для точной постановки диагноза
Принципы терапии капилляротоксикоза
Лечение этого заболевания у пациентов с острой фазой сопровождается четкой необходимостью соблюдения постельного режима, гипоаллергенной диеты, абсолютного иключения антибиотиков и прочих препаратов, которые усиливают сенсибилизацию организма.
Основным средством для лечения геморрагического васкулита является гепарин. Инструкция к этому препарату гласит, что он замедляет свертывание крови, а также растворяет кровяные сгустки.
Использование преднизолона не дает 100% эффективности, поэтому является спорной терапией. В случае отсутствия результата от кортикостероидной терапии используют цитостатики. При тяжелом течении проводят гемосорбцию, иммуносорбцию и плазмоферез.
Гепарин – основной препарат для лечения капилляротоксикоза
При выраженном суставном синдроме используют противовоспалительные препараты. Применение антигистаминных возможно в случае аллергического анамнеза или эксудативно-катарального диатеза. Если имеет место абдоминальный синдром и пищевая аллергия – назначают энтеросорбенты.
Из фото и видео в этой статье нам удалось узнать про особенности капилляротоксикоза, а именно о синдромах, которыми он сопровождается, его формах и степенях, методах постановки диагноза и подбора терапии.
виды, причины, симптомы и лечение
Капилляротоксикоз – синоним геморрагического васкулита, болезни Шенлейн-Геноха. Речь идет о довольно распространенном поражении кожных покровов и стенок сосудов. Это довольно серьезное заболевание, которое требует обязательной длительной, комплексной терапии.
Это довольно серьезное заболевание, которое требует обязательной длительной, комплексной терапии.
Не занимайтесь самолечением. При первых признаках заболевания обращайтесь к врачу.
Прогноз, как правило, носит благоприятный характер, но только при условии своевременного начала терапевтических мероприятий. Чаще всего заболевание диагностируется у молодых людей, но четкого разграничения по половому и возрастному признаку нет.
Первопричина данной патологии — аллергическое поражение организма. Запуск такой реакции провоцируется целым рядом неблагоприятных факторов. Зачастую речь идет о продуктах питания, химических элементах либо лекарственных препаратов. Важное требование — триггер должен спровоцировать в организме нетипичную реакцию. Аллергены сами по себе могут быть различными, поэтому выделяют различные и формы и симптомы болезни.
Такое поражение зачастую встречается у малышей. У них эта патология протекает в разы тяжелее. Достаточно часто капилляротоксикоз может развиваться на фоне осложненной ангины, после медицинских вмешательств. В целом капилляротоксикоз у детей чаще всего — результат непосредственного влияния аллергена на слабый, незащищенный организм. У взрослых лиц несколько иной принцип развития заболевания. Капилляротоксикоз у взрослых провоцирует скрытая инфекция. При геморрагическом васкулите поражение может распространиться на любые органы. То есть, болезнь довольно часто развивается в почечных, сердечных структурах.
В целом капилляротоксикоз у детей чаще всего — результат непосредственного влияния аллергена на слабый, незащищенный организм. У взрослых лиц несколько иной принцип развития заболевания. Капилляротоксикоз у взрослых провоцирует скрытая инфекция. При геморрагическом васкулите поражение может распространиться на любые органы. То есть, болезнь довольно часто развивается в почечных, сердечных структурах.
В целом можно выделить такие этиологические факторы, которые провоцируют капилляротоксикоз:
- острые бактериальные инфекции;
- длительно текущие инфекционные заболевания с частыми рецидивами;
- вирусные заболевания;
- радиоактивное или лучевое облучение;
- сахарный диабет;
- системные заболевания;
- аллергическая реакция на лекарства или прививки;
- частое и длительное переохлаждение.
Не исключается и такая причина, как наследственная предрасположенность к заболеванию.
Капилляротоксикоз бывает нескольких форм. При этом радикально отличается клиника, симптоматика и выраженность поражения. Выделяют такие виды патологического процесса:
- некротическая форма. Такой капилляротоксикоз диагностируется у детей. На коже появляются всевозможные образования в виде пятен, узелковых элементов. Симптомы то появляются, то исчезают, но с каждым разом элементы только увеличиваются в размерах и усиливаются до некрозов. Данная форма является не только самой тяжелой, но и самой редкой.
- кожная форма;
- кожно-суставная форма поражения. Она зачастую развивается у взрослых больных. Появляется лихорадка, болезненность в суставах, мышцах. В ряде случаев бывают довольно интенсивные кровотечения;
- почечная форма – геморрагические высыпания образуются в тканях почек;
- смешанная форма – капилляротоксикоз такого вида сочетает в себе клинику вышеописанных форм.
Патологический процесс затрагивает внутренние органы. Основными симптомами заболевания становятся геморрагические поражения желудочно-кишечного тракта.
Основными симптомами заболевания становятся геморрагические поражения желудочно-кишечного тракта.
Клиническая картина общего характера у взрослого характеризуется таким образом:
- геморрагии на кожных покровах;
- поражение суставного аппарата в виде артралгий, артритов;
- сбои в работе желудочно-кишечного тракта, которые часто сопровождаются внутренним кровотечением;
- поражение тканей почек, что будет проявляться в виде нарушения работы мочеполовой системы.
Капилляротоксикоз у детей сопровождается:
- геморрагическими высыпаниями;
- болезненностью в животе, отчего ребенок становится капризным, постоянно плачет, плохо ест.
Очень часто заболевание сопровождается появлением гранулоцитов в сосудистой стенке.
Геморрагические высыпания при капилляротоксикозе
Как показывает практика, чем раньше диагностировано капилляротоксичное заболевание, тем проще его излечить. Специфических лабораторных тестов, по которым можно уверенно поставить диагноз геморрагического васкулита, сегодня не существует. Для предварительного диагноза важно провести анализы на иммунный статус в крови. Выявляют неспецифический лейкоцитоз и увеличение СОЭ. Изменения в первую очередь выявляются именно в крови. Определяющим симптомом называют значительное увеличение IgA. Проводят такие анализы:
Специфических лабораторных тестов, по которым можно уверенно поставить диагноз геморрагического васкулита, сегодня не существует. Для предварительного диагноза важно провести анализы на иммунный статус в крови. Выявляют неспецифический лейкоцитоз и увеличение СОЭ. Изменения в первую очередь выявляются именно в крови. Определяющим симптомом называют значительное увеличение IgA. Проводят такие анализы:
- общий анализ крови и развернутый биохимический;
- общий анализ мочи;
- УЗИ мочеполовой системы;
- гастроэнтерологические исследования – ФГДС, эндоскопия, УЗИ.
Капилляротоксикоз у взрослых и детей диагностируется одинаково. После получения результатов необходимых исследований доктором будут установлены причины болезни, предписана эффективная терапия и соблюдение правильного режима питания, которого следует придерживаться.
Капилляротоксикоз лечение подразумевает только комплексное. Для успешного лечения необходимо не только устранить клинику патологического процесса, но и нейтрализовать действие патогенных микроорганизмов, а также убрать все очаги инфекции, способные спровоцировать новый патологический иммунный ответ. Для этого больному предписывают курсы десенсибилизирующих (устраняющих аллергические проявления) медикаментозных средств, а также проводят лечение антибиотиками. При назначении антибиотиков требуется обязательно учитывать тесты на переносимость, так как антибиотики сами по себе обладают высокой аллергенностью.
Для этого больному предписывают курсы десенсибилизирующих (устраняющих аллергические проявления) медикаментозных средств, а также проводят лечение антибиотиками. При назначении антибиотиков требуется обязательно учитывать тесты на переносимость, так как антибиотики сами по себе обладают высокой аллергенностью.
Важно устранить все основные симптомы заболевания, именуемого как геморрагический васкулит. Для этого в схему комплексной терапии при капилляротоксикозе включены также иммуномодуляторы. Симптомы патологии довольно быстро минимизируются, ведь данные лекарства заставляют защитные механизмы человека работать более активно.
Терапия болезни обязательно включает препараты, укрепляющие капилляры, а также антикоагулянты, регулирующие вязкость крови, и препараты, воздействующие на трофику тканей. При тяжелом течении болезни проводят лечение гормонами.
В целом схема терапии нетяжелой формы заболевания включает:
- антигистаминные препараты — «Супрастин» или «Димедрол»;
- витамин С и «Рутин»;
- глюконат кальция;
- растворы хлорида кальция внутривенно;
- (при тяжелом течении) кортикостероиды.

Геморрагическую болезнь лечат индивидуально. Для каждого больного подбирается своя схема и дозировка медикаментов. Для этого лечащий врач детально изучает течение заболевания, особенности каждого больного.
Геморрагический патологический процесс нужно лечить и наружными (местными) медикаментами. Широко используются мази, гели. Среди них:
- «Венорутон»;
- «Солкосерил».
При наличии тяжелой почечной формы заболевания иногда даже показан гемодиализ.
Важным элементом комплексной терапии является применение средств нетрадиционной терапии. В домашних условиях обычно используют:
- цветки арники;
- гвоздику;
- руту.
При наличии частых, интенсивных рецидивов показано санаторно-курортное лечение. Больным категорически запрещено курить, употреблять спиртное либо наркотические вещества, назначается диета.
Важно не допустить новых эпизодов патологии. Для этого показана санация очагов инфекции. Больным нельзя находиться на солнце. Прогноз капилляротоксикоз носит благоприятный. Но вместе с этим не всегда удается полностью излечить патологию. Более того, течение болезни не всегда возможно спрогнозировать.
Больным нельзя находиться на солнце. Прогноз капилляротоксикоз носит благоприятный. Но вместе с этим не всегда удается полностью излечить патологию. Более того, течение болезни не всегда возможно спрогнозировать.
Капилляротоксикоз — особенности, симптомы и лечение
Содержание:
Капилляротоксикоз – частая патология аллергического характера, при которой страдает не только кожа, но и стенки капилляров, что негативно сказывается на их проницаемости.
Заболевание диагностировать очень сложно, так как обычно оно проявляется на фоне других болезней. Это может вызвать серьёзные осложнения, избавиться от которых уже не получится.
Основные сведения
Второе название этого состояния – болезнь Шенлейна-Геноха. В его основе – истончение стенок самых мелких сосудов, которые называются капиллярами. Из-за этого появляются не только симптомы на поверхности тела, но и происходит деформация внутренних органов. Чаще всего диагностируется у мужчин и у детей. Причём капилляротоксикоз у детей протекает очень тяжело и с разными осложнениями.
Из-за этого появляются не только симптомы на поверхности тела, но и происходит деформация внутренних органов. Чаще всего диагностируется у мужчин и у детей. Причём капилляротоксикоз у детей протекает очень тяжело и с разными осложнениями.
Обычно симптомы появляются весной и осенью, особенно если до этого была простуда, грипп или ангина, либо было сильное переохлаждение. Симптомы будут зависеть не только от возраста и степени тяжести, но и формы.
Особенности протекания у мужчин и женщин
Чтобы вовремя обратиться к врачу, следует обязательно знать симптомы этой болезни. Признаки будут полностью зависеть от клинического типа, поэтому доктор может выявить один из них. Это:
- Кожный.
- Почечный.
- Суставной.
- Абдоминальный.
- Геморрагический.
- Злокачественный, который считается самым серьёзным и отличается от остальных моментальным распространением по всему телу.
Капилляротоксикоз почечной формы относится к одному из самых тяжёлых. Кроме симптомов аллергии, которая появляется на коже, отличается снижением количества мочи, болями в пояснице, отёками ног и повышенным давлением.
Кроме симптомов аллергии, которая появляется на коже, отличается снижением количества мочи, болями в пояснице, отёками ног и повышенным давлением.
Кожная форма затрагивает только руки и ноги, а также места их сгибов. Сыпь несимметричная, может появиться на лице, ладонях, стопах, ягодицах. Нередко вместо сыпи появляются пузырьки с жидким содержимым, которые лопаются и начинают подсыхать, при этом охватывая большую площадь из-за слияния между собой. Это приводит к сильному отёку, а затем появляется шелушение, которое чаще всего заканчивается появлением пигментных пятен.
При суставной форме сыпь распространяется на всё тело, а через несколько дней начинают появляются суставные синдромы – болевые ощущения в коленях или локтях, припухлость. Затем все симптомы исчезают сами по себе, но могут появиться снова при повторном появлении сыпи.
Особенности течения у малышей
Капилляротоксикоз у детей проявляется кожной сыпью, которая может быть разной степени интенсивности. В основном она появляется на ногах в районах суставов, редко затрагивает лицо и шею.
В основном она появляется на ногах в районах суставов, редко затрагивает лицо и шею.
Как только появилась сыпь, начинается и поражение капилляров. Поэтому многие детки жалуются на боли в животе, вздутие кишечника. Ребёнок постоянно лежит на боку с притянутыми к животу ногами. Наступает отёк мягких тканей, нередко в этот момент развивается рвота и тошнота.
У деток первого года жизни заболевание развивается мгновенно, из-за чего и называется злокачественным. Появляются сразу все симптомы, которые могут нанести непоправимый вред организму малыша.
Основные провоцирующие факторы
Капилляротоксикоз у взрослых и у детей имеет свои причины. Чаще всего ими становятся:
- Неправильное питание.
- Реакция на прививку.
- Ангина и другие затяжные инфекции.
- Переохлаждение.
- Заражение глистами.
- Нарушения в работе эндокринной системы.
- Повреждение кожи.
- Резкая смена температуры воздуха.
Каждый случай строго индивидуален, поэтому разобраться в причинах и назначить правильное лечение может только врач.
Как избавиться
Лечение капилляротоксикоза должен проводить врач. Первое, что следует сделать – купировать все имеющиеся симптомы при помощи лекарственных препаратов. Затем нужно выяснить, что стало причиной такой резкой аллергической реакции и почему произошло поражение капилляров. А перед этим следует обязательно нейтрализовать все антигены, которые и вызывают воспалительный и аллергический процесс.
И, наконец, при помощи антибиотиков нужно блокировать все очаги инфекции. На фоне лечения антибиотиками нужно длительное время принимать лекарств от аллергии и препараты, которые положительно влияют на состояние иммунной системы. Необходимо принимать лекарства для укрепления стенки сосудов и для регуляции вязкости крови. При наличии осложнений и тяжёлой степени тяжести лечение только стационарное с применением гормональных препаратов.
Определить симптомы и лечить капилляротоксикоз у детей должен не только педиатр, но и дерматолог, а также врач – аллерголог.
Последствия без лечения могут быть самыми серьёзными, включая внутреннее кровотечение и развитие перитонита. Нередко нарушается работа кишечника, внутренних органов и суставов.
Геморрагический васкулит — симптомы, лечение, причины болезни, первые признаки
Описание
Геморрагический васкулит или болезнь Шенлейн-Геноха – это распространенная разновидность васкулитов, при которой происходит воспалительное поражение микрососудов, а также их микротромбообразование.
Согласно статистике, геморрагическим васкулитом страдает около 14 человек из 100000 населения.
Наиболее часто данное заболевание поражает сосуды почек, органов ЖКТ и кожных покровов. При геморрагическом васкулите кожной формы у больных возникает характерная сыпь. Именно поэтому данную патологию еще называют аллергическим геморрагическим васкулитом.
Геморрагическим васкулитом страдают пациенты разных возрастов, однако, у детей младше 3 лет он встречается реже. Основной процент пациентов составляют дети и подростки в возрасте 4-20 лет (около 40% от всех пациентов). Примечательно, что геморрагическим васкулитом страдают чаще представители мужского пола (соотношение больных 2:1). Как правило, пик заболеваемости приходится на весну.
Примечательно, что геморрагическим васкулитом страдают чаще представители мужского пола (соотношение больных 2:1). Как правило, пик заболеваемости приходится на весну.
Код МКБ 10 геморрагического васкулита имеет вид D65-D69. Это значит, что он относится к группе заболеваний под шифром D69, то есть имеет признаки аллергической пурпуры. В то же время D65 говорит о наличии внутрисосудистых патологий, при которых происходит нарушение свертываемости крови.
Патогенез и причины патологии
Возбудителями болезни Шлеймана-Геноха являются стрептококки, микоплазмы, а также респираторные инфекции.
Именно поэтому заболевание чаще всего начинает проявлять свои первые симптомы спустя неделю-месяц после перенесенных тяжелых инфекционных заболеваний.
Однако причиной заболевания могут быть не только инфекции. Нередко толчком к развитию болезни становится переохлаждение, использование некачественной вакцины или неподходящих медикаментозных препаратов, аллергические реакции, а также укусы насекомых или ожоги. Причины геморрагического васкулита у взрослых могут заключаться в применении некоторых антибактериальных препаратов, особенно, пенициллиновой группы.
Причины геморрагического васкулита у взрослых могут заключаться в применении некоторых антибактериальных препаратов, особенно, пенициллиновой группы.
Причиной такого заболевания как геморрагический васкулит может быть нарушение иммунитета пациента. Замечено, что люди, склонные к различным проявлениям аллергических реакций, страдают болезнью Шенлейна Геноха несколько чаще. Так, иммунная система некоторых больных активирует систему комплимента, которая в итоге начинает атаковать сосуды собственного организма. Клетки иммунитета также могут внедряться в стенки пораженных сосудов. В результате этого происходит свертывание крови и, как следствие, тромбообразование. Так как стенки сосудов утрачивают свою целостность, то кровь, находящаяся в них, начинает выходить наружу. Этим и объясняется образование красных пятен при кожном геморрагическом васкулите.
Геморрагический васкулит у взрослых часто сочетается с нарушениями метаболизма. Беременность женщины также может стать провоцирующим фактором в развитии заболевания. Это связано с тем, что организм пациенток в этот период легко поддается влиянию различных неблагоприятных факторов извне. Геморрагический васкулит при беременности может сопровождаться отслоением плаценты, кислородным голоданием и недоразвитием плода.
Это связано с тем, что организм пациенток в этот период легко поддается влиянию различных неблагоприятных факторов извне. Геморрагический васкулит при беременности может сопровождаться отслоением плаценты, кислородным голоданием и недоразвитием плода.
Какой врач лечит геморрагический васкулит?
При возникновении первых симптомов заболевания больной должен как можно скорее обратиться к своему участковом терапевту. И хотя он не занимается лечением данного заболевания, но может направить пациента к специалисту, который необходим. Как правило, к ревмтологу – врачу, который занимается лечением ревматических заболеваний. К таким относятся и различные патологии соединительных тканей и суставов, характеризующиеся аутоиммунной природой. В эту группу заболевании входит и геморрагический васкулит. В некоторых случаях для назначения правильного лечения может потребоваться консультация специалистов более узких направлений, например, нефролога или хирурга. Только после этого больному будет поставлен точный диагноз, назначено правильное лечение и рекомендована диета.
Разновидности геморрагических васкулитов
По характеру клинического течения геморрагический васкулит делится на острый (как правило, бывает на первых этапах заболевания или в моменты обострения) и находящийся в фазе стихания (период, когда самочувствие больного улучшается).
Исходя из степени тяжести, болезнь Шенлейна Геноха бывает:
- легкой степени. В данном случае у больного относительно удовлетворительное состояние. У него присутствует небольшое количество сыпи, а суставные боли слабовыраженные;
- средней степени. У больного присутствует обильная сыпь, суставные боли часто сочетаются с артритом, иногда возникает дискомфорт в брюшной полости, в моче могут присутствовать примеси крови;
- тяжелой степени. На теле больного присутствуют множественные высыпания с участками некроза, возникает отек Квинке, происходит нарушение белково-липидного комплекса в результате поражения почек, присутствует кровь в моче, возникают кровотечения в органах ЖКТ.
 В некоторых случаях почки могут прекратить выполнять свои функции.
В некоторых случаях почки могут прекратить выполнять свои функции.
По длительности течения заболевание делится на: острое (меньше 2 месяцев), затяжное (около 6 месяцев) и хроническое.
Исходя из того какой тип органов поражает заболевание, формы геморрагического васкулита могут быть следующими:
- геморрагический васкулит кожи – заболевание поражает исключительно кожные покровы. Наиболее часто кожная форма болезни развивается по причине наследственной предрасположенности, инфекции и аллергии;
- кожно-суставная форма геморрагического васкулита – помимо кожи происходит поражение еще и суставов, причем, как правило, крупных (например, коленные). Примечательно, что врачи чаще диагностируют геморрагический васкулит ног, который нередко сопровождается их отеком;
- геморрагический васкулит абдоминальной формы – заболевание поражает кожу и органы ЖКТ. При этой форме пациенты могут жаловаться на дискомфорт в брюшной полости;
- почечный – заболевание поражает почки.
 При этой разновидности патологии высыпания на коже практически никогда не возникают.
При этой разновидности патологии высыпания на коже практически никогда не возникают.
Геморрагический васкулит у детей
В отличие от взрослых геморрагический васкулит у детей протекает чаще без наличия высыпаний на кожных покровах (в 50% случаев). У взрослых же этот показатель равняется 30%. У пациентов детского возраста заболевание начинается с поражения органов пищеварения и суставов.
Поражение почек у них встречается достаточно редко, протекает в легкой форме, а функция органов после выздоровления быстро восстанавливается. Сердце при данной патологии у детей также страдает гораздо реже, нежели у взрослых.
Исходя из этого, становится понятно, что прогноз заболевания у детей достаточно благоприятный, особенно, при своевременной диагностике, правильном лечении и недопущении перехода заболевания из острой стадии в хроническую. Однако, исходя из того, что точные причины геморрагического васкулита до сих пор не выяснены, даже после выздоровления таким детям требуется пожизненный охранный режим.
Прогноз и последствия
Геморрагический васкулит кожной формы не представляет угрозы жизни пациента. При условии своевременной диагностики и лечения 50% больных успешно излечиваются. У остальных пациентов врачи добиваются ремиссии, которая, к сожалению, время от времени может переходить в острую форму.
В целом прогноз заболевания во многом зависит от формы патологии, вызвавших ее причин и характера ее течения.
Хроническая форма заболевания с периодическими обострениями симптомов и минимальным поражением почек имеет один из самых благоприятных прогнозов. Однако при отсутствии лечения последствием геморрагического васкулита у взрослых может быть нарушение работы почек. В итоге больному всю жизнь придется проходить медицинские процедуры по очищению крови. При тяжелой форме кожно-абдоминального геморрагического васкулита спрогнозировать итог болезни сложно.
Среди основных последствий геморрагического васкулита можно выделить:
- воспалительное поражение органов брюшной полости;
- хронические заболевания почек, характеризующиеся расстройством их функций на срок 3 месяцев и более;
- нарушение проходимости кишечника, гибель некоторых участков внутренних органов;
- снижение гемоглобина;
- нарушение функций внутренних органов и систем.

Пациентов с геморрагическим васкулитом в армию не призывают. Обычно им выдают военный билет и отправляют в запас.
Симптомы
Фото: offeringhope.org
Геморрагический васкулит – заболевание довольно редкое. Оно поражает сосуды и капилляры и относится к разряду инфекционно – аллергических сосудистых заболеваний. В зависимости от формы и сложности заболевания симптоматика может несколько разниться.
Для острого течения васкулита характерно проявление всех (или практически всех) симптомов одновременно. Особенно следует выделить так называемое молниеносное протекание болезни. В этом случае нужно как можно скорее обратиться за квалифицированной медицинской неотложной помощью в условиях реанимации. В противном же случае больной рискует умереть по причине почечной недостаточности, спустя всего несколько часов от начала проявления симптоматики.
Но обычно протекание болезни не такое стремительное, и симптомы недуга проявляются на протяжении некоторого времени (к примеру – недели). Это не означает, что вы не должны реагировать, как только заметите подобные признаки заболевания. Следует незамедлительно обратиться за помощью к специалистам. Симптомы проявляются постепенно и могут даже исчезать, но это не значит, что недуг отступил.
Это не означает, что вы не должны реагировать, как только заметите подобные признаки заболевания. Следует незамедлительно обратиться за помощью к специалистам. Симптомы проявляются постепенно и могут даже исчезать, но это не значит, что недуг отступил.
Вне зависимости от сложности и скоротечности васкулита он у взрослых проявляются следующие симптомы:
- Сыпь на коже при васкулите. Зачастую проявление симптомов начинается именно с появления сыпи или, скорее, маленьких кровоизлияний в области голеней и ступней ног. Со временем высыпания поднимаются выше, и поражают участки на бедрах и ягодицах, участки вокруг суставов. В редких случаях высыпания также появляются на животе и нижней части спины. Визуально высыпания выглядят как небольшие красные пузырьки, которые не исчезают даже после надавливания. Сыпь может быть разной насыщенности: как небольшие отдельные пятнышки, так и обширные образования, которые сливаются между собой. Со временем такие пятнышки превратятся в пигментные пятна.
- У некоторых пациентов наблюдается повышение температуры до 38-39°С, состояние больного характеризируется вялостью, присутствует ощущение усталости и тяжести. Больному лучше предложить прилечь и постараться отдохнуть. Не стоит беспокоить пациента до приезда врача.
- Зуд на коже. В половине случаев заболевания геморрагическим васкулитом симптомы включают в себя зуд. Начинается он зачастую при появлении на месте высыпания небольших язвочек, которые образуются вследствие некроза тканей на месте высыпаний.
- Характерным симптомом при геморрагическом васкулите является боль в суставах. Зачастую она появляется на первых стадиях заболевания. Боль появляется в крупных суставах коленных чашечек или тазобедренных суставах. Иногда воспаленные суставы отекают и даже немного изменяют свою форму. Через несколько дней припухлость проходит сама собой, а боль купируется, и работа сустава приходит в норму.
- Болевые ощущения в области живота. Она появляется вследствие желудочно-кишечных кровоизлияний. Довольно часто этот признак проявляется вместе с другими симптомами геморрагического васкулита у взрослых. Боли напоминают схватки и уменьшаются при принятии коленно-локтевой позы. Иногда к симптомам геморрагического васкулита добавляются рвота и жидкий стул с примесями крови или слизи. Но спустя несколько дней симптомы острой боли пройдут самостоятельно.
- Поражение почек – один из самых важных и опасных симптомов геморрагического васкулита. У больного появляются ноющие боли в нижней части спины, отекает лицо и руки, повышается температура. Иногда в моче появляются небольшие примеси крови. Пациент ощущает постоянную слабость и апатию, бледнеет лицо, постоянно отсутствует аппетит. К этим симптомам нужно отнестись особенно внимательно, потому что они при геморрагическом васкулите ведут к развитию почечной недостаточности, которая, в свою очередь, может повлечь летальный исход.
Кроме описанных выше общепринятых симптомов могут появляться еще и индивидуальные, к ним относится:
- Головная боль и мигрени;
- Головокружения;
- Ухудшение памяти;
- Рассеяность;
- Раздражительность.
Все они свидетельствуют о нарушениях в работе центральной нервной системы. Также диагностируются поражения легких, которые проявляются тяжелым кашлем с отхаркиванием кровяной слизи, отдышкой. Иногда мужчины чувствуют боли и отечность в области яичек.
Симптомы у детей
К сожалению, подвергнуты воздействию данной болезни не только взрослые, но и дети. При этом симптоматика у малышей несколько отличается. Помните, что самолечение ведет только к усугублению заболевания. Обязательно стоит посетить врача педиатра для определения точного диагноза и выбора лечения для ребенка.
При геморрагическом васкулите в зависимости от характера симптомов различают следующие синдромы:
- Кожный
- Суставной
- Почечный
- Абдоминальный
- Злокачественный с молниеносным протеканием.
Все они могут выступать, объединившись с несколькими другими, или самостоятельно. При геморрагическом васкулите отмечается поражение сосудов в любой области, в том числе могут быть затронуты легкие, почки, мозг и его оболочки.
Рассмотрим геморрагический васкулит и его симптомы у детей подробнее:
- Кожный синдром. Этот симптом встречается чаще остальных. Сыпь поражает чаще всего ноги, ягодицы, реже – нижнюю часть спины и живота. Выглядит она как кровянистые прыщики, иногда (в более тяжелой форме) она покрывается корочками и принимает вид небольших язвочек. Даже после излечения болезни на месте сыпи остается заметная пигментация.
- Суставной синдром. Он появляется вместе с сыпью или спустя немного времени после ее появления и характеризуется болью разной интенсивности в области больших суставов. Чаще всего у детей боль проходит достаточно быстро, но может рецидивировать во время повторного высыпания.
- Абдоминальный синдром при геморрагическом васкулите наблюдается довольно часто (примерно у 65% больных детей). Абдоминальный синдром зачастую предшествует сыпи и другим симптомам геморрагического васкулита, что делает диагностику заболевания довольно трудной. Боль в животе имеет схваткообразный характер и зачастую очень сильная. Обусловлена она кровоизлияниями в стенку кишечника, возможна кровавая рвота или дефекация с примесями крови. При обильных кровотечениях наблюдается потеря сознания или резкое развитие анемии, провоцируется кишечная непроходимость, аппендицит и перекрут кисты яичника. Именно поэтому очень важно обратить внимание на симптомы как можно раньше и обратится к врачу за помощью.
Диагностировать геморрагический васкулит, симптомы которого достаточно двухзначны, достаточно сложно, что нередко приводит к ненужным хирургическим вмешательствам.
У детей симптомы иногда проявляются головными болями и другими нарушениями центральной нервной системы, поражениями легких и кровоизлияниями в легкие. При геморрагическом васкулите также могут быть обнаружены примеси крови в моче.
Диагностика
Фото: glisty24.ru
Диагноз геморрагический васкулит может устанавливать только врач, исходя из характера кожных высыпаний, в том числе – исходя из наличия или отсутствия высыпаний на ногах. Однако не все так просто. Даже у опытных медицинских работников могут возникать проблемы постановкой диагноза, в случае если у пациента первые симптомы проявились не в виде кожных высыпаний, а в виде болей в суставах или дискомфорта в брюшной полости. Как правило, данные признаки заболевания сопровождаются еще и химическими изменениями состава мочи.
Обычно точный диагноз врач ставит только после появления на теле пациента сыпи.
Геморрагический васкулит – это довольно редкое и сложное заболевание, поэтому для постановки точного диагноза больному, возможно, придется обратиться не только к участковому терапевту.
Для подтверждения диагноза пациенты порой вынуждены пройти обследование у хирурга, нефролога, пульмонолога, иммунолога, инфекциониста, ЛОР-врача, стоматолога (для возможного выявления и лечения инфекций в ротовой полости) и аллерголога.
Для того чтобы отличить геморрагический васкулит от других болезней, практически всегда требуется помощь врача-узиста, рентгенолаборанта и некоторых других медицинских работников.
Лабораторные методы исследования
Для диагностики геморрагического васкулита практически всегда нужны различные анализы биологических жидкостей.
Клинический анализ крови при геморрагическом васкулите – это способ лабораторного исследования, который определяет, в каком количество содержится каждый тип клеток крови. Благодаря этому медицинские работники могут оценить состояние внутренних органов и систем пациента.
Как правило, при проведении анализа крови у больных обнаруживается повышение уровня лейкоцитов, эозинофилов, нейтрофльных гранулоцитов и тромбоцитов. Если у пациента отсутствуют кровотечения внутренних органов, то количество гемоглобина и эритроцитов остается в нормальном количестве.
Помимо данного анализа врачи нередко прибегают к проведению общего анализа мочи.
Общий анализ мочи – это метод лабораторного исследования, при котором специалисты определяют физические свойства и химический состав мочи пациента.
Показатели общего анализа мочи у пациентов могут отличаться от нормальных, если болезнь сопровождается воспалительным поражением почек. В этом случае анализ обычно показывает изменения транзиторного осадка мочи. Больные геморрагическим васкулитом имеют повышенную свертываемость крови. Поэтому для контроля динамики лечения необходимо время от времени выполнять общий анализ крови. Таким образом, лабораторная диагностика крови пациента сможет показать специалисту, стала ли кровь пациента более или менее склонной к образованию тромбов.
Стоит отметить, что повышенная свертываемость крови имеет довольно выраженный характер при тяжелом течении заболевания.
Если заболевание пациента имеет волнообразный характер и сопровождается воспалительным поражением почек, то это может служить поводом для проведения иммуннограммы и обнаружения скрытых бактериальных или вирусных инфекций. Обычно у пациентов, особенно в детском возрасте, анализ крови показывает повышенный уровень IgG. При постоянно повторяющихся заболеваниях и воспалениях почек в крови часто бывает повышенное количество криоглобулинов и циркулирующих иммунных комплексов.
Биохимический анализ крови при геморрагическом васкулите целесообразно применять, только если у пациента имеются симптомы болезней почек. В этом случае анализ обычно указывает на высокое содержание калия и азотистых шлаков.
Инструментальные методы исследования
При показаниях специалист может назначить больному проведение ЭКГ.
ЭКГ – это метод инструментального исследования, при котором на мониторе прибора отражаются характер работы сердца.
Довольно часто для уточнения диагноза врачи советуют пройти больным рентгенографию грудной клетки.
Рентгенография – еще один инструментальный метод исследования, при котором специалист фотографирует различные органы и части тела пациента с помощью рентгеновых лучей и таким образом получает проекционное изображение нужной области на бумаге или диске. Кроме этого может понадобиться выполнение УЗИ органов брюшной полости и почек.
УЗИ – это неинвазивный инструментальный метод диагностики, при котором врач осматривает внутренние органы пациента благодаря использованию ультразвуковых волн.
У детей врачи часто выполняют нефросцинтиграфию. Так как у пациентов детского возраста крайне редко встречаются заболевания почек, то обнаружение при данном методе обследования каких-либо нарушений может указывать на наличие у пациента геморрагического васкулита. Однако данная методика применяется не только для диагностики геморрагического васкулита. Нередко ее применяют для контроля динамики лечения и дальнейшего прогнозирования течения болезни.
Если в ходе лечения иммунная система пациента все равно продолжает атаковать ткани собственных почек, врач может назначить проведение биопсии почки.
Биопсия – это метод диагностики, при котором врач отщипывает кусочек ткани исследуемого органа и изучает его под микроскопом, является одним из наиболее эффективных методов диагностики многих серьезных заболеваний.
Дифференциальная диагностика геморрагического васкулита
Во время диагностики геморрагического васкулита важно отличить данное заболевание от других патологий, которые также могут сопровождаться высыпаниями на кожных покровах, например, от некоторых заболеваний печени, инфекционных болезней, болезней лимфатической системы, почек и суставов, а также злокачественных новообразований.
Если у пациента на теле присутствует мелкая обильная сыпь, то врач может заподозрить у него наличие тромбоцитопинической пурпуры. Тем не менее, при геморрагическом васкулите сыпь обычно локализуется только в определенных местах (преимущественно в области ягодиц и нижних конечностей), при этом в крови не снижается уровень тромбоцитов.
Абдоминальный синдром, который часто сопровождает геморрагический васкулит очень важно отличить от заболеваний брюшной полости требующих срочного лечения. К таким относятся: прободная язва, аппендицит, нарушение проходимости кишечника и язвенных поражений стенок толстого кишечника.
При геморрагическом васкулдите у пациентов также образуется черный кал с неприятным запахом, у них могут возникать схваткообразные боли в животе и рвота с примесью крови. Однако помимо этого у них также присутствуют признаки поражения суставов, и имеется характерная сыпь на теле. Именно по этой причине при поступлении в больницу пациентов с заболеваниями острого живота врач может осматривать их на наличие кожных высыпаний, проверять на артрит и воспалительные процессы в почках.
Если у пациента произошло тяжелое поражение тканей почек, то врач может заподозрить у него наличие заболеваний, при которых происходит поражение гломерул. В этом случае, чтобы убедится в наличии геморрагического васкулита, понадобиться анализ крови или проведение инструментальных методов исследования.
Если у больного все же имеются тяжелые заболевания почек, то врач обычно интересуется, не было ли у его пациента геморрагического васкулита в детстве.
В то же время болезни почек следует отличать от идиопатической возвратной макрогематурии, которая часто повторяется несмотря даже на агрессивное лечение.
Дифференциальная диагностика геморрагического васкулита от других заболеваний суставов обычно не вызывает сложностей. Исключением в этой ситуации может быть системная красная волчанка. Хотя в этом случае в крови пациента обнаруживаются иммунные маркеры, не присущие геморрагическому васкулиту.
Исходя из всего этого, можно понять, что поставить самостоятельно в домашних условиях такой диагноз как геморрагический васкулит невозможно. Это связано в первую очередь с тем, что данная патология может иметь схожие симптомы и с некоторыми другими патологиями. Именно поэтому даже опытные врачи при диагностике геморрагического васкулита вынуждены прибегать к лабораторным и инструментальным способам исследования.
Только если диагноз будет поставлен правильно, лечение пациента пройдет максимально быстро, легко и результативно. Из этого следует, что лечение геморрагического васкулита в домашних условиях ни в коем случае не должно проводиться без консультации специалиста.
Лечение
Фото: fortitechpremixes.com
В современной медицине применяется, как правило, комплексный подход к лечению геморрагического васкулита у взрослых и детей (диета, медикаментозное лечение, постельный режим).
Лечение у взрослых, которое назначается людям, страдающим от геморрагического васкулита имеет ряд особенностей и рекомендаций.
Целью лечения как у взрослых, так и у детей является восстановление естественного функционирования, пораженных геморрагическим васкулитом, органов и вообще всего иммунитета, чего можно добиться только комплексным лечением. Отказываться от лечения геморрагического васкулита строго запрещено.
Для того чтобы понять как лечить геморрагический васкулит у взрослых, что можно употреблять в пищу при данном заболевании, рекомендуется обратиться к специалисту, который занимается профилактикой и лечением данного заболевания. К лечению геморрагического васкулита, как у взрослых, так и у детей стоит подойти со всей ответственностью и серьезностью.
Очень часто пациенты не знают, к какому врачу обратиться с проблемой геморрагического васкулита, как он лечится, какое лечение наиболее эффективно. Консультациями по лечению такого заболевания, как геморрагический васкулит у взрослых и детей, как и собственно лечением самого заболевания (геморрагического васкулита), занимается врач-ревматолог, который в результате осмотра, выпишет соответственные рекомендации и назначит определенный план лечения.
Все люди, у которых открылся геморрагический васкулит кожной формы, должны быть в обязательном порядке госпитализированы, чтобы пройти курс лечения. Лечение у взрослых может затянуться, однако, стоит запастись терпением. Запускать геморрагический васкулит нельзя, это чревато еще более сложными заболеваниями, которые с большим трудом поддаются лечению.
Когда лечение назначено, и человек, страдающий геморрагическим васкулитом госпитализирован, он должен придерживаться некоторых правил, сопровождающих лечение заболевания, которые устанавливает врач:
- При лечении геморрагического васкулита необходимо избегать излишней нагрузки на ноги и их переохлаждения. Тогда время лечения заметно сократится.
- Во время лечения геморрагического васкулита у взрослых и детей нужно исключить все вакцинации и прививки. Лечение данной патологии и параллельное проведение плановых и неплановых вакцинаций недопустимы.
- Пациентам, проходящим курс лечения, противопоказаны многие лекарственные препараты. Запрещено у взрослых и детей:
Лечение иных заболеваний, одновременно с геморрагическим васкулитом антибиотическими средствами;
- лечение (или профилактика) витаминами;
- лечение сульфаниламидами;
- лечение аминокапроновыми кислотами;
- лечение препаратами, содержащими кальций, и многими другими.
Из-за того, что многие препараты противопоказаны при геморрагическом васкулите, заниматься лечением заболевания самостоятельно не стоит, это очень опасно!
При лечении геморрагического васкулита у взрослых и детей вся инфицированная (геморрагическим васкулитом) поверхность должна быть тщательно обработана. Лечение антибиотиками назначает врач на основании серьёзных на то причин, когда геморрагический васкулит не поддается иному лечению.
Если при возникновении геморрагического васкулита синхронно или друг за другом развиваются несколько его серьёзных синдромов, не поддающихся стандартному лечению, то это служит серьезным основанием для назначения индивидуального метода лечения. Как будет лечиться каждое из них, тоже решается врачом в индивидуальном порядке.
Если геморрагический васкулит у взрослых протекает тяжело и плохо поддается лечению, когда геморрагический васкулит у взрослых кожной формы сопровождается ярко выраженной интоксикацией, которая тоже нуждается в лечении, врачи могут выписать рекомендации к проведению пациенту плазмафереза. В процессе проведения процедуры происходит лечение посредством очищения крови от вредоносных токсинов, которое несет в себе геморрагический васкулит. Лечение у взрослых таким методом является очень действенным и результативным. Геморрагический васкулит постепенно будет сходить, что можно будет заметить по результатам.
Следование рекомендациям врача по особой диете при геморрагическом васкулите у взрослых и детей является обязательным условием для результативного лечения.
Прежде всего лечение заболевания сконцентрировано на ликвидацию осложнений, спровоцированных геморрагическим васкулитом. Например, лечение, направленное на нормализацию работы желудочно-кишечного тракта, способствующее снижению кислотности. Еще более строгая диета назначается при таком осложнении геморрагического васкулита, как нарушение функционирования желудка. Лечение посимптомно часто применяется при работе с пациентами, страдающими геморрагическим васкулитом.
В качестве дополнительного лечения у взрослых при геморрагическом васкулите могут быть выписаны следующие процедуры:
- лечение массажем;
- лечение посредством особых упражнений.
Такими методами геморрагический васкулит лечится как дополнение к основной терапии.
Люди, страдающие геморрагическим васкулитом, могут доверить лечение массажем только опытному специалисту. Это даст дополнительную гарантию того, что лечение будет эффективным.
Геморрагический васкулит. Операбельное лечение
В некоторых случаях лечение может потребовать хирургического вмешательства. Такие меры применяются при запущенных и тяжелых случаях геморрагического васкулита у взрослых, при неэффективности лечения медикаментозным способом.
В подавляющем большинстве случаев геморрагический васкулит поддается лечению консервативным (стандартными) методами. Геморрагический васкулит нуждается в хирургическом лечении исключительно в случаях тяжелых форм заболевания и возникающих на их фоне осложнений, которые не поддаются иному лечению.
Существуют несколько видов васкулита:
Специального лечения против геморрагического васкулита, как у взрослых так и у детей на сегодняшний день не разработано. В период обострения заболевания требуется «железное» следование всем рекомендациям врача, особенно – соблюдению постельного режима и диеты.
Особое значение при лечении геморрагического васкулита, как у взрослых, так и у детей врачи придают специально предусмотренной для этих случаев диете.
Лечение геморрагического васкулита. Диета.
Соблюдение особой диеты является очень важной стадией комплексного лечения геморрагического васкулита как у взрослых, так и у детей. Диета в лечении данного заболевания стоит на первом месте.
При лечении таких признаков геморрагического васкулита, как расстройство желудка, жидкий стул, кровотечение в кишечнике у взрослых рекомендовано назначение диеты, согласно столу №1, у детей – диета № 5. Что можно употреблять в пищу и основной список продуктов, который входит в диету, стоит дополнительно обговорить с врачом.
Итак, в период лечения геморрагического васкулита у взрослых и детей любому пациенту необходима щадящая для желудочно-кишечного тракта диета. Из рациона больного нужно убрать те продукты, в состав которых входят аллергенные компоненты. Лечение без диеты не даст результатов.
Диета необходима и после пройденного лечения. В реабилитационный период геморрагического васкулита у взрослых и детей диета подразумевает исключить из рациона пациента определенный список продуктов. Для плодотворного лечения пищу необходимо варить, тушить, парить, запекать (без добавления масла), употребление соли свести к минимуму – стандартная диета без жирного. Геморрагический васкулит «не терпит» ничего жареного, жирного и острого.
Список продуктов, запрещенных диетой при геморрагическом васкулите:
- какаосодержащие продукты и само какао;
кофесодержащие продукты и сам кофе;
шоколад и батончики из него;
шоколадные конфеты;
цитрусовые;
ягоды, овощи и фрукты красного цвета;
куриные яйца.
После того, как посредством лечения, достигнута ремиссия геморрагического васкулита, пациенту надлежит в течение года соблюдать антиаллергенную диету (такой период ремиссии должен быть как у взрослых, так и у детей), постепенно сужая список продуктов, запрещенных диетой.
Схему питания и список продуктов в период ремиссии геморрагического васкулита врачи подбирают субъективно для каждого из пациентов, учитывая методы лечения, проявления геморрагического васкулита и особенности анамнеза.
Заключение
Итак, лечение геморрагического васкулита как у взрослых, так и у детей происходит в условиях специально подобранной (антиаллергенной) диеты и строгого соблюдения рекомендованного врачом, постельного режима. Когда пациенту лечат геморрагический васкулит, специалисты, как правило, отменяют лекарственные препараты, которые могли явиться причиной зарождения заболевания или которые могли теоретически его спровоцировать.
Также лечение геморрагического васкулита у взрослых и детей предусматривает некоторое ограничение к двигательной активности пациента. Иногда больному геморрагическим васкулитом при лечении будет показан постельный режим в течение трех-четырех недель. Если во время лечения пациент нарушит рекомендации врача (даже относительно постельного режима), у него может наступить вторичная волна геморрагического васкулита с еще большим количеством раздражающих кожу высыпаний, квалифицируемая специалистами, как ортостатическая пурпура.
Прогнозы по лечению геморрагического васкулита у взрослых и детей врачи ставят благоприятные. Отвечая на вопрос: «Как лечить геморрагический васкулит?» они подчеркивают, что лечение геморрагического васкулита будет теме эффективнее, чем раньше было обращение за медицинской помощью. Пренебрежение лечением, диетой чревато серьезными проблемами, ведь геморрагический васкулит опасен осложнениями.
Очень важно помнить о том, что:
- геморрагический васкулит нуждается в лечении,
- необходимо воздерживаться от самостоятельного лечения геморрагического васкулита;
- за помощью по лечению геморрагического васкулита нужно при первых его первых признаках.
- лечение геморрагического васкулита необходимо доверять только квалифицированным специалистам.
- при лечении заболевания очень важно соблюдать диету.
- профилактика геморрагического васкулита у взрослых и детей включает в себя своевременное его выявление, 2 раза в год стоит соблюдать очищающую диету, проходить лечение инфекций вовремя.
Лекарства
Фото: opt-611422.ssl.1c-bitrix-cdn.ru
Лечение геморрагического васкулита представляется ограничением продуктов питания, имеющих возможные аллергены, в случаях с абдоминальными формами необходимо по возможности придерживаться голода в течение 2–4 дней. Однако ключевую роль играет консервативное (медикаментозное) лечение, без которого никогда не удаётся вылечить геморрагический васкулит. Лекарства, применяемые для его лечения можно разделить на несколько групп:
- Прямые антикоагулянты.
- Антиагреганты.
- Препараты сульфонового (противолепрозные) ряда в комбинации.
- Антигистаминные препараты (как в форме мази, так и внутрь).
- Нестероидные противовоспалительные средства.
- Глюкокортикостероиды.
Антикоагулянты, применяемые при геморрагическом васкулите
Применяются преимущественно прямые антикоагулянты, которые делятся на 2 группы:
- Гепарин — нефракционированный.
- Низкомолекулярные гепарины — препараты низкомолекулярного гепарина (ПНГ): фраксипарин, фрагмин.
Гепарин (НГ) — это кислый мукополисахарид, усиливающий действие антитромбина III (дальше идёт инактивация тромбина). Таким образом, гепарин и антитромбин III действуют всегда совместно, одним комплексом. Гепарин не всасывается в ЖКТ, поэтому применяется парентерально (внутривенно или подкожно).
При геморрагическом васкулите рекомендуется первоначально вводить 2500–5000 единиц 2–4 раза в сутки, всего 5–7 дней.
Низкомолекулярные гепарины (ПНГ), в отличие от нефракционированного гепарина, слабее действуют на тромбин, но очень сильно ингибируют фактор Xa. Также, ПНГ действуют в 2 раза дольше и назначаются 1–2 раза в день. При подкожном введении обладают большей биодоступностью.
Антиагреганты при геморрагическом васкулите
Их можно подразделить на несколько групп:
- Ингибиторы циклооксигеназы.
- Ингибиторы фосфодиэстеразы.
- Блокаторы рецепторов АДФ.
- Антагонисты рецепторов IIb/IIIA.
Ингибиторы циклооксигеназы многочисленные в своём роде не обладают достаточными антиагрегантными свойствами. Только ацетилсалициловая кислота (аспирин) в малы дозах (70–325 мг/д) ингибирует циклооксигеназу необратимо, что снижает синтез тромбоксана А2 и тем самым тормозят агрегацию.
При геморрагическом васкулите оптимальная доза аспирина составляет 75 мг один раз в день — утром.
Ингибиторы фосфодиэстеразы, в частности дипиридамол (курантил), тормозят агрегацию тромбоцитов путём блокирования фосфодиэстеразы и захвата аденозина, что увеличивает содержание ц-АМФ и ц-ГМФв тромбоцитах. Применяется обычно в сочетании с аспирином или непрямыми антикоагулянтами (варфарин). При геморрагическом васкулите дозой выбора дипиридамола является 75 мг 2–3 раза в день.
Блокаторы рецепторов АДФ, к которым относятся такие препараты как тиклопидин и клопидогрел, тормозят агрегацию за счёт необратимого блокирования АДФ-рецепторов в тромбоцитах. Важно отметить, что они применяются в тех случаях, когда противопоказано назначать аспирин. Применяются при геморрагическом васкулите в дозировке 0,2 г — 3 раза в день. Клопидогрел предпочтительнее ввиду меньшей вероятности побочных эффектов.
Антагонисты рецепторов (рецепторного комплекса гликопротеинов) IIb/IIIa назначаются только парентерально (внутривенно). К этой группе относятся абциксимаб (или реопро), тирофибан. Назначаются в течение 4 недель, при сопутствующих нефритах могут назначаться до 6 месяцев.
Противолепрозные препараты (сульфоновый ряд) при геморрагическом васкулите.
Назначается дапсон в дозировке 50–75 мг 2 раза в день совместно с тренталом в дозировке 400 мг 3 раза в день. Терапия проводится циклически (5 дней) с однодневным перерывом между ними до того момента, пока не исчезнут симптомы васкулита. Эффект от такой терапии достаточно высокий.
Антигистаминные препараты при геморрагическом васкулите.
Как правило, они применяются при кожном зуде, причиной которого является геморрагический васкулит. Мазь, содержащая антигистаминные компоненты, применяется местно (локально) на зудящие места. Чаще всего применяются тавегил по 1 мг два раза в день — в утреннее и вечернее время, или супрастин по 25 мг 3 раза в день.
НПВС при геморрагическом васкулите.
Эта группа применяется при сильном воспалении и высокой температуре, сопровождаемых выраженными суставными болями. Применяется диклофенак по 25 мг 3 раза в день, индометацин в такой же дозировке 3 раза в день.
Глюкокортикостероиды при геморрагическом васкулите применяются в случае неэффективности НПВС либо совместно с цитостатиками при некоторых гломерулонефритах. Преднизолон применяется из расчёта 0,5 мг на 1 кг массы тела в течение 5–7 дней. Затем делается перерыв на 5 дней.
Лечение народными средствами не оправдывает себя по той причине, что многие растения являются аллергеном для человека с геморрагическим васкулитом и лишь осложнят течение болезни. Важно помнить, что самолечение может привести к печальным последствиям! Всегда следует обратиться к врачу.
Народные средства
Фото: healthstone.site
Лечение геморрагического васкулита народными средствами приносит пользу только после обязательного разрешения врача. Он рекомендует своим пациентам многие эффективные способы борьбы с этой патологией. Рассмотрим подробнее некоторые методы народного лечения геморрагического васкулита.
Фитосборы для борьбы с болезнью
Если больному установлен диагноз «геморрагический васкулит», то ему рекомендовано делать такие сборы из лекарственных растений.
Для приготовления такого сбора смешайте в равных пропорциях следующие компоненты:
- плоды японской софоры;
- соцветия бузины;
- тысячелистник;
- спорыш;
- листья крапивы.
Все компоненты надо старательно измельчить, перемешать. Для приготовления настоя рекомендуется взять столовую ложку смеси, залить ее кипящей водой и настоять один час. Рекомендуется выпить стакан такого настоя за два приема в течение суток.
Схемы очищения кишечника
Если у пациента диагностирован геморрагический васкулит, лечение народными средствами должно сочетаться с очищением кишечника. Для регулирования деятельности органов пищеварительного тракта успешно применяются такие лекарственные травы:
- девясил;
- бессмертник;
- полынь;
- пижма.
Для получения настоя рекомендуется перемешать в равных пропорциях указанные травы и добавить в литр кипящей воды две ст. л. растительной смеси. Ее надо настаивать два часа, желательно в термосе. Процеженный и охлажденный настой пьют по полстакана за полчаса до еды. Необходимо выпить такой настой за два приема.
Очищение крови
Для того чтобы очистить кровь, рекомендуют применять толстолистный бадан. Высушенные листья растения добавляются в стакан кипятка и настаивают в термосе. Это лекарство надо выпивать утром натощак со столовой ложкой меда.
Больным на заметку
Страдающим геморрагическим васкулитом желательно выполнять такие рекомендации:
- полезно принимать препараты витамина К, а также травы и продукты, содержащие это вещество;
- полезно есть черную смородину;
- больным рекомендуется употреблять зеленый чай, обладающий антиоксидантными свойствами;
- настойка болиголова также приносит пользу для сосудов, однако, ввиду ее ядовитости следует тщательно выполнять рекомендации врача.
И самый главный совет: перед тем, как начать лечение геморрагического васкулита народными способами, рекомендуется посоветоваться с терапевтом.
Информация носит справочный характер и не является руководством к действию. Не занимайтесь самолечением. При первых симптомах заболевания обратитесь к врачу.Васкулит:,, | doc.ua
Как правило, встречается васкулит у детей и подростков. Взрослые люди, равно как и представители преклонного возраста, в зону риска заболевания васкулитом попадают очень и очень редко. В целом, васкулит классифицируется как аллергическое заболевание и делится на две категории: первичный и вторичный.
Первичный васкулит — это самостоятельное проявление болезни, причины и симптомы которой мы рассмотрим ниже. Вторичный — когда васкулит становится одним из симптомов какого-либо кожного заболевания, связанного с иммунной системой: это может быть сифилис, скарлатина или гепатит.
Причины
Васкулит, причины которого выявить сложно, является опасным заболеванием. От этого могут возникнуть и некоторые трудности с лечением, так как врач должен обладать достоверной информацией о том, что вызвало васкулит, чтобы процесс лечения пошел во благо, а не во вред. Кстати, именно медикаменты в некоторых случаях и являются возбудителем болезни, поэтому на вопрос врача «Есть ли у вас аллергия на препарат?» не стоит отвечать наугад.
В других случаях, причиной возникновения васкулита могут быть вирусы кожных заболевания. Это, как раз, и есть вторичная категория. Чаще всего, это гепатит.
Более тяжелый случай — когда иммунная система не воспринимает ткани кровеносных сосудов как родные и начинает вести с ними борьбу, ошибочно идентифицируя их как чужеродное тело.
Еще одна из причин, по которой васкулит может развиваться, причем с самых ранних лет, — это наследственность. Заболевание не обязательно проявится сразу, однако предрасположенность имеет место быть.
Симптомы
Если сосуды поразил васкулит, симптомы его определить бывает непросто. Заболевание настолько коварно, что на протяжении долгого времени человек может думать, что болеет чем-то другим, совершенно неопасным. Подклассификаций васкулита невероятно много, а симптомы напрямую зависят от того, какая именно из зон поражена. Но все же, некоторые общие проявления выделить можно. Это сыпь, зуд, слабость, боль в суставах, лихорадка, потеря аппетита и как следствие — истощение.
Геморрагический васкулит, лечение которого нужно начать незамедлительно (за счет того, что его распознать легче, нежели другой), сопровождается подкожными кровоизлияниями. Пораженные капилляры выступают в виде неровных красных пятен на коже.
Аллергический васкулит характерен похожими симптомами, однако может уходить глубже, поражая нервную систему или кровеносные сосуды мозга, что впоследствии может привести к инсульту и даже инфаркту.
Системный васкулит может проявляться по-разному. Ответвлений у него — более чем достаточно. Например, гранулематоз Вегенера может быть похож по проявлениям на гайморит или отит. Эозинофильный ангиит очень похож на астму, а височный артериит походит на обыкновенную мигрень — распознать его можно, если вы начинаете замечать ухудшение зрения.
Осложнения
Чем дольше вы не обращаете внимания на болезнь, тем более уязвимым становится организм. Постепенно он начинает сдаваться, и процесс разлада происходит все быстрее.
Если поражена зона легких, человек находится на пути к пневмонии, инфаркту легкого, гипертензии, пневмосклерозу. Сердце подвержено инфаркту миокарда, стенокардии, поражению мышц (это значит, сердце не сможет сокращаться в нормальном порядке) и миокардиосклерозу. Осложнения, связанные с желудочно-кишечным трактом, проявляются в виде острого хронического панкреатита, увеличения печени, селезенки, тромбозе брыжеечных сосудов и так далее. Что же качается нервной системы, от этого, прежде всего, страдает мозг.
Диагностика
Для того, чтобы самостоятельно диагностировать у себя васкулит, первых проявлений в виде пятен (даже на самой здоровой коже) — вполне достаточно. Точный диагноз вам может поставить только грамотный врач-гематолог. Если этого не сделать, не узнать причины заболевания и его точную классификацию, то назначить правильное лечение будет попросту невозможно. Обследование включает в себя процедуру биопсии, а именно — определение антител к цитоплазме нейтрофилов в сыворотке крови. Таким образом, можно не просто поставить диагноз со стопроцентной точностью, но и сказать наверняка, вернется болезнь или нет. Если в клинике вам предлагают несколько вариантов (в зависимости от ценовой категории), наиболее верным решением будет остановиться именно на АНЦА.
Лечение
При постановке диагноза васкулит, лечение могут совместно проводить хирурги, окулисты, невропатологи, терапевты, отоларингологи, нефрологи и другие специалисты, которые будут наблюдать за и внутренними повреждениями и влиянием выписанных препаратов. В процессе лечения, в первую очередь, снимается воспаление, чтобы картина заболевания стала четче. Затем подавляется иммунитет, чтобы враждебно настроенная система больше не оказывала сопротивление кровеносным сосудам. Последний этап — улучшение кровотока.
Чем опасен васкулит фигуристки Слуцкой
Бывшая фигуристка Ирина Слуцкая призналась, что страдает от васкулита — поражения стенок сосудов. С чем связано это заболевание, какие возможны осложнения и как держать его под контролем, рассказывает «Газета.Ru».
Бывшая фигуристка Ирина Слуцкая сообщила, что страдает от васкулита. Сохранить карьеру ей помог длительный и трудный курс лечения.
«У меня еще сложнейшее заболевание, после которого спасибо, что я выжила, потому что иногда эти заболевания заканчиваются летальным исходом. Те препараты, которые я принимала, — с ними тяжело держать себя. Это был героизм. Я не скрываю этого. И я собой в первую очередь горжусь. Горжусь, что смогла преодолеть невзгоды. Даже на приеме гормональных препаратов я себя очень жестко держала и была в одном весе», — отметила чемпионка.
Системные васкулиты — группа заболеваний, характеризующихся воспалением сосудистой стенки.
Это приводит к ишемическим изменениям органов и тканей, кровоснабжающихся соответствующими сосудами, проявления васкулита зависят от типа, размера, локализации пораженных сосудов и активности системного воспаления. Этиология большинства первичных васкулитов неизвестна. Предполагается, что многие микроорганизмы могут привести к воспалению сосудов, но только некоторые формы васкулита у отдельных больных удается четко связать с определенными факторами — лекарственная гиперчувствительность, вирусы гепатита В, С и т. п. Также при развитии ряда форм доказана роль наследственности.
Васкулиты относятся к числу наиболее тяжелых форм хронической патологии человека. Их распространенность колеблется от 0,4 до 14 и более случаев на 100 тыс. населения. Эпидемиологические исследования показывают, что распространенность васкулитов постепенно увеличивается.
Полагают, что в возникновении васкулита одновременно участвуют несколько иммунных, а возможно, и неиммунных патологических процессов. Большое внимание уделяется антинейтрофильным цитоплазматическим антителам (АНЦА) — аутоантителам, реагирующим с различными ферментами цитоплазмы нейтрофилов. Связанные с ними васкулиты относятся к редким жизнеугрожающим состояниям и при отсутствии иммуноподавляющей терапии приводят к смерти пациента.
Опасность васкулита заключается в возможности развития серьезных осложнений.
В особо тяжелых случаях, когда часть кровеносного сосуда вытягивается и расширяется, увеличивается вероятность образования аневризмы — выпяченного участка стенок. Опасность этого патологического процесса заключается в разрыве аневризмы, который может вызвать множество необратимых последствий: от нарушений кровообращения до летального исхода. В частности, от разрыва аневризмы аорты скончался 9 мая журналист, главный редактор радиостанции «Говорит Москва» Сергей Доренко.
В случае противоположного поведения сосудов при васкулите, когда воспаление способствует их сужению, есть вероятность прекращения кровоснабжения отдельных органов и тканей. Если альтернативные кровеносные сосуды не смогут обеспечить поступление к ним крови в необходимом количестве, то может произойти омертвение пораженных тканей или органов.
Васкулиты принципиально подразделяются на первичные — вызванные воспалением самих сосудов, и вторичные — при которых воспаление сосуда является реакцией на другое заболевание.
Васкулиты классифицируются в зависимости от поражаемых сосудов — васкулиты крупных сосудов, сосудов среднего размера, мелких сосудов, поражающие сосуды различных размеров. Также есть васкулиты отдельных органов. Всего насчитывается более 25 различных форм болезни.
Геморрагический васкулит — наиболее распространенный из них, он встречается примерно у 140 человек из миллиона. В его основе лежит асептическое воспаление стенок микрососудов, множественное микротромбообразование, поражающее сосуды кожи и внутренних органов, чаще всего почек и кишечника. Главная его причина — циркуляция в крови иммунных комплексов и активированных компонентов системы комплемента, ферментной системы, защищающей организм от чужеродных агентов.
В здоровом организме иммунные комплексы выводятся из организма специальными клетками — клетками фагоцитарной системы. Чрезмерное накопление циркулирующих иммунных комплексов в условиях преобладания антигенов или при недостаточном образовании антител приводит к отложению их на внутреннем слое сосудов с вторичной активацией белков системы комплемента и изменении сосудистой стенки.
У большинства больных (66-80%) развитию заболевания предшествует инфекция верхних дыхательных путей. Также возможно его развитие после тифа, кори, желтой лихорадки. Другими потенциальными «спусковыми крючками» могут стать прием лекарств, пищевая аллергия, укусы насекомых, переохлаждение.
Чаще всего болезнь поражает кожу (образуется выраженная сыпь) и суставы.
Для лечения используются антикоагулянты, кортикостероиды, иммунодепрессанты. Также необходимо соблюдать постельный режим и отказаться от аллергенных продуктов.
Как правило, геморрагический васкулит протекает доброкачественно. Обычно болезнь заканчивается спонтанной ремиссией или полным выздоровлением в течение 2-3 недель от момента появления первых высыпаний на коже. В некоторых случаях болезнь приобретает рецидивирующее течение. Возможны тяжелые осложнения, обусловленные поражением почек или кишечника.
Среди пожилых женщин наиболее распространен гигантоклеточный артериит — воспалительное поражение крупных и средних артерий. Заболевание начинается с повышения температуры, причем температура может быть как субфебрильной, так и высокой. Пациент чувствует слабость, теряет аппетит и, как следствие, вес. Заболевание сопровождается сильными головными болями, депрессией и нарушением сна.
Характерный симптом, который, впрочем, наблюдается не у всех больных — острые боли в области языка и жевательных мышц. Возникают они при разговоре или во время еды. Они такие сильные, что человеку необходимо прекратить жевать или говорить.
В стенках артерий развивается воспаление, которое приводит к образованию специфических гигантских клеток. Через некоторое время стенки артерии уплотняются, утолщаются, просвет сосуда сужается. Кроме того, в пораженной артерии могут развиваться пристеночные тромбы. Все это способствует нарушению притока крови к органу, который питает пораженная артерия. Обескровленный орган не может функционировать в нормальном режиме.
Наиболее эффективный способ лечения на сегодняшний день — прием кортикостероидов.
Симптоматика других васкулитов разнообразна.
Для узелкового периартерита, поражающего в основном мужчин, характерны боли в мышцах, повышение температуры, снижение массы тела.
При гранулематозе Вегенера появляются боли в околоносовых пазухах, гнойные или кровянистые выделения из носа, язвы на слизистой носа, разрушение носовой перегородки, а также почечная недостаточность, боли в грудной клетке, кровавый кашель.
Наиболее важный признак синдрома Бехчета — рецидивирующий стоматит. Второй по частоте признак — язвы на мошонке и половом члене у мужчин, влагалище и наружных половых органах у женщин. Также развиваются различные воспаления глаз.
При неспецифическом аортоартериите больные жалуются на онемение и боли в конечностях, спине и животе, обмороки и нарушения зрения.
Для диагностики используются анализы крови и мочи, исследование сосудов, флюорография. В качестве лечения используются в основном иммунодепрессанты, антикоагулянты, противовоспалительные препараты. Остальные лекарства зависят от вида заболевания. При лечении васкулитов необходима слаженная работа терапевтов, нефрологов, отоларингологов, невропатологов, хирургов, окулистов и других врачей.
Вылечить васкулит нельзя, но при правильно подобранной терапии большинство пациентов могут контролировать заболевание.
Прогноз заболевания зависит не только от типа и степени повреждения кровеносных сосудов, но и продолжительности заболевания до начала лечения, а также от реакции на лечение. Риск повреждения органов и систем организма связан с длительностью и интенсивностью заболевания. Повреждение жизненно важных органов может привести к тяжелым последствиям на всю жизнь.
В большинстве случаев можно добиться ремиссии в течение первого года лечения. Период ремиссии может продолжаться всю жизнь, но, как правило, для этого требуется долгосрочное лечение. Периоды ремиссии могут прерываться из-за обострения васкулита, когда пациент нуждается в усиленной терапии. При отсутствии лечения вероятность летального исхода высока. Васкулит является редким заболеванием, поэтому существует мало данных о долгосрочном прогнозе.
Синдром системной капиллярной утечки — Симптомы и причины
Обзор
Синдром системной утечки капилляров — редкое заболевание, характеризующееся повторяющимися вспышками массивной утечки плазмы из кровеносных сосудов в соседние полости и мышцы тела. Это приводит к резкому падению артериального давления, которое, если его не лечить, может привести к органной недостаточности и смерти.
Это состояние, также называемое болезнью Кларксона, может быть ошибочно принято за тяжелые реакции на широко распространенные инфекции (септический шок) или тяжелые аллергические реакции (анафилактический шок).Приступы могут быть спровоцированы инфекцией верхних дыхательных путей или сильными физическими нагрузками. Частота приступов может варьироваться от нескольких в год до единичного случая за всю жизнь.
Продукты и услуги
Показать больше продуктов Mayo ClinicСимптомы
Приступам синдрома системной капиллярной утечки часто предшествуют один-два дня появления одного или нескольких неспецифических симптомов, которые могут включать:
- Раздражительность
- Усталость
- Боль в животе
- Тошнота
- Мышечные боли
- Повышенная жажда
- Внезапное увеличение массы тела
По мере того, как жидкость вытекает из кровотока, объем крови и артериальное давление падают.Это может лишить ткани почек, мозга и печени кислорода и питательных веществ, необходимых для нормальной работы.
Лечение синдрома системной утечки капилляров в клинике Мэйо
14 ноября 2020 г.
Показать ссылки- Синдром системной утечки капилляров. Информационный центр по генетическим и редким заболеваниям. https: // rarediseases.info.nih.gov/diseases/1084/systemic-capillary-leak-syndrome. По состоянию на 12 октября 2017 г.
- Анея Р. Идиопатический синдром системной утечки капилляров. https://www.uptodate.com/contents/search. По состоянию на 12 октября 2017 г.
- Druey KM, et al. Синдром идиопатической системной утечки капилляров (болезнь Кларксона). Журнал аллергии и клинической иммунологии. 2017; 140: 663.
- Kapoor P, et al. Синдром идиопатической системной утечки капилляров (болезнь Кларксона): опыт клиники Мэйо.Труды клиники Мэйо. 2010; 85: 905.
- Коричневый AY. Allscripts EPSi. Клиника Мэйо, Рочестер, Миннесота, 30 августа 2017 г.
Связанные
Продукты и услуги
Показать больше продуктов и услуг Mayo ClinicСиндром системной капиллярной утечки
Синдром капиллярной утечки: этиология, патофизиология и лечение
При различных заболеваниях человека увеличение проницаемости капилляров для белков приводит к потере богатой белками жидкости из внутрисосудистого в интерстициальное пространство.Хотя сепсис является заболеванием, наиболее часто связанным с этим явлением, многие другие заболевания могут приводить к «сепсисоподобному» синдрому с проявлениями диффузного точечного отека, экссудативных серозных полостей, некардиогенного отека легких, гипотонии и, в некоторых случаях, гиповолемии. шок с полиорганной недостаточностью. Термин «синдром утечки капилляров» использовался для описания этой совокупности проявлений заболевания, связанных с повышенной проницаемостью капилляров для белков. Другие заболевания, помимо сепсиса, которые могут привести к синдрому утечки капилляров, включают синдром идиопатической системной утечки капилляров или болезнь Кларксона, синдром приживления трансплантата, синдром дифференцировки, синдром гиперстимуляции яичников, гемофагоцитарный лимфогистиоцитоз, вирусные геморрагические лихорадки, аутоиммунные заболевания, отравление змеиным укусом и отравление ритуалом.Лекарства, включая некоторые интерлейкины, некоторые моноклональные антитела и гемцитабин, также могут вызывать синдром утечки капилляров. При всех этих заболеваниях обычно наблюдается острое повреждение почек. Помимо гипотензии, цитокины, вероятно, играют важную роль в патофизиологии острого повреждения почек при синдроме утечки капилляров. Управление жидкостями — важная часть лечения синдрома утечки капилляров; гиповолемия и гипотензия могут вызвать повреждение органа, тогда как капиллярная утечка вводимой жидкости может усугубить отек органа, что приведет к прогрессирующему повреждению органа.Цель этой статьи — обсудить другие заболевания, помимо сепсиса, которые вызывают утечку капилляров, а также рассмотреть их общую патофизиологию и лечение.
Ключевые слова: острая травма почек; синдром утечки капилляров; проницаемость капилляров; цитокины.
Синдром идиопатической системной капиллярной утечки (болезнь Кларксона): опыт клиники Мэйо
Резюме
ЦЕЛЬ: Определить клинические особенности, естественный анамнез и исход четко определенной когорты из 25 последовательных пациентов с синдромом идиопатической системной капиллярной утечки ( SCLS) оценивается в центре третичной медицинской помощи.
ПАЦИЕНТЫ И МЕТОДЫ: Были проанализированы записи пациентов с диагнозом SCLS с 1 ноября 1981 г. по 30 апреля 2008 г. Описательная статистика использовалась для анализа демографических данных пациентов, клинических особенностей, осложнений и терапевтических вмешательств.
РЕЗУЛЬТАТЫ: Из 34 пациентов, чьи записи были проанализированы, 25 соответствовали всем диагностическим критериям SCLS. Средний возраст постановки диагноза SCLS составлял 44 года. Среднее время наблюдения за выжившими пациентами составило 4,9 года, а среднее время до постановки диагноза с момента появления симптомов — 1.1 год (межквартильный размах 0,5-4,1 года). О гриппе или миалгии сообщили 14 пациентов (56%) в начале острого приступа SCLS, а рабдомиолиз развился у 9 пациентов (36%). Пациенты с более сильным снижением уровня альбумина имели более высокую вероятность развития рабдомиолиза ( p = 0,03). Моноклональная гаммапатия, преимущественно IgG-κ-типа, была обнаружена у 19 пациентов (76%). Частота прогрессирования множественной миеломы составила 0,7% на человеко-год наблюдения. Общий ответ на различные методы лечения составил 76%, и у 24% пациентов сохранялась стойкая (> 2 лет) полная ремиссия.Расчетная 5-летняя общая выживаемость составила 76% (95% доверительный интервал, 59% -97%).
ЗАКЛЮЧЕНИЕ: Синдром системной утечки капилляров, редкое заболевание, которое встречается у людей среднего возраста, обычно диагностируется после значительной задержки с момента появления симптомов. Степень снижения альбумина во время приступа коррелирует с развитием рабдомиолиза. Снижение частоты и / или тяжести приступов наблюдалось почти у трех четвертей пациентов, которым было предложено эмпирическое лечение.Скорость прогрессирования множественной миеломы сравнима с таковой при моноклональной гаммопатии неустановленного значения.
BM = костный мозг; IQR = межквартильный размах; MGUS = моноклональная гаммопатия неопределенного значения; ММ = множественная миелома; ОС = общая выживаемость; ПК = плазматическая ячейка; SCLS = синдром системной утечки капилляров; VEGF = фактор роста эндотелия сосудов
Синдром идиопатической системной утечки капилляров (SCLS), также известный как болезнь Кларксона и спонтанный периодический отек , является потенциально фатальным заболеванием, характеризующимся стереотипными «атаками» различной интенсивности гиповолемического шока и генерализованный отек в сочетании с гемоконцентрацией (обнаруживаемой по повышенному гематокриту) и гипоальбуминемией, обычно возникающий при отсутствии альбуминурии. 1 Присутствие сывороточного белка М, примечательного признака, является единственной существенной лабораторной аномалией во время фазы покоя между приступами. 2 Хотя точная частота этого заболевания неизвестна, за последние 15 лет был отмечен относительный всплеск числа зарегистрированных случаев, возможно, в результате повышения осведомленности и успешной идентификации пациентов с множеством сложных симптомов и лабораторных исследований. это может быть объединено общим диагнозом идиопатический SCLS. 3,4 Хотя первоначальные сообщения были получены в Соединенных Штатах и Европе, позже случаи заболевания были зарегистрированы по всему миру, включая Индию, Японию и Кувейт. 5-8
Цели нашего исследования состояли в том, чтобы определить клинические особенности, естественное течение и исход четко определенной когорты последовательных пациентов с SCLS и сравнить наши результаты с данными ранее описанных случаев и небольших ретроспективных исследований. .
Путь от первого описания группы симптомов у пациентки до их формального признания клиническим синдромом системной капиллярной утечки поучителен и заслуживает обсуждения.В 1960 году Кларксон и др. 9 описали случай 32-летней женщины с ничем не примечательным семейным анамнезом, которая пережила «странное циклическое заболевание, при котором у нее периодически возникали внезапные массивные движения плазмы из ее сосудистого русла». Заболевание характеризовалось повторяющимися эпизодами отека, гиповолемического шока, гипоальбуминемии, гемоконцентрации и сохранения М-белка в сыворотке крови. 9 За этим первым описанием SCLS через 2 года последовал другой случай 29-летнего мужчины с эпизодами отека, увеличения веса, крапивницы, лихорадки и недомогания, в дополнение к повышенным уровням гамма-глобулина в сыворотке крови, спленомегалией. , и выраженная эозинофилия (50% -70%). 10 Хотя первоначально этот пациент считался похожим на индексный случай, у этого пациента отсутствовала характерная гипотензия, и в конечном итоге у него был диагностирован эпизодический ангионевротический отек с эозинофилией, теперь известный как синдром Глейха . 11,12
Год спустя (1963) И. Вайнбрен 13 предложил термин спонтанный периодический отек вместо циклический отек для этого синдрома у 45-летнего англичанина с повторяющимися приступами отека. это «… развивалось быстро: в течение нескольких часов он почувствовал себя плохо, почувствовал сильную жажду и отвращение к еде.Эти атаки были сопоставимы с теми, что описаны в первоначальном случае Кларксона. Четыре года спустя, в 1967 году, Мелвин Хорвит, один из приглашенных соавторов отчета об индексном случае, написал еще один отчет о фатальном гиповолемическом шоке неизвестной этиологии, в котором результаты вскрытия предполагали диффузный интерстициальный отек, отек легких и серозные выделения. 14 В течение следующих двух десятилетий в медицинской литературе появилось еще только 20 случаев. 15,16
В 1992 и 1999 годах в 2 небольших сериях случаев из нашего учреждения сообщалось об эффективности тербуталина и аминофиллина при лечении этого заболевания. 17,18 В 1997 году более крупное многоцентровое ретроспективное исследование Amoura et al. 19 описало течение SCLS и оценило эффективность доступной терапии в когорте из 13 пациентов.
ПАЦИЕНТЫ И МЕТОДЫ
С одобрения Институционального наблюдательного совета Mayo Clinic, записи всех пациентов, осмотренных в Mayo Clinic в Рочестере, штат Миннесота, с 1 ноября 1981 года по 30 апреля 2008 года с диагнозом SCLS, гиперпроницаемость капилляров. , Болезнь Кларксона и ангионевротический отек с гипоальбуминемией.Диагноз SCLS был основан на недвусмысленных документах о повторяющихся приступах гипотензии, повышенных концентрациях гематокрита, периферических отеках и гипоальбуминемии без альбуминурии. Моноклональная гаммопатия не считалась обязательным критерием, но ее одновременное наличие усиливало диагноз. Пациенты, физические признаки, симптомы и результаты лабораторных исследований которых могут быть объяснены альтернативным диагнозом, исключались, если этот альтернативный диагноз подтверждался дальнейшими исследованиями.
Были включены отчеты лабораторных исследований, полученные во время первого прототипного «приступа» и / или в течение 30 дней после контакта с пациентом. Большинство пациентов лечились в других медицинских центрах; с их согласия данные были извлечены из задокументированных записей направляющих учреждений. Были получены данные последующего наблюдения, и было предпринято как минимум 2 попытки связаться с выжившими пациентами по телефону. Когда это было возможно, пытались определить причину смерти. В рамках ретроспективного обзора мы попытались классифицировать исход болезни в нашей когорте.
Статистический анализ
Описательная статистика и простые графики разброса использовались для анализа демографических данных пациентов, клинических особенностей, осложнений и терапевтических вмешательств. Общая выживаемость (ОС) оценивалась по методу Каплана-Мейера и определялась как время от даты постановки диагноза до смерти или последнего наблюдения. Пациенты, жившие на момент последнего зарегистрированного наблюдения, были подвергнуты цензуре. Знаковые ранговые тесты Вилкоксона использовались для проверки изменений лабораторных параметров во время атаки относительно исходного уровня, а тесты суммы рангов Вилкоксона использовались для проверки связи между изменениями альбумина и концентрацией гематокрита во время приступа относительно исходного уровня и развитием клинических проявлений. осложнения.Все тесты были двусторонними, и все анализы проводились с использованием программного обеспечения SAS, версия 9.1 (Институт SAS, Кэри, Северная Каролина).
РЕЗУЛЬТАТЫ
Из 34 пациентов, чьи записи были проанализированы, 25 соответствовали всем диагностическим критериям SCLS. очерчивает демографический профиль исследуемой когорты. Среднее время между появлением симптомов и окончательным диагнозом составляло 1,1 года (межквартильный размах [IQR], 0,5–4,1 года). У 3 пациентов официальный диагноз был поставлен более чем через 5 лет после появления симптомов (через 5 лет).5, 8,0 и 32,0 года). Среднее количество острых приступов в год составило 3 (IQR, 0,5–5,0 приступов в год).
ТАБЛИЦА 1.
Демография исследуемых пациентов при диагностике SCLS a
Препятствующие факторы
Гриппоподобная болезнь или миалгии у большинства пациентов предвещали кризис, но были отмечены значительные различия в продроматах (). Большинство пациентов сообщали об утомляемости и глубоком истощении, а также головокружении в начале приступа.
ТАБЛИЦА 2.
Клинические симптомы у 25 пациентов с синдромом системной капиллярной утечки
Семейный анамнез в основном не имел причин. У одного пациента с прогрессированием заболевания до множественной миеломы (ММ) был брат или сестра, которые умерли от ММ в возрасте 44 лет. Кроме того, новорожденный пациента с SCLS умер от кардиореспираторной дисфункции на фоне глубокой гипотензии, гемоконцентрации и лейкоцитоза на 17-й день жизни. Патологоанатомические исследования наводили на мысль о SCLS. Однако электронная микроскопия не показала расширения межклеточных промежутков эндотелиальных клеток.
В периоды покоя между приступами результаты физикального обследования были практически ничем не примечательными, за исключением 2 пациентов с хроническим SCLS, у которых был прогрессирующий генерализованный отек с плевральными и перикардиальными выпотами. Остаточное повреждение как следствие компартмент-синдрома или инсульта во время предыдущего приступа было отмечено у нескольких пациентов (). Резкое снижение артериального давления наблюдалось у всех пациентов в кризисной ситуации. Среднее систолическое артериальное давление, доступное для 16 пациентов (64%), составило 72 мм рт. Ст. (IQR, 57.0-90,5 мм рт. Ст.) Во время приступа.
ТАБЛИЦА 3.
Частота осложнений у 25 пациентов с синдромом системной капиллярной утечки
Рабдомиолиз, диагностированный по повышенному уровню креатинкиназы в соответствующих клинических условиях, был отмечен у 9 пациентов (36%) во время как минимум 1 приступа, у 5 пациентов (20%) развивается компартмент-синдром. Большинству пациентов с компартмент-синдромом (60%) потребовалась фасциотомия. Тест суммы рангов Вилкоксона, сравнивающий распределение альбумина у пациентов с рабдомиолизом и без рабдомиолиза, предполагает, что чем больше разница в альбумине от исходного уровня до приступа, тем выше вероятность ассоциированного рабдомиолиз ( P =.03; ). Однако никакой связи между рабдомиолизом и изменением концентрации гематокрита не наблюдалось ( P = 0,73).
Разница в альбумине (от исходного уровня до атаки) и развитие рабдомиолиза. Степень снижения альбумина во время приступа коррелирует с развитием рабдомиолиза.
Два пациента поступили с тампонадой сердца, потребовавшей срочного перикардиоцентеза с последующей установкой перикардиального окна. Отек легких во время фазы набора — ятрогенное осложнение лечения SCLS, которое возникает в результате нормализации проницаемости капилляров во время фазы выздоровления болезни в условиях продолжающейся интенсивной жидкостной реанимации. 5,20 Заболевание развилось у 10 (40%) пациентов, некоторым из которых потребовалась ИВЛ.
Результаты лабораторных исследований
У всех пациентов было документально подтвержденное повышение концентрации гематокрита во время приступа (). В среднее абсолютное увеличение гематокрита составило 19,8% (IQR, 14,8–28,0%) от исходного уровня (знаковый ранговый критерий Вилкоксона, P <0,001). Лейкоцитоз наблюдался у 36% пациентов, отклонение, которое, наряду с сопутствующим повышением концентрации гемоглобина, привело к неправильной диагностике истинной полицитемии у 12% пациентов.Ни в одном случае не было обнаружено никаких доказательств эозинофилии, кардинального проявления синдрома Глейха или тромбоцитоза.
ТАБЛИЦА 4.
Лабораторные значения на исходном уровне и во время приступов у пациентов с синдромом системной капиллярной утечки a, b
Приступы характеризовались значительным снижением альбумина (среднее снижение 1,9 г / дл; IQR 1,0 -2,2 г / дл; знаковый ранговый критерий Уилкоксона, P <0,001;). Белок М был обнаружен в исследованиях электрофореза / иммунофиксации белков сыворотки у 19 пациентов (76%) и имел тип IgG у всех, кроме 1 пациента.Почти три четверти преобладающих легких цепей относились к подтипу κ. Уровень М-белка был классически низким (медиана 0,6 г / дл; IQR 0-1,1 г / дл). Компонент М в моче был обнаружен примерно у трети (n = 7) из 23 обследованных пациентов.
Из 18 пациентов, перенесших биопсию костного мозга (BM) во время курса SCLS, 9 (50%) имели доказательства пролиферации моноклональных плазматических клеток (PC). У одного пациента было от 5% до 10% атипичных клональных ПК на аспирате BM, несмотря на неопределяемый сывороточный белок М, и молекулярно-генетические исследования с использованием праймеров полимеразной цепной реакции IgH выявили перестройки генов IgH.Другой пациент имел эозинофильную гиперплазию в BM без эозинофилии периферической крови. Только у 2 пациентов при последующем наблюдении было 10% или более ПК костного мозга.
У 20 пациентов, прошедших тестирование на эстеразу комплемента 1 (антиген и функция), отсутствие низких значений у всех пациентов исключило наследственный ангионевротический отек, что необходимо учитывать при дифференциальной диагностике SCLS. 21,22 Уровни C3 и C4 были низкими у 28% и 22%, соответственно, из 18 протестированных пациентов. У одного пациента был низкий общий гемолитический комплемент.
У двенадцати пациентов развилась острая почечная недостаточность со средним увеличением креатинина на 1 мг / дл (IQR, 0,55–3,4 мг / дл). Острая почечная недостаточность определялась как абсолютное повышение креатинина на 0,3 мг / дл или значение на 50% выше исходного уровня или снижение диуреза до менее 0,5 мл / кг / ч в течение более 6 часов, проявляющееся в течение 48 часов. появления симптомов. Двум пациентам временно потребовался гемодиализ.
Последующее наблюдение
Среднее время наблюдения за живыми пациентами составляло 4.9 лет (IQR, 3,2-8,5 года). После 17,0 лет тщательного наблюдения прогрессирование до ММ произошло у 1 пациента с исходным уровнем IgG-κ M-спайком 1,05 г / дл. У этого пациента был брат или сестра, которому в возрасте 44 лет был поставлен диагноз ММ. Прогресс к ММ ознаменовался резким увеличением белка М до 2,2 г / дл и протеинурией Бенс-Джонса наряду с острой почечной недостаточностью и анемией. Флуоресцентная гибридизация in situ позволила идентифицировать гипердиплоидный клон ПК. Пациент умер в течение 2 месяцев после прогрессирования до ММ.У другого пациента с 25-летней историей моноклональной гаммопатии неопределенного значения (MGUS) были результаты биопсии BM, указывающие на амилоидоз AL с BMPC от 10% до 15%. При поступлении у нее рецидивирующий SCLS превратился в хроническую форму с постоянными излияниями, требующими нескольких торакоцентеза и перикардиоцентеза. Сердечный амилоидоз также мог способствовать появлению ее симптомов; однако, прежде чем этот диагноз мог быть окончательно установлен с помощью эндомиокардиальной биопсии, пациент умер.Вскрытие не проводилось.
Лечение, ответ и выживаемость
Терапевтическое вмешательство было зарегистрировано для всех 25 пациентов. Наиболее частым первым выбором для долгосрочной профилактической терапии был метилксантин (теофиллин или аминофиллин) у 23 пациентов (92%), а также β-агонист тербуталин у 21 пациента (84%). Ингибитор лейкотриена применяли у 10 пациентов (40%). Эти пациенты часто не проявляли значимого ответа или непереносимости терапии первой линии.
У 4-летнего пациента терапия монтелукастом заметно снизила частоту и тяжесть приступов.Комбинация зафирлукаста и ингибитора ангиотензинпревращающего фермента лизиноприла позволила достичь большей глубины ответа у 2 пациентов.
Как немедленное, так и долгосрочное лечение SCLS включало противовоспалительную терапию у некоторых пациентов, включая использование преднизона у 12 пациентов (48%) и индометацина у 1 (4%).
Успешное ведение тяжелых острых приступов включало разумное использование кристаллоидных / коллоидных расширителей объема и мочегонных средств. Кроме того, у 1 пациента были применены адреналин и плазмаферез с исчезновением симптомов.В целом побочные эффекты терапии были сообщили 11 пациентов (44%) и были преимущественно симпатомиметиками, связанными с использованием β-агонистов. Один пациент умер от инфекционных осложнений длительной терапии кортикостероидами.
Мы разработали новый набор критериев, чтобы обеспечить единообразие в определении клинических исходов пациентов в наших ретроспективных анализах. Легкие, самоограничивающиеся эпизоды не требовали госпитализации, тогда как приступы средней и тяжелой степени требовали стационарного наблюдения или госпитализации с внутривенной инфузионной инфузией и часто требовали интенсивной терапии.Эти критерии помогли объективно оценить и сравнить влияние терапевтического вмешательства (). Пациенты, которые достигли 100% -ного отсутствия приступов в течение 2 лет и более, были классифицированы как пациенты, у которых был ответ Mayo Clinic (MC) 100. Пациенты, достигшие 50% или более снижения частоты и / или тяжести приступов, были классифицированы как достигшие ответа MC50.
ТАБЛИЦА 5.
Долгосрочный ответ у 25 исследуемых пациентов
Диапазон терапии для 6 пациентов в группе MC100 варьировался.Примечательно, что 2 пациента, которые остаются в группе MC100, на момент постановки диагноза находились в педиатрической возрастной группе. Один взрослый пациент остался на терапии MC100 без поддерживающая терапия, в то время как другие поддерживали длительную терапию MC100 с продолжающейся терапией на момент последнего наблюдения.
Информация о выживаемости была доступна для 24 пациентов, за которыми наблюдали в общей сложности 140 человеко-лет. Было зарегистрировано девять смертей. Было отмечено неуклонное снижение выживаемости в течение первых 5 лет после постановки диагноза, за которым последовало очевидное плато от 6 до 12 лет.Прогресс до ММ произошел у 1 пациента. Скорость перехода к ММ на человеко-год наблюдения составила 0,7%. Признавая ограниченное наблюдение за выжившими пациентами на момент проведения этого анализа и тот факт, что это заболевание имеет длительное клиническое течение (т. Е. Пациенты живы в течение длительного периода), мы сообщаем о 1, 5 и 10 случаях. оценки за год вместе с 95% доверительными интервалами (ДИ). Расчетные показатели ОВ через 1, 5 и 10 лет составляли 96% (95% ДИ, 87% -100%), 76% (95% ДИ, 59% -97%) и 68% (95% ДИ, 87% -100%) % ДИ, 49% -94%), соответственно ().
Кривая Каплана-Мейера общей выживаемости пациентов с синдромом идиопатической системной утечки капилляров. вертикальные линии на графике обозначают цензоры.
Дифференциальный диагноз
Посещения нескольких узких специалистов предшествовали однозначному установлению диагноза SCLS в этой когорте. Из-за совпадения множества клинических и лабораторных характеристик с другими заболеваниями, SCLS считается диагнозом исключения (). Интересно, что 12% пациентов были направлены для дальнейшего обследования и лечения неправильно диагностированной истинной полицитемии, что является важным фактором при дифференциальной диагностике SCLS. 23 Две трети этих пациентов перенесли флеботомию в других учреждениях, несмотря на нормальный уровень эритропоэтина в сыворотке крови.
ТАБЛИЦА 6.
Дифференциальный диагноз, рассмотренный у 25 исследуемых пациентов с синдромом системной капиллярной утечки
ОБСУЖДЕНИЕ
Патогенез SCLS остается неясным. Были задействованы цитокины, лейкотриены, фактор роста эндотелия сосудов (VEGF) и комплемент. Во время эпизодов повышенной проницаемости было отмечено значительное увеличение количества М-клеток периферической крови, положительных по рецептору интерлейкина 2. 24 Белки с массой до 900 кДа могут экстравазировать, но точная причина повышенной проницаемости остается неизвестной. Формирование эндотелиального микровезикулярного тела и пузырьков во время приступов свидетельствует об эндотелиальном апоптозе; однако попытки напрямую связать белок М с повреждением эндотелия оказались безуспешными. 25,26 Появление этого синдрома у 17-дневного младенца в нашей серии исследований предполагает возможность внутриутробного переноса растворимых медиаторов или наследственное заболевание.
В нашу когорту вошли только пациенты, у которых были спонтанные приступы без четкой этиологии. Другой термин, вторичный SCLS , был придуман для обозначения подобных приступов генерализованной гиперпроницаемости сосудов, при которых известен причинный фактор SCLS. Фактор некроза опухоли, интерферон-α и β, ацитретин, эпопростенол, гемцитабин, интерлейкин 2, денилейкин дифтитокс и филграстим вовлечены во вторичный SCLS. 27-31 Гепатит С и злокачественные новообразования также были зарегистрированы как этиологические факторы, но ни один из пациентов в нашей когорте не имел таких заболеваний одновременно во время первоначальной оценки. 32-35
Сходства в распределении по возрасту и полу были отмечены между нашей когортой и группой Amoura et al. 19 Плохая представленность афроамериканцев, вероятно, была отражением предвзятого отношения к специалистам. На данный момент зарегистрировано лишь несколько случаев в детской возрастной группе, и наше исследование добавляет еще 2, что свидетельствует о редкости этого заболевания у детей. 36-39
Чтобы повысить осведомленность об этом заболевании, недавно в базу данных Национальной организации редких заболеваний был добавлен отчет о SCLS.Веб-сайт поддержки пациентов (http://www.rareshare.org) также включает SCLS. Увеличение числа зарегистрированных случаев SCLS за последнее десятилетие, возможно, можно объяснить большей осведомленностью клиницистов, а не увеличением его заболеваемости. 3
Как подчеркивается во многих иллюстративных случаях, отсроченная постановка диагноза и неправильный диагноз увеличивают заболеваемость пациентов и могут отрицательно повлиять на исход. Длительное время задержки (в среднем 13,5 месяцев) между появлением симптомов и постановкой правильного диагноза было примечательным открытием в нашем исследовании.
Мы использовали строгие критерии для определения пациентов с SCLS в этой серии. Сосуществование MGUS, предупреждающие знаки, триггерные факторы, олигурия с началом приступа, отек легких и полиурия в фазе рекрутмента с последующим спонтанным исчезновением симптомов являются типичными признаками, но не являются обязательными для постановки официального диагноза.
Хотя большинство пациентов могли распознать начало приступа из-за рецидива симптомов и аналогичных, если не идентичных, триггерных факторов, тяжесть приступа была менее предсказуемой, поэтому для пациента было важно незамедлительно обратиться за неотложной помощью в отделение начало приступа независимо от его степени тяжести.
За исключением единичного случая, когда новорожденный у пациента с SCLS, семейный анамнез не имел никакого отношения, и это открытие хорошо согласуется с предыдущими сообщениями. Частота приступов варьировалась в широких пределах. Как и в ранее описанном случае, у подгруппы пациентов (8%) была диагностирована хроническая повышенная проницаемость, характеризующаяся стабильным артериальным давлением, стойким отеком (хотя и в меньшей степени между острыми обострениями) и, иногда, серозными излияниями. 40
У пациентки Кларксон была установлена четкая временная связь с менструальным циклом.В нашей серии только у 1 пациентки были кризы, связанные с менструацией, и, в отличие от предыдущих отчетов, приступов в послеродовом периоде не наблюдалось. 41
Сохранение мышления — не редкость во время атаки SCLS. В этой серии только у 2 пациентов возникли судороги во время криза, у 1 из которых был отек мозга, что хорошо задокументировано в SCLS. 42 Гипоперфузия головного мозга у 1 пациента привела к инсульту. Острая почечная недостаточность, отмечаемая почти у половины пациентов, является частым осложнением и следствием снижения перфузии почек, вызванного гипотензией, острого канальцевого некроза и пигментурии, связанной с рабдомиолизом. 43-45 Терапия по спасению тканей (декомпрессия) потребовалась 3 из 5 пациентов, у которых развился компартмент-синдром, серьезное осложнение SCLS из-за массивной утечки жидкости в мышечные ткани. 46-48 Острый тромбоз глубоких вен, который произошел у 8% пациентов, возможно, был вызван атакой активации компонентов триады Вирхова.
Обнаружение белка М у большинства пациентов (n = 19; 76%) может быть связано с предвзятостью отбора пациентов, направленных в нашу клинику диспротеинемии.Однако результаты аналогичны результатам французского исследования Amoura et al., 19 , в котором во всех 13 случаях сообщалось о MGUS (11 случаев типа κ), и последующем обзоре, в котором 39 из 50 случаев имели MGUS (28 из них). тип κ). 3 Важно повторить, что отсутствие M-шипа не исключает SCLS. 49,50 В отличие от других расстройств ПК, таких как синдром POEMS ( p олинейропатия, o rganomegaly, e эндокринопатия, m оноклональная гаммопатия и s изменения кинов), который почти всегда связан с IgG -λ или IgA-λ и синдром Шницлера (хроническая крапивница, моноклональная гаммопатия, лихорадка, артралгия, боль в костях и лимфаденопатия), который связан с моноклональной гаммапатией IgM, пациенты с болезнью Кларксона преимущественно имеют IgG-κ или IgA-κ. моноклональная гаммопатия. 51,52 В отличие от синдромов Шницлера и POEMS, компонент M не является основным критерием, необходимым для диагностики SCLS. 51,52
Сообщалось о развитии MM, лейкемии плазматических клеток и, в редких случаях, системного амилоидоза. 2,6,53 В нашей когорте скорость трансформации составила 0,7% на человеко-год наблюдения, что сопоставимо с 1% в год, зарегистрированным в MGUS. 54 Поэтому необходимо наблюдение за MM. Повторяемость (или тяжесть) приступов не коррелировала с размером М-спайка.
Это расстройство, особенно непредсказуемость повторяющихся опасных для жизни эпизодов, а также побочных эффектов лечения, сказалось на эмоциональном состоянии большинства пациентов, некоторые из которых также проявляли явные признаки большой депрессии.
Многому можно научиться, разграничивая отдельные «фазы» атаки. Во время начальной фазы утечки осторожное увеличение объема и мониторинг центрального венозного давления могут помочь в поддержании адекватной перфузии жизненно важных органов. 18 Чрезмерно агрессивная гидратация может вызвать отек легких.Терапия кортикостероидами может быть полезной во время приступа 16,33,55 , потому что замешано цитокин-опосредованное повреждение эндотелия. 56 Кроме того, плазмаферез 16,19,57,58 и внутривенное введение гамма-глобулина 19,50,59 оказались успешными в острой фазе. В нашем исследовании 1 пациент получил внутривенный иммуноглобулин в стороннем учреждении из-за дефицита IgG2 до того, как был установлен диагноз SCLS, и только 1 пациент прошел плазмаферез.
На сегодняшний день профилактика, опосредованная тербуталином и аминофиллином 17 , которая увеличивает циклический аденозинмонофосфат или ингибирует внутриклеточный путь киназы Rho 60 , оказала наибольшее влияние на поддержание периодов покоя. 18 Недавно были использованы верапамил, 49 ингибиторов лейкотриена, 61,62 иммуноадсорбции, 61 и талидомид (который, возможно, действует посредством ингибирования фактора некроза опухоли α в М-клетках) 57 .Также используются эндотелиальные мишени, такие как VEGF. Терапия с использованием моноклональных антител, таких как бевацизумаб (анти-VEGF) и инфликсимаб (противоопухолевый фактор некроза α), использовалась с переменным успехом. 63,64 По сообщениям, введение антимиеломной терапии у пациентов с SCLS и сопутствующей ММ снизило последующие приступы SCLS. 19 Однако это наблюдение не могло быть подтверждено в нашей когорте, потому что единственный пациент с SCLS и MM умер вскоре после того, как последний был поставлен диагноз.
Пятилетняя выживаемость в 76% в нашей когорте отражает улучшение смертности по сравнению с предыдущими исследованиями, 16,19 , но фактор, который больше всего способствует этому улучшенному результату, окончательно не определен.
Ограничения при изучении естественного течения и клинического течения редкого заболевания хорошо известны. Наше исследование имеет обычные ограничения ретроспективного анализа отобранных пациентов из центра третичной медицинской помощи с ограниченным последующим наблюдением.
Синдром идиопатической системной капиллярной утечки (болезнь Кларксона): опыт клиники Мэйо
Резюме
ЦЕЛЬ: Определить клинические особенности, естественный анамнез и исход четко определенной когорты из 25 последовательных пациентов с синдромом идиопатической системной капиллярной утечки ( SCLS) оценивается в центре третичной медицинской помощи.
ПАЦИЕНТЫ И МЕТОДЫ: Были проанализированы записи пациентов с диагнозом SCLS с 1 ноября 1981 г. по 30 апреля 2008 г. Описательная статистика использовалась для анализа демографических данных пациентов, клинических особенностей, осложнений и терапевтических вмешательств.
РЕЗУЛЬТАТЫ: Из 34 пациентов, чьи записи были проанализированы, 25 соответствовали всем диагностическим критериям SCLS. Средний возраст постановки диагноза SCLS составлял 44 года. Среднее время наблюдения за выжившими пациентами составило 4,9 года, а среднее время до постановки диагноза с момента появления симптомов — 1.1 год (межквартильный размах 0,5-4,1 года). О гриппе или миалгии сообщили 14 пациентов (56%) в начале острого приступа SCLS, а рабдомиолиз развился у 9 пациентов (36%). Пациенты с более сильным снижением уровня альбумина имели более высокую вероятность развития рабдомиолиза ( p = 0,03). Моноклональная гаммапатия, преимущественно IgG-κ-типа, была обнаружена у 19 пациентов (76%). Частота прогрессирования множественной миеломы составила 0,7% на человеко-год наблюдения. Общий ответ на различные методы лечения составил 76%, и у 24% пациентов сохранялась стойкая (> 2 лет) полная ремиссия.Расчетная 5-летняя общая выживаемость составила 76% (95% доверительный интервал, 59% -97%).
ЗАКЛЮЧЕНИЕ: Синдром системной утечки капилляров, редкое заболевание, которое встречается у людей среднего возраста, обычно диагностируется после значительной задержки с момента появления симптомов. Степень снижения альбумина во время приступа коррелирует с развитием рабдомиолиза. Снижение частоты и / или тяжести приступов наблюдалось почти у трех четвертей пациентов, которым было предложено эмпирическое лечение.Скорость прогрессирования множественной миеломы сравнима с таковой при моноклональной гаммопатии неустановленного значения.
BM = костный мозг; IQR = межквартильный размах; MGUS = моноклональная гаммопатия неопределенного значения; ММ = множественная миелома; ОС = общая выживаемость; ПК = плазматическая ячейка; SCLS = синдром системной утечки капилляров; VEGF = фактор роста эндотелия сосудов
Синдром идиопатической системной утечки капилляров (SCLS), также известный как болезнь Кларксона и спонтанный периодический отек , является потенциально фатальным заболеванием, характеризующимся стереотипными «атаками» различной интенсивности гиповолемического шока и генерализованный отек в сочетании с гемоконцентрацией (обнаруживаемой по повышенному гематокриту) и гипоальбуминемией, обычно возникающий при отсутствии альбуминурии. 1 Присутствие сывороточного белка М, примечательного признака, является единственной существенной лабораторной аномалией во время фазы покоя между приступами. 2 Хотя точная частота этого заболевания неизвестна, за последние 15 лет был отмечен относительный всплеск числа зарегистрированных случаев, возможно, в результате повышения осведомленности и успешной идентификации пациентов с множеством сложных симптомов и лабораторных исследований. это может быть объединено общим диагнозом идиопатический SCLS. 3,4 Хотя первоначальные сообщения были получены в Соединенных Штатах и Европе, позже случаи заболевания были зарегистрированы по всему миру, включая Индию, Японию и Кувейт. 5-8
Цели нашего исследования состояли в том, чтобы определить клинические особенности, естественное течение и исход четко определенной когорты последовательных пациентов с SCLS и сравнить наши результаты с данными ранее описанных случаев и небольших ретроспективных исследований. .
Путь от первого описания группы симптомов у пациентки до их формального признания клиническим синдромом системной капиллярной утечки поучителен и заслуживает обсуждения.В 1960 году Кларксон и др. 9 описали случай 32-летней женщины с ничем не примечательным семейным анамнезом, которая пережила «странное циклическое заболевание, при котором у нее периодически возникали внезапные массивные движения плазмы из ее сосудистого русла». Заболевание характеризовалось повторяющимися эпизодами отека, гиповолемического шока, гипоальбуминемии, гемоконцентрации и сохранения М-белка в сыворотке крови. 9 За этим первым описанием SCLS через 2 года последовал другой случай 29-летнего мужчины с эпизодами отека, увеличения веса, крапивницы, лихорадки и недомогания, в дополнение к повышенным уровням гамма-глобулина в сыворотке крови, спленомегалией. , и выраженная эозинофилия (50% -70%). 10 Хотя первоначально этот пациент считался похожим на индексный случай, у этого пациента отсутствовала характерная гипотензия, и в конечном итоге у него был диагностирован эпизодический ангионевротический отек с эозинофилией, теперь известный как синдром Глейха . 11,12
Год спустя (1963) И. Вайнбрен 13 предложил термин спонтанный периодический отек вместо циклический отек для этого синдрома у 45-летнего англичанина с повторяющимися приступами отека. это «… развивалось быстро: в течение нескольких часов он почувствовал себя плохо, почувствовал сильную жажду и отвращение к еде.Эти атаки были сопоставимы с теми, что описаны в первоначальном случае Кларксона. Четыре года спустя, в 1967 году, Мелвин Хорвит, один из приглашенных соавторов отчета об индексном случае, написал еще один отчет о фатальном гиповолемическом шоке неизвестной этиологии, в котором результаты вскрытия предполагали диффузный интерстициальный отек, отек легких и серозные выделения. 14 В течение следующих двух десятилетий в медицинской литературе появилось еще только 20 случаев. 15,16
В 1992 и 1999 годах в 2 небольших сериях случаев из нашего учреждения сообщалось об эффективности тербуталина и аминофиллина при лечении этого заболевания. 17,18 В 1997 году более крупное многоцентровое ретроспективное исследование Amoura et al. 19 описало течение SCLS и оценило эффективность доступной терапии в когорте из 13 пациентов.
ПАЦИЕНТЫ И МЕТОДЫ
С одобрения Институционального наблюдательного совета Mayo Clinic, записи всех пациентов, осмотренных в Mayo Clinic в Рочестере, штат Миннесота, с 1 ноября 1981 года по 30 апреля 2008 года с диагнозом SCLS, гиперпроницаемость капилляров. , Болезнь Кларксона и ангионевротический отек с гипоальбуминемией.Диагноз SCLS был основан на недвусмысленных документах о повторяющихся приступах гипотензии, повышенных концентрациях гематокрита, периферических отеках и гипоальбуминемии без альбуминурии. Моноклональная гаммопатия не считалась обязательным критерием, но ее одновременное наличие усиливало диагноз. Пациенты, физические признаки, симптомы и результаты лабораторных исследований которых могут быть объяснены альтернативным диагнозом, исключались, если этот альтернативный диагноз подтверждался дальнейшими исследованиями.
Были включены отчеты лабораторных исследований, полученные во время первого прототипного «приступа» и / или в течение 30 дней после контакта с пациентом. Большинство пациентов лечились в других медицинских центрах; с их согласия данные были извлечены из задокументированных записей направляющих учреждений. Были получены данные последующего наблюдения, и было предпринято как минимум 2 попытки связаться с выжившими пациентами по телефону. Когда это было возможно, пытались определить причину смерти. В рамках ретроспективного обзора мы попытались классифицировать исход болезни в нашей когорте.
Статистический анализ
Описательная статистика и простые графики разброса использовались для анализа демографических данных пациентов, клинических особенностей, осложнений и терапевтических вмешательств. Общая выживаемость (ОС) оценивалась по методу Каплана-Мейера и определялась как время от даты постановки диагноза до смерти или последнего наблюдения. Пациенты, жившие на момент последнего зарегистрированного наблюдения, были подвергнуты цензуре. Знаковые ранговые тесты Вилкоксона использовались для проверки изменений лабораторных параметров во время атаки относительно исходного уровня, а тесты суммы рангов Вилкоксона использовались для проверки связи между изменениями альбумина и концентрацией гематокрита во время приступа относительно исходного уровня и развитием клинических проявлений. осложнения.Все тесты были двусторонними, и все анализы проводились с использованием программного обеспечения SAS, версия 9.1 (Институт SAS, Кэри, Северная Каролина).
РЕЗУЛЬТАТЫ
Из 34 пациентов, чьи записи были проанализированы, 25 соответствовали всем диагностическим критериям SCLS. очерчивает демографический профиль исследуемой когорты. Среднее время между появлением симптомов и окончательным диагнозом составляло 1,1 года (межквартильный размах [IQR], 0,5–4,1 года). У 3 пациентов официальный диагноз был поставлен более чем через 5 лет после появления симптомов (через 5 лет).5, 8,0 и 32,0 года). Среднее количество острых приступов в год составило 3 (IQR, 0,5–5,0 приступов в год).
ТАБЛИЦА 1.
Демография исследуемых пациентов при диагностике SCLS a
Препятствующие факторы
Гриппоподобная болезнь или миалгии у большинства пациентов предвещали кризис, но были отмечены значительные различия в продроматах (). Большинство пациентов сообщали об утомляемости и глубоком истощении, а также головокружении в начале приступа.
ТАБЛИЦА 2.
Клинические симптомы у 25 пациентов с синдромом системной капиллярной утечки
Семейный анамнез в основном не имел причин. У одного пациента с прогрессированием заболевания до множественной миеломы (ММ) был брат или сестра, которые умерли от ММ в возрасте 44 лет. Кроме того, новорожденный пациента с SCLS умер от кардиореспираторной дисфункции на фоне глубокой гипотензии, гемоконцентрации и лейкоцитоза на 17-й день жизни. Патологоанатомические исследования наводили на мысль о SCLS. Однако электронная микроскопия не показала расширения межклеточных промежутков эндотелиальных клеток.
В периоды покоя между приступами результаты физикального обследования были практически ничем не примечательными, за исключением 2 пациентов с хроническим SCLS, у которых был прогрессирующий генерализованный отек с плевральными и перикардиальными выпотами. Остаточное повреждение как следствие компартмент-синдрома или инсульта во время предыдущего приступа было отмечено у нескольких пациентов (). Резкое снижение артериального давления наблюдалось у всех пациентов в кризисной ситуации. Среднее систолическое артериальное давление, доступное для 16 пациентов (64%), составило 72 мм рт. Ст. (IQR, 57.0-90,5 мм рт. Ст.) Во время приступа.
ТАБЛИЦА 3.
Частота осложнений у 25 пациентов с синдромом системной капиллярной утечки
Рабдомиолиз, диагностированный по повышенному уровню креатинкиназы в соответствующих клинических условиях, был отмечен у 9 пациентов (36%) во время как минимум 1 приступа, у 5 пациентов (20%) развивается компартмент-синдром. Большинству пациентов с компартмент-синдромом (60%) потребовалась фасциотомия. Тест суммы рангов Вилкоксона, сравнивающий распределение альбумина у пациентов с рабдомиолизом и без рабдомиолиза, предполагает, что чем больше разница в альбумине от исходного уровня до приступа, тем выше вероятность ассоциированного рабдомиолиз ( P =.03; ). Однако никакой связи между рабдомиолизом и изменением концентрации гематокрита не наблюдалось ( P = 0,73).
Разница в альбумине (от исходного уровня до атаки) и развитие рабдомиолиза. Степень снижения альбумина во время приступа коррелирует с развитием рабдомиолиза.
Два пациента поступили с тампонадой сердца, потребовавшей срочного перикардиоцентеза с последующей установкой перикардиального окна. Отек легких во время фазы набора — ятрогенное осложнение лечения SCLS, которое возникает в результате нормализации проницаемости капилляров во время фазы выздоровления болезни в условиях продолжающейся интенсивной жидкостной реанимации. 5,20 Заболевание развилось у 10 (40%) пациентов, некоторым из которых потребовалась ИВЛ.
Результаты лабораторных исследований
У всех пациентов было документально подтвержденное повышение концентрации гематокрита во время приступа (). В среднее абсолютное увеличение гематокрита составило 19,8% (IQR, 14,8–28,0%) от исходного уровня (знаковый ранговый критерий Вилкоксона, P <0,001). Лейкоцитоз наблюдался у 36% пациентов, отклонение, которое, наряду с сопутствующим повышением концентрации гемоглобина, привело к неправильной диагностике истинной полицитемии у 12% пациентов.Ни в одном случае не было обнаружено никаких доказательств эозинофилии, кардинального проявления синдрома Глейха или тромбоцитоза.
ТАБЛИЦА 4.
Лабораторные значения на исходном уровне и во время приступов у пациентов с синдромом системной капиллярной утечки a, b
Приступы характеризовались значительным снижением альбумина (среднее снижение 1,9 г / дл; IQR 1,0 -2,2 г / дл; знаковый ранговый критерий Уилкоксона, P <0,001;). Белок М был обнаружен в исследованиях электрофореза / иммунофиксации белков сыворотки у 19 пациентов (76%) и имел тип IgG у всех, кроме 1 пациента.Почти три четверти преобладающих легких цепей относились к подтипу κ. Уровень М-белка был классически низким (медиана 0,6 г / дл; IQR 0-1,1 г / дл). Компонент М в моче был обнаружен примерно у трети (n = 7) из 23 обследованных пациентов.
Из 18 пациентов, перенесших биопсию костного мозга (BM) во время курса SCLS, 9 (50%) имели доказательства пролиферации моноклональных плазматических клеток (PC). У одного пациента было от 5% до 10% атипичных клональных ПК на аспирате BM, несмотря на неопределяемый сывороточный белок М, и молекулярно-генетические исследования с использованием праймеров полимеразной цепной реакции IgH выявили перестройки генов IgH.Другой пациент имел эозинофильную гиперплазию в BM без эозинофилии периферической крови. Только у 2 пациентов при последующем наблюдении было 10% или более ПК костного мозга.
У 20 пациентов, прошедших тестирование на эстеразу комплемента 1 (антиген и функция), отсутствие низких значений у всех пациентов исключило наследственный ангионевротический отек, что необходимо учитывать при дифференциальной диагностике SCLS. 21,22 Уровни C3 и C4 были низкими у 28% и 22%, соответственно, из 18 протестированных пациентов. У одного пациента был низкий общий гемолитический комплемент.
У двенадцати пациентов развилась острая почечная недостаточность со средним увеличением креатинина на 1 мг / дл (IQR, 0,55–3,4 мг / дл). Острая почечная недостаточность определялась как абсолютное повышение креатинина на 0,3 мг / дл или значение на 50% выше исходного уровня или снижение диуреза до менее 0,5 мл / кг / ч в течение более 6 часов, проявляющееся в течение 48 часов. появления симптомов. Двум пациентам временно потребовался гемодиализ.
Последующее наблюдение
Среднее время наблюдения за живыми пациентами составляло 4.9 лет (IQR, 3,2-8,5 года). После 17,0 лет тщательного наблюдения прогрессирование до ММ произошло у 1 пациента с исходным уровнем IgG-κ M-спайком 1,05 г / дл. У этого пациента был брат или сестра, которому в возрасте 44 лет был поставлен диагноз ММ. Прогресс к ММ ознаменовался резким увеличением белка М до 2,2 г / дл и протеинурией Бенс-Джонса наряду с острой почечной недостаточностью и анемией. Флуоресцентная гибридизация in situ позволила идентифицировать гипердиплоидный клон ПК. Пациент умер в течение 2 месяцев после прогрессирования до ММ.У другого пациента с 25-летней историей моноклональной гаммопатии неопределенного значения (MGUS) были результаты биопсии BM, указывающие на амилоидоз AL с BMPC от 10% до 15%. При поступлении у нее рецидивирующий SCLS превратился в хроническую форму с постоянными излияниями, требующими нескольких торакоцентеза и перикардиоцентеза. Сердечный амилоидоз также мог способствовать появлению ее симптомов; однако, прежде чем этот диагноз мог быть окончательно установлен с помощью эндомиокардиальной биопсии, пациент умер.Вскрытие не проводилось.
Лечение, ответ и выживаемость
Терапевтическое вмешательство было зарегистрировано для всех 25 пациентов. Наиболее частым первым выбором для долгосрочной профилактической терапии был метилксантин (теофиллин или аминофиллин) у 23 пациентов (92%), а также β-агонист тербуталин у 21 пациента (84%). Ингибитор лейкотриена применяли у 10 пациентов (40%). Эти пациенты часто не проявляли значимого ответа или непереносимости терапии первой линии.
У 4-летнего пациента терапия монтелукастом заметно снизила частоту и тяжесть приступов.Комбинация зафирлукаста и ингибитора ангиотензинпревращающего фермента лизиноприла позволила достичь большей глубины ответа у 2 пациентов.
Как немедленное, так и долгосрочное лечение SCLS включало противовоспалительную терапию у некоторых пациентов, включая использование преднизона у 12 пациентов (48%) и индометацина у 1 (4%).
Успешное ведение тяжелых острых приступов включало разумное использование кристаллоидных / коллоидных расширителей объема и мочегонных средств. Кроме того, у 1 пациента были применены адреналин и плазмаферез с исчезновением симптомов.В целом побочные эффекты терапии были сообщили 11 пациентов (44%) и были преимущественно симпатомиметиками, связанными с использованием β-агонистов. Один пациент умер от инфекционных осложнений длительной терапии кортикостероидами.
Мы разработали новый набор критериев, чтобы обеспечить единообразие в определении клинических исходов пациентов в наших ретроспективных анализах. Легкие, самоограничивающиеся эпизоды не требовали госпитализации, тогда как приступы средней и тяжелой степени требовали стационарного наблюдения или госпитализации с внутривенной инфузионной инфузией и часто требовали интенсивной терапии.Эти критерии помогли объективно оценить и сравнить влияние терапевтического вмешательства (). Пациенты, которые достигли 100% -ного отсутствия приступов в течение 2 лет и более, были классифицированы как пациенты, у которых был ответ Mayo Clinic (MC) 100. Пациенты, достигшие 50% или более снижения частоты и / или тяжести приступов, были классифицированы как достигшие ответа MC50.
ТАБЛИЦА 5.
Долгосрочный ответ у 25 исследуемых пациентов
Диапазон терапии для 6 пациентов в группе MC100 варьировался.Примечательно, что 2 пациента, которые остаются в группе MC100, на момент постановки диагноза находились в педиатрической возрастной группе. Один взрослый пациент остался на терапии MC100 без поддерживающая терапия, в то время как другие поддерживали длительную терапию MC100 с продолжающейся терапией на момент последнего наблюдения.
Информация о выживаемости была доступна для 24 пациентов, за которыми наблюдали в общей сложности 140 человеко-лет. Было зарегистрировано девять смертей. Было отмечено неуклонное снижение выживаемости в течение первых 5 лет после постановки диагноза, за которым последовало очевидное плато от 6 до 12 лет.Прогресс до ММ произошел у 1 пациента. Скорость перехода к ММ на человеко-год наблюдения составила 0,7%. Признавая ограниченное наблюдение за выжившими пациентами на момент проведения этого анализа и тот факт, что это заболевание имеет длительное клиническое течение (т. Е. Пациенты живы в течение длительного периода), мы сообщаем о 1, 5 и 10 случаях. оценки за год вместе с 95% доверительными интервалами (ДИ). Расчетные показатели ОВ через 1, 5 и 10 лет составляли 96% (95% ДИ, 87% -100%), 76% (95% ДИ, 59% -97%) и 68% (95% ДИ, 87% -100%) % ДИ, 49% -94%), соответственно ().
Кривая Каплана-Мейера общей выживаемости пациентов с синдромом идиопатической системной утечки капилляров. вертикальные линии на графике обозначают цензоры.
Дифференциальный диагноз
Посещения нескольких узких специалистов предшествовали однозначному установлению диагноза SCLS в этой когорте. Из-за совпадения множества клинических и лабораторных характеристик с другими заболеваниями, SCLS считается диагнозом исключения (). Интересно, что 12% пациентов были направлены для дальнейшего обследования и лечения неправильно диагностированной истинной полицитемии, что является важным фактором при дифференциальной диагностике SCLS. 23 Две трети этих пациентов перенесли флеботомию в других учреждениях, несмотря на нормальный уровень эритропоэтина в сыворотке крови.
ТАБЛИЦА 6.
Дифференциальный диагноз, рассмотренный у 25 исследуемых пациентов с синдромом системной капиллярной утечки
ОБСУЖДЕНИЕ
Патогенез SCLS остается неясным. Были задействованы цитокины, лейкотриены, фактор роста эндотелия сосудов (VEGF) и комплемент. Во время эпизодов повышенной проницаемости было отмечено значительное увеличение количества М-клеток периферической крови, положительных по рецептору интерлейкина 2. 24 Белки с массой до 900 кДа могут экстравазировать, но точная причина повышенной проницаемости остается неизвестной. Формирование эндотелиального микровезикулярного тела и пузырьков во время приступов свидетельствует об эндотелиальном апоптозе; однако попытки напрямую связать белок М с повреждением эндотелия оказались безуспешными. 25,26 Появление этого синдрома у 17-дневного младенца в нашей серии исследований предполагает возможность внутриутробного переноса растворимых медиаторов или наследственное заболевание.
В нашу когорту вошли только пациенты, у которых были спонтанные приступы без четкой этиологии. Другой термин, вторичный SCLS , был придуман для обозначения подобных приступов генерализованной гиперпроницаемости сосудов, при которых известен причинный фактор SCLS. Фактор некроза опухоли, интерферон-α и β, ацитретин, эпопростенол, гемцитабин, интерлейкин 2, денилейкин дифтитокс и филграстим вовлечены во вторичный SCLS. 27-31 Гепатит С и злокачественные новообразования также были зарегистрированы как этиологические факторы, но ни один из пациентов в нашей когорте не имел таких заболеваний одновременно во время первоначальной оценки. 32-35
Сходства в распределении по возрасту и полу были отмечены между нашей когортой и группой Amoura et al. 19 Плохая представленность афроамериканцев, вероятно, была отражением предвзятого отношения к специалистам. На данный момент зарегистрировано лишь несколько случаев в детской возрастной группе, и наше исследование добавляет еще 2, что свидетельствует о редкости этого заболевания у детей. 36-39
Чтобы повысить осведомленность об этом заболевании, недавно в базу данных Национальной организации редких заболеваний был добавлен отчет о SCLS.Веб-сайт поддержки пациентов (http://www.rareshare.org) также включает SCLS. Увеличение числа зарегистрированных случаев SCLS за последнее десятилетие, возможно, можно объяснить большей осведомленностью клиницистов, а не увеличением его заболеваемости. 3
Как подчеркивается во многих иллюстративных случаях, отсроченная постановка диагноза и неправильный диагноз увеличивают заболеваемость пациентов и могут отрицательно повлиять на исход. Длительное время задержки (в среднем 13,5 месяцев) между появлением симптомов и постановкой правильного диагноза было примечательным открытием в нашем исследовании.
Мы использовали строгие критерии для определения пациентов с SCLS в этой серии. Сосуществование MGUS, предупреждающие знаки, триггерные факторы, олигурия с началом приступа, отек легких и полиурия в фазе рекрутмента с последующим спонтанным исчезновением симптомов являются типичными признаками, но не являются обязательными для постановки официального диагноза.
Хотя большинство пациентов могли распознать начало приступа из-за рецидива симптомов и аналогичных, если не идентичных, триггерных факторов, тяжесть приступа была менее предсказуемой, поэтому для пациента было важно незамедлительно обратиться за неотложной помощью в отделение начало приступа независимо от его степени тяжести.
За исключением единичного случая, когда новорожденный у пациента с SCLS, семейный анамнез не имел никакого отношения, и это открытие хорошо согласуется с предыдущими сообщениями. Частота приступов варьировалась в широких пределах. Как и в ранее описанном случае, у подгруппы пациентов (8%) была диагностирована хроническая повышенная проницаемость, характеризующаяся стабильным артериальным давлением, стойким отеком (хотя и в меньшей степени между острыми обострениями) и, иногда, серозными излияниями. 40
У пациентки Кларксон была установлена четкая временная связь с менструальным циклом.В нашей серии только у 1 пациентки были кризы, связанные с менструацией, и, в отличие от предыдущих отчетов, приступов в послеродовом периоде не наблюдалось. 41
Сохранение мышления — не редкость во время атаки SCLS. В этой серии только у 2 пациентов возникли судороги во время криза, у 1 из которых был отек мозга, что хорошо задокументировано в SCLS. 42 Гипоперфузия головного мозга у 1 пациента привела к инсульту. Острая почечная недостаточность, отмечаемая почти у половины пациентов, является частым осложнением и следствием снижения перфузии почек, вызванного гипотензией, острого канальцевого некроза и пигментурии, связанной с рабдомиолизом. 43-45 Терапия по спасению тканей (декомпрессия) потребовалась 3 из 5 пациентов, у которых развился компартмент-синдром, серьезное осложнение SCLS из-за массивной утечки жидкости в мышечные ткани. 46-48 Острый тромбоз глубоких вен, который произошел у 8% пациентов, возможно, был вызван атакой активации компонентов триады Вирхова.
Обнаружение белка М у большинства пациентов (n = 19; 76%) может быть связано с предвзятостью отбора пациентов, направленных в нашу клинику диспротеинемии.Однако результаты аналогичны результатам французского исследования Amoura et al., 19 , в котором во всех 13 случаях сообщалось о MGUS (11 случаев типа κ), и последующем обзоре, в котором 39 из 50 случаев имели MGUS (28 из них). тип κ). 3 Важно повторить, что отсутствие M-шипа не исключает SCLS. 49,50 В отличие от других расстройств ПК, таких как синдром POEMS ( p олинейропатия, o rganomegaly, e эндокринопатия, m оноклональная гаммопатия и s изменения кинов), который почти всегда связан с IgG -λ или IgA-λ и синдром Шницлера (хроническая крапивница, моноклональная гаммопатия, лихорадка, артралгия, боль в костях и лимфаденопатия), который связан с моноклональной гаммапатией IgM, пациенты с болезнью Кларксона преимущественно имеют IgG-κ или IgA-κ. моноклональная гаммопатия. 51,52 В отличие от синдромов Шницлера и POEMS, компонент M не является основным критерием, необходимым для диагностики SCLS. 51,52
Сообщалось о развитии MM, лейкемии плазматических клеток и, в редких случаях, системного амилоидоза. 2,6,53 В нашей когорте скорость трансформации составила 0,7% на человеко-год наблюдения, что сопоставимо с 1% в год, зарегистрированным в MGUS. 54 Поэтому необходимо наблюдение за MM. Повторяемость (или тяжесть) приступов не коррелировала с размером М-спайка.
Это расстройство, особенно непредсказуемость повторяющихся опасных для жизни эпизодов, а также побочных эффектов лечения, сказалось на эмоциональном состоянии большинства пациентов, некоторые из которых также проявляли явные признаки большой депрессии.
Многому можно научиться, разграничивая отдельные «фазы» атаки. Во время начальной фазы утечки осторожное увеличение объема и мониторинг центрального венозного давления могут помочь в поддержании адекватной перфузии жизненно важных органов. 18 Чрезмерно агрессивная гидратация может вызвать отек легких.Терапия кортикостероидами может быть полезной во время приступа 16,33,55 , потому что замешано цитокин-опосредованное повреждение эндотелия. 56 Кроме того, плазмаферез 16,19,57,58 и внутривенное введение гамма-глобулина 19,50,59 оказались успешными в острой фазе. В нашем исследовании 1 пациент получил внутривенный иммуноглобулин в стороннем учреждении из-за дефицита IgG2 до того, как был установлен диагноз SCLS, и только 1 пациент прошел плазмаферез.
На сегодняшний день профилактика, опосредованная тербуталином и аминофиллином 17 , которая увеличивает циклический аденозинмонофосфат или ингибирует внутриклеточный путь киназы Rho 60 , оказала наибольшее влияние на поддержание периодов покоя. 18 Недавно были использованы верапамил, 49 ингибиторов лейкотриена, 61,62 иммуноадсорбции, 61 и талидомид (который, возможно, действует посредством ингибирования фактора некроза опухоли α в М-клетках) 57 .Также используются эндотелиальные мишени, такие как VEGF. Терапия с использованием моноклональных антител, таких как бевацизумаб (анти-VEGF) и инфликсимаб (противоопухолевый фактор некроза α), использовалась с переменным успехом. 63,64 По сообщениям, введение антимиеломной терапии у пациентов с SCLS и сопутствующей ММ снизило последующие приступы SCLS. 19 Однако это наблюдение не могло быть подтверждено в нашей когорте, потому что единственный пациент с SCLS и MM умер вскоре после того, как последний был поставлен диагноз.
Пятилетняя выживаемость в 76% в нашей когорте отражает улучшение смертности по сравнению с предыдущими исследованиями, 16,19 , но фактор, который больше всего способствует этому улучшенному результату, окончательно не определен.
Ограничения при изучении естественного течения и клинического течения редкого заболевания хорошо известны. Наше исследование имеет обычные ограничения ретроспективного анализа отобранных пациентов из центра третичной медицинской помощи с ограниченным последующим наблюдением.
Синдром идиопатической системной капиллярной утечки (болезнь Кларксона): опыт клиники Мэйо
Резюме
ЦЕЛЬ: Определить клинические особенности, естественный анамнез и исход четко определенной когорты из 25 последовательных пациентов с синдромом идиопатической системной капиллярной утечки ( SCLS) оценивается в центре третичной медицинской помощи.
ПАЦИЕНТЫ И МЕТОДЫ: Были проанализированы записи пациентов с диагнозом SCLS с 1 ноября 1981 г. по 30 апреля 2008 г. Описательная статистика использовалась для анализа демографических данных пациентов, клинических особенностей, осложнений и терапевтических вмешательств.
РЕЗУЛЬТАТЫ: Из 34 пациентов, чьи записи были проанализированы, 25 соответствовали всем диагностическим критериям SCLS. Средний возраст постановки диагноза SCLS составлял 44 года. Среднее время наблюдения за выжившими пациентами составило 4,9 года, а среднее время до постановки диагноза с момента появления симптомов — 1.1 год (межквартильный размах 0,5-4,1 года). О гриппе или миалгии сообщили 14 пациентов (56%) в начале острого приступа SCLS, а рабдомиолиз развился у 9 пациентов (36%). Пациенты с более сильным снижением уровня альбумина имели более высокую вероятность развития рабдомиолиза ( p = 0,03). Моноклональная гаммапатия, преимущественно IgG-κ-типа, была обнаружена у 19 пациентов (76%). Частота прогрессирования множественной миеломы составила 0,7% на человеко-год наблюдения. Общий ответ на различные методы лечения составил 76%, и у 24% пациентов сохранялась стойкая (> 2 лет) полная ремиссия.Расчетная 5-летняя общая выживаемость составила 76% (95% доверительный интервал, 59% -97%).
ЗАКЛЮЧЕНИЕ: Синдром системной утечки капилляров, редкое заболевание, которое встречается у людей среднего возраста, обычно диагностируется после значительной задержки с момента появления симптомов. Степень снижения альбумина во время приступа коррелирует с развитием рабдомиолиза. Снижение частоты и / или тяжести приступов наблюдалось почти у трех четвертей пациентов, которым было предложено эмпирическое лечение.Скорость прогрессирования множественной миеломы сравнима с таковой при моноклональной гаммопатии неустановленного значения.
BM = костный мозг; IQR = межквартильный размах; MGUS = моноклональная гаммопатия неопределенного значения; ММ = множественная миелома; ОС = общая выживаемость; ПК = плазматическая ячейка; SCLS = синдром системной утечки капилляров; VEGF = фактор роста эндотелия сосудов
Синдром идиопатической системной утечки капилляров (SCLS), также известный как болезнь Кларксона и спонтанный периодический отек , является потенциально фатальным заболеванием, характеризующимся стереотипными «атаками» различной интенсивности гиповолемического шока и генерализованный отек в сочетании с гемоконцентрацией (обнаруживаемой по повышенному гематокриту) и гипоальбуминемией, обычно возникающий при отсутствии альбуминурии. 1 Присутствие сывороточного белка М, примечательного признака, является единственной существенной лабораторной аномалией во время фазы покоя между приступами. 2 Хотя точная частота этого заболевания неизвестна, за последние 15 лет был отмечен относительный всплеск числа зарегистрированных случаев, возможно, в результате повышения осведомленности и успешной идентификации пациентов с множеством сложных симптомов и лабораторных исследований. это может быть объединено общим диагнозом идиопатический SCLS. 3,4 Хотя первоначальные сообщения были получены в Соединенных Штатах и Европе, позже случаи заболевания были зарегистрированы по всему миру, включая Индию, Японию и Кувейт. 5-8
Цели нашего исследования состояли в том, чтобы определить клинические особенности, естественное течение и исход четко определенной когорты последовательных пациентов с SCLS и сравнить наши результаты с данными ранее описанных случаев и небольших ретроспективных исследований. .
Путь от первого описания группы симптомов у пациентки до их формального признания клиническим синдромом системной капиллярной утечки поучителен и заслуживает обсуждения.В 1960 году Кларксон и др. 9 описали случай 32-летней женщины с ничем не примечательным семейным анамнезом, которая пережила «странное циклическое заболевание, при котором у нее периодически возникали внезапные массивные движения плазмы из ее сосудистого русла». Заболевание характеризовалось повторяющимися эпизодами отека, гиповолемического шока, гипоальбуминемии, гемоконцентрации и сохранения М-белка в сыворотке крови. 9 За этим первым описанием SCLS через 2 года последовал другой случай 29-летнего мужчины с эпизодами отека, увеличения веса, крапивницы, лихорадки и недомогания, в дополнение к повышенным уровням гамма-глобулина в сыворотке крови, спленомегалией. , и выраженная эозинофилия (50% -70%). 10 Хотя первоначально этот пациент считался похожим на индексный случай, у этого пациента отсутствовала характерная гипотензия, и в конечном итоге у него был диагностирован эпизодический ангионевротический отек с эозинофилией, теперь известный как синдром Глейха . 11,12
Год спустя (1963) И. Вайнбрен 13 предложил термин спонтанный периодический отек вместо циклический отек для этого синдрома у 45-летнего англичанина с повторяющимися приступами отека. это «… развивалось быстро: в течение нескольких часов он почувствовал себя плохо, почувствовал сильную жажду и отвращение к еде.Эти атаки были сопоставимы с теми, что описаны в первоначальном случае Кларксона. Четыре года спустя, в 1967 году, Мелвин Хорвит, один из приглашенных соавторов отчета об индексном случае, написал еще один отчет о фатальном гиповолемическом шоке неизвестной этиологии, в котором результаты вскрытия предполагали диффузный интерстициальный отек, отек легких и серозные выделения. 14 В течение следующих двух десятилетий в медицинской литературе появилось еще только 20 случаев. 15,16
В 1992 и 1999 годах в 2 небольших сериях случаев из нашего учреждения сообщалось об эффективности тербуталина и аминофиллина при лечении этого заболевания. 17,18 В 1997 году более крупное многоцентровое ретроспективное исследование Amoura et al. 19 описало течение SCLS и оценило эффективность доступной терапии в когорте из 13 пациентов.
ПАЦИЕНТЫ И МЕТОДЫ
С одобрения Институционального наблюдательного совета Mayo Clinic, записи всех пациентов, осмотренных в Mayo Clinic в Рочестере, штат Миннесота, с 1 ноября 1981 года по 30 апреля 2008 года с диагнозом SCLS, гиперпроницаемость капилляров. , Болезнь Кларксона и ангионевротический отек с гипоальбуминемией.Диагноз SCLS был основан на недвусмысленных документах о повторяющихся приступах гипотензии, повышенных концентрациях гематокрита, периферических отеках и гипоальбуминемии без альбуминурии. Моноклональная гаммопатия не считалась обязательным критерием, но ее одновременное наличие усиливало диагноз. Пациенты, физические признаки, симптомы и результаты лабораторных исследований которых могут быть объяснены альтернативным диагнозом, исключались, если этот альтернативный диагноз подтверждался дальнейшими исследованиями.
Были включены отчеты лабораторных исследований, полученные во время первого прототипного «приступа» и / или в течение 30 дней после контакта с пациентом. Большинство пациентов лечились в других медицинских центрах; с их согласия данные были извлечены из задокументированных записей направляющих учреждений. Были получены данные последующего наблюдения, и было предпринято как минимум 2 попытки связаться с выжившими пациентами по телефону. Когда это было возможно, пытались определить причину смерти. В рамках ретроспективного обзора мы попытались классифицировать исход болезни в нашей когорте.
Статистический анализ
Описательная статистика и простые графики разброса использовались для анализа демографических данных пациентов, клинических особенностей, осложнений и терапевтических вмешательств. Общая выживаемость (ОС) оценивалась по методу Каплана-Мейера и определялась как время от даты постановки диагноза до смерти или последнего наблюдения. Пациенты, жившие на момент последнего зарегистрированного наблюдения, были подвергнуты цензуре. Знаковые ранговые тесты Вилкоксона использовались для проверки изменений лабораторных параметров во время атаки относительно исходного уровня, а тесты суммы рангов Вилкоксона использовались для проверки связи между изменениями альбумина и концентрацией гематокрита во время приступа относительно исходного уровня и развитием клинических проявлений. осложнения.Все тесты были двусторонними, и все анализы проводились с использованием программного обеспечения SAS, версия 9.1 (Институт SAS, Кэри, Северная Каролина).
РЕЗУЛЬТАТЫ
Из 34 пациентов, чьи записи были проанализированы, 25 соответствовали всем диагностическим критериям SCLS. очерчивает демографический профиль исследуемой когорты. Среднее время между появлением симптомов и окончательным диагнозом составляло 1,1 года (межквартильный размах [IQR], 0,5–4,1 года). У 3 пациентов официальный диагноз был поставлен более чем через 5 лет после появления симптомов (через 5 лет).5, 8,0 и 32,0 года). Среднее количество острых приступов в год составило 3 (IQR, 0,5–5,0 приступов в год).
ТАБЛИЦА 1.
Демография исследуемых пациентов при диагностике SCLS a
Препятствующие факторы
Гриппоподобная болезнь или миалгии у большинства пациентов предвещали кризис, но были отмечены значительные различия в продроматах (). Большинство пациентов сообщали об утомляемости и глубоком истощении, а также головокружении в начале приступа.
ТАБЛИЦА 2.
Клинические симптомы у 25 пациентов с синдромом системной капиллярной утечки
Семейный анамнез в основном не имел причин. У одного пациента с прогрессированием заболевания до множественной миеломы (ММ) был брат или сестра, которые умерли от ММ в возрасте 44 лет. Кроме того, новорожденный пациента с SCLS умер от кардиореспираторной дисфункции на фоне глубокой гипотензии, гемоконцентрации и лейкоцитоза на 17-й день жизни. Патологоанатомические исследования наводили на мысль о SCLS. Однако электронная микроскопия не показала расширения межклеточных промежутков эндотелиальных клеток.
В периоды покоя между приступами результаты физикального обследования были практически ничем не примечательными, за исключением 2 пациентов с хроническим SCLS, у которых был прогрессирующий генерализованный отек с плевральными и перикардиальными выпотами. Остаточное повреждение как следствие компартмент-синдрома или инсульта во время предыдущего приступа было отмечено у нескольких пациентов (). Резкое снижение артериального давления наблюдалось у всех пациентов в кризисной ситуации. Среднее систолическое артериальное давление, доступное для 16 пациентов (64%), составило 72 мм рт. Ст. (IQR, 57.0-90,5 мм рт. Ст.) Во время приступа.
ТАБЛИЦА 3.
Частота осложнений у 25 пациентов с синдромом системной капиллярной утечки
Рабдомиолиз, диагностированный по повышенному уровню креатинкиназы в соответствующих клинических условиях, был отмечен у 9 пациентов (36%) во время как минимум 1 приступа, у 5 пациентов (20%) развивается компартмент-синдром. Большинству пациентов с компартмент-синдромом (60%) потребовалась фасциотомия. Тест суммы рангов Вилкоксона, сравнивающий распределение альбумина у пациентов с рабдомиолизом и без рабдомиолиза, предполагает, что чем больше разница в альбумине от исходного уровня до приступа, тем выше вероятность ассоциированного рабдомиолиз ( P =.03; ). Однако никакой связи между рабдомиолизом и изменением концентрации гематокрита не наблюдалось ( P = 0,73).
Разница в альбумине (от исходного уровня до атаки) и развитие рабдомиолиза. Степень снижения альбумина во время приступа коррелирует с развитием рабдомиолиза.
Два пациента поступили с тампонадой сердца, потребовавшей срочного перикардиоцентеза с последующей установкой перикардиального окна. Отек легких во время фазы набора — ятрогенное осложнение лечения SCLS, которое возникает в результате нормализации проницаемости капилляров во время фазы выздоровления болезни в условиях продолжающейся интенсивной жидкостной реанимации. 5,20 Заболевание развилось у 10 (40%) пациентов, некоторым из которых потребовалась ИВЛ.
Результаты лабораторных исследований
У всех пациентов было документально подтвержденное повышение концентрации гематокрита во время приступа (). В среднее абсолютное увеличение гематокрита составило 19,8% (IQR, 14,8–28,0%) от исходного уровня (знаковый ранговый критерий Вилкоксона, P <0,001). Лейкоцитоз наблюдался у 36% пациентов, отклонение, которое, наряду с сопутствующим повышением концентрации гемоглобина, привело к неправильной диагностике истинной полицитемии у 12% пациентов.Ни в одном случае не было обнаружено никаких доказательств эозинофилии, кардинального проявления синдрома Глейха или тромбоцитоза.
ТАБЛИЦА 4.
Лабораторные значения на исходном уровне и во время приступов у пациентов с синдромом системной капиллярной утечки a, b
Приступы характеризовались значительным снижением альбумина (среднее снижение 1,9 г / дл; IQR 1,0 -2,2 г / дл; знаковый ранговый критерий Уилкоксона, P <0,001;). Белок М был обнаружен в исследованиях электрофореза / иммунофиксации белков сыворотки у 19 пациентов (76%) и имел тип IgG у всех, кроме 1 пациента.Почти три четверти преобладающих легких цепей относились к подтипу κ. Уровень М-белка был классически низким (медиана 0,6 г / дл; IQR 0-1,1 г / дл). Компонент М в моче был обнаружен примерно у трети (n = 7) из 23 обследованных пациентов.
Из 18 пациентов, перенесших биопсию костного мозга (BM) во время курса SCLS, 9 (50%) имели доказательства пролиферации моноклональных плазматических клеток (PC). У одного пациента было от 5% до 10% атипичных клональных ПК на аспирате BM, несмотря на неопределяемый сывороточный белок М, и молекулярно-генетические исследования с использованием праймеров полимеразной цепной реакции IgH выявили перестройки генов IgH.Другой пациент имел эозинофильную гиперплазию в BM без эозинофилии периферической крови. Только у 2 пациентов при последующем наблюдении было 10% или более ПК костного мозга.
У 20 пациентов, прошедших тестирование на эстеразу комплемента 1 (антиген и функция), отсутствие низких значений у всех пациентов исключило наследственный ангионевротический отек, что необходимо учитывать при дифференциальной диагностике SCLS. 21,22 Уровни C3 и C4 были низкими у 28% и 22%, соответственно, из 18 протестированных пациентов. У одного пациента был низкий общий гемолитический комплемент.
У двенадцати пациентов развилась острая почечная недостаточность со средним увеличением креатинина на 1 мг / дл (IQR, 0,55–3,4 мг / дл). Острая почечная недостаточность определялась как абсолютное повышение креатинина на 0,3 мг / дл или значение на 50% выше исходного уровня или снижение диуреза до менее 0,5 мл / кг / ч в течение более 6 часов, проявляющееся в течение 48 часов. появления симптомов. Двум пациентам временно потребовался гемодиализ.
Последующее наблюдение
Среднее время наблюдения за живыми пациентами составляло 4.9 лет (IQR, 3,2-8,5 года). После 17,0 лет тщательного наблюдения прогрессирование до ММ произошло у 1 пациента с исходным уровнем IgG-κ M-спайком 1,05 г / дл. У этого пациента был брат или сестра, которому в возрасте 44 лет был поставлен диагноз ММ. Прогресс к ММ ознаменовался резким увеличением белка М до 2,2 г / дл и протеинурией Бенс-Джонса наряду с острой почечной недостаточностью и анемией. Флуоресцентная гибридизация in situ позволила идентифицировать гипердиплоидный клон ПК. Пациент умер в течение 2 месяцев после прогрессирования до ММ.У другого пациента с 25-летней историей моноклональной гаммопатии неопределенного значения (MGUS) были результаты биопсии BM, указывающие на амилоидоз AL с BMPC от 10% до 15%. При поступлении у нее рецидивирующий SCLS превратился в хроническую форму с постоянными излияниями, требующими нескольких торакоцентеза и перикардиоцентеза. Сердечный амилоидоз также мог способствовать появлению ее симптомов; однако, прежде чем этот диагноз мог быть окончательно установлен с помощью эндомиокардиальной биопсии, пациент умер.Вскрытие не проводилось.
Лечение, ответ и выживаемость
Терапевтическое вмешательство было зарегистрировано для всех 25 пациентов. Наиболее частым первым выбором для долгосрочной профилактической терапии был метилксантин (теофиллин или аминофиллин) у 23 пациентов (92%), а также β-агонист тербуталин у 21 пациента (84%). Ингибитор лейкотриена применяли у 10 пациентов (40%). Эти пациенты часто не проявляли значимого ответа или непереносимости терапии первой линии.
У 4-летнего пациента терапия монтелукастом заметно снизила частоту и тяжесть приступов.Комбинация зафирлукаста и ингибитора ангиотензинпревращающего фермента лизиноприла позволила достичь большей глубины ответа у 2 пациентов.
Как немедленное, так и долгосрочное лечение SCLS включало противовоспалительную терапию у некоторых пациентов, включая использование преднизона у 12 пациентов (48%) и индометацина у 1 (4%).
Успешное ведение тяжелых острых приступов включало разумное использование кристаллоидных / коллоидных расширителей объема и мочегонных средств. Кроме того, у 1 пациента были применены адреналин и плазмаферез с исчезновением симптомов.В целом побочные эффекты терапии были сообщили 11 пациентов (44%) и были преимущественно симпатомиметиками, связанными с использованием β-агонистов. Один пациент умер от инфекционных осложнений длительной терапии кортикостероидами.
Мы разработали новый набор критериев, чтобы обеспечить единообразие в определении клинических исходов пациентов в наших ретроспективных анализах. Легкие, самоограничивающиеся эпизоды не требовали госпитализации, тогда как приступы средней и тяжелой степени требовали стационарного наблюдения или госпитализации с внутривенной инфузионной инфузией и часто требовали интенсивной терапии.Эти критерии помогли объективно оценить и сравнить влияние терапевтического вмешательства (). Пациенты, которые достигли 100% -ного отсутствия приступов в течение 2 лет и более, были классифицированы как пациенты, у которых был ответ Mayo Clinic (MC) 100. Пациенты, достигшие 50% или более снижения частоты и / или тяжести приступов, были классифицированы как достигшие ответа MC50.
ТАБЛИЦА 5.
Долгосрочный ответ у 25 исследуемых пациентов
Диапазон терапии для 6 пациентов в группе MC100 варьировался.Примечательно, что 2 пациента, которые остаются в группе MC100, на момент постановки диагноза находились в педиатрической возрастной группе. Один взрослый пациент остался на терапии MC100 без поддерживающая терапия, в то время как другие поддерживали длительную терапию MC100 с продолжающейся терапией на момент последнего наблюдения.
Информация о выживаемости была доступна для 24 пациентов, за которыми наблюдали в общей сложности 140 человеко-лет. Было зарегистрировано девять смертей. Было отмечено неуклонное снижение выживаемости в течение первых 5 лет после постановки диагноза, за которым последовало очевидное плато от 6 до 12 лет.Прогресс до ММ произошел у 1 пациента. Скорость перехода к ММ на человеко-год наблюдения составила 0,7%. Признавая ограниченное наблюдение за выжившими пациентами на момент проведения этого анализа и тот факт, что это заболевание имеет длительное клиническое течение (т. Е. Пациенты живы в течение длительного периода), мы сообщаем о 1, 5 и 10 случаях. оценки за год вместе с 95% доверительными интервалами (ДИ). Расчетные показатели ОВ через 1, 5 и 10 лет составляли 96% (95% ДИ, 87% -100%), 76% (95% ДИ, 59% -97%) и 68% (95% ДИ, 87% -100%) % ДИ, 49% -94%), соответственно ().
Кривая Каплана-Мейера общей выживаемости пациентов с синдромом идиопатической системной утечки капилляров. вертикальные линии на графике обозначают цензоры.
Дифференциальный диагноз
Посещения нескольких узких специалистов предшествовали однозначному установлению диагноза SCLS в этой когорте. Из-за совпадения множества клинических и лабораторных характеристик с другими заболеваниями, SCLS считается диагнозом исключения (). Интересно, что 12% пациентов были направлены для дальнейшего обследования и лечения неправильно диагностированной истинной полицитемии, что является важным фактором при дифференциальной диагностике SCLS. 23 Две трети этих пациентов перенесли флеботомию в других учреждениях, несмотря на нормальный уровень эритропоэтина в сыворотке крови.
ТАБЛИЦА 6.
Дифференциальный диагноз, рассмотренный у 25 исследуемых пациентов с синдромом системной капиллярной утечки
ОБСУЖДЕНИЕ
Патогенез SCLS остается неясным. Были задействованы цитокины, лейкотриены, фактор роста эндотелия сосудов (VEGF) и комплемент. Во время эпизодов повышенной проницаемости было отмечено значительное увеличение количества М-клеток периферической крови, положительных по рецептору интерлейкина 2. 24 Белки с массой до 900 кДа могут экстравазировать, но точная причина повышенной проницаемости остается неизвестной. Формирование эндотелиального микровезикулярного тела и пузырьков во время приступов свидетельствует об эндотелиальном апоптозе; однако попытки напрямую связать белок М с повреждением эндотелия оказались безуспешными. 25,26 Появление этого синдрома у 17-дневного младенца в нашей серии исследований предполагает возможность внутриутробного переноса растворимых медиаторов или наследственное заболевание.
В нашу когорту вошли только пациенты, у которых были спонтанные приступы без четкой этиологии. Другой термин, вторичный SCLS , был придуман для обозначения подобных приступов генерализованной гиперпроницаемости сосудов, при которых известен причинный фактор SCLS. Фактор некроза опухоли, интерферон-α и β, ацитретин, эпопростенол, гемцитабин, интерлейкин 2, денилейкин дифтитокс и филграстим вовлечены во вторичный SCLS. 27-31 Гепатит С и злокачественные новообразования также были зарегистрированы как этиологические факторы, но ни один из пациентов в нашей когорте не имел таких заболеваний одновременно во время первоначальной оценки. 32-35
Сходства в распределении по возрасту и полу были отмечены между нашей когортой и группой Amoura et al. 19 Плохая представленность афроамериканцев, вероятно, была отражением предвзятого отношения к специалистам. На данный момент зарегистрировано лишь несколько случаев в детской возрастной группе, и наше исследование добавляет еще 2, что свидетельствует о редкости этого заболевания у детей. 36-39
Чтобы повысить осведомленность об этом заболевании, недавно в базу данных Национальной организации редких заболеваний был добавлен отчет о SCLS.Веб-сайт поддержки пациентов (http://www.rareshare.org) также включает SCLS. Увеличение числа зарегистрированных случаев SCLS за последнее десятилетие, возможно, можно объяснить большей осведомленностью клиницистов, а не увеличением его заболеваемости. 3
Как подчеркивается во многих иллюстративных случаях, отсроченная постановка диагноза и неправильный диагноз увеличивают заболеваемость пациентов и могут отрицательно повлиять на исход. Длительное время задержки (в среднем 13,5 месяцев) между появлением симптомов и постановкой правильного диагноза было примечательным открытием в нашем исследовании.
Мы использовали строгие критерии для определения пациентов с SCLS в этой серии. Сосуществование MGUS, предупреждающие знаки, триггерные факторы, олигурия с началом приступа, отек легких и полиурия в фазе рекрутмента с последующим спонтанным исчезновением симптомов являются типичными признаками, но не являются обязательными для постановки официального диагноза.
Хотя большинство пациентов могли распознать начало приступа из-за рецидива симптомов и аналогичных, если не идентичных, триггерных факторов, тяжесть приступа была менее предсказуемой, поэтому для пациента было важно незамедлительно обратиться за неотложной помощью в отделение начало приступа независимо от его степени тяжести.
За исключением единичного случая, когда новорожденный у пациента с SCLS, семейный анамнез не имел никакого отношения, и это открытие хорошо согласуется с предыдущими сообщениями. Частота приступов варьировалась в широких пределах. Как и в ранее описанном случае, у подгруппы пациентов (8%) была диагностирована хроническая повышенная проницаемость, характеризующаяся стабильным артериальным давлением, стойким отеком (хотя и в меньшей степени между острыми обострениями) и, иногда, серозными излияниями. 40
У пациентки Кларксон была установлена четкая временная связь с менструальным циклом.В нашей серии только у 1 пациентки были кризы, связанные с менструацией, и, в отличие от предыдущих отчетов, приступов в послеродовом периоде не наблюдалось. 41
Сохранение мышления — не редкость во время атаки SCLS. В этой серии только у 2 пациентов возникли судороги во время криза, у 1 из которых был отек мозга, что хорошо задокументировано в SCLS. 42 Гипоперфузия головного мозга у 1 пациента привела к инсульту. Острая почечная недостаточность, отмечаемая почти у половины пациентов, является частым осложнением и следствием снижения перфузии почек, вызванного гипотензией, острого канальцевого некроза и пигментурии, связанной с рабдомиолизом. 43-45 Терапия по спасению тканей (декомпрессия) потребовалась 3 из 5 пациентов, у которых развился компартмент-синдром, серьезное осложнение SCLS из-за массивной утечки жидкости в мышечные ткани. 46-48 Острый тромбоз глубоких вен, который произошел у 8% пациентов, возможно, был вызван атакой активации компонентов триады Вирхова.
Обнаружение белка М у большинства пациентов (n = 19; 76%) может быть связано с предвзятостью отбора пациентов, направленных в нашу клинику диспротеинемии.Однако результаты аналогичны результатам французского исследования Amoura et al., 19 , в котором во всех 13 случаях сообщалось о MGUS (11 случаев типа κ), и последующем обзоре, в котором 39 из 50 случаев имели MGUS (28 из них). тип κ). 3 Важно повторить, что отсутствие M-шипа не исключает SCLS. 49,50 В отличие от других расстройств ПК, таких как синдром POEMS ( p олинейропатия, o rganomegaly, e эндокринопатия, m оноклональная гаммопатия и s изменения кинов), который почти всегда связан с IgG -λ или IgA-λ и синдром Шницлера (хроническая крапивница, моноклональная гаммопатия, лихорадка, артралгия, боль в костях и лимфаденопатия), который связан с моноклональной гаммапатией IgM, пациенты с болезнью Кларксона преимущественно имеют IgG-κ или IgA-κ. моноклональная гаммопатия. 51,52 В отличие от синдромов Шницлера и POEMS, компонент M не является основным критерием, необходимым для диагностики SCLS. 51,52
Сообщалось о развитии MM, лейкемии плазматических клеток и, в редких случаях, системного амилоидоза. 2,6,53 В нашей когорте скорость трансформации составила 0,7% на человеко-год наблюдения, что сопоставимо с 1% в год, зарегистрированным в MGUS. 54 Поэтому необходимо наблюдение за MM. Повторяемость (или тяжесть) приступов не коррелировала с размером М-спайка.
Это расстройство, особенно непредсказуемость повторяющихся опасных для жизни эпизодов, а также побочных эффектов лечения, сказалось на эмоциональном состоянии большинства пациентов, некоторые из которых также проявляли явные признаки большой депрессии.
Многому можно научиться, разграничивая отдельные «фазы» атаки. Во время начальной фазы утечки осторожное увеличение объема и мониторинг центрального венозного давления могут помочь в поддержании адекватной перфузии жизненно важных органов. 18 Чрезмерно агрессивная гидратация может вызвать отек легких.Терапия кортикостероидами может быть полезной во время приступа 16,33,55 , потому что замешано цитокин-опосредованное повреждение эндотелия. 56 Кроме того, плазмаферез 16,19,57,58 и внутривенное введение гамма-глобулина 19,50,59 оказались успешными в острой фазе. В нашем исследовании 1 пациент получил внутривенный иммуноглобулин в стороннем учреждении из-за дефицита IgG2 до того, как был установлен диагноз SCLS, и только 1 пациент прошел плазмаферез.
На сегодняшний день профилактика, опосредованная тербуталином и аминофиллином 17 , которая увеличивает циклический аденозинмонофосфат или ингибирует внутриклеточный путь киназы Rho 60 , оказала наибольшее влияние на поддержание периодов покоя. 18 Недавно были использованы верапамил, 49 ингибиторов лейкотриена, 61,62 иммуноадсорбции, 61 и талидомид (который, возможно, действует посредством ингибирования фактора некроза опухоли α в М-клетках) 57 .Также используются эндотелиальные мишени, такие как VEGF. Терапия с использованием моноклональных антител, таких как бевацизумаб (анти-VEGF) и инфликсимаб (противоопухолевый фактор некроза α), использовалась с переменным успехом. 63,64 По сообщениям, введение антимиеломной терапии у пациентов с SCLS и сопутствующей ММ снизило последующие приступы SCLS. 19 Однако это наблюдение не могло быть подтверждено в нашей когорте, потому что единственный пациент с SCLS и MM умер вскоре после того, как последний был поставлен диагноз.
Пятилетняя выживаемость в 76% в нашей когорте отражает улучшение смертности по сравнению с предыдущими исследованиями, 16,19 , но фактор, который больше всего способствует этому улучшенному результату, окончательно не определен.
Ограничения при изучении естественного течения и клинического течения редкого заболевания хорошо известны. Наше исследование имеет обычные ограничения ретроспективного анализа отобранных пациентов из центра третичной медицинской помощи с ограниченным последующим наблюдением.
Пурпура Геноха-Шенляйна — NORD (Национальная организация по редким заболеваниям)
Обычная пурпура — наиболее распространенный тип пурпуры, чаще всего встречающийся у женщин старше 50 лет.При отсутствии травмы поражения пурпурой возникают чаще, чем подкожные кровотечения. Однако после операции или даже незначительных травм хрупкость кровеносных сосудов приводит к чрезмерному кровотечению. Кровотечение можно уменьшить кратковременной терапией кортикостероидами и / или, у женщин в постменопаузе, введением эстрогена.
Цинга, разновидность пурпуры, возникает в результате дефицита витамина С в рационе. Симптомы могут включать общую слабость, анемию, губчатые десны и склонность к кровотечению (кровоизлиянию) под кожей (подкожно) и из нежных слизистых оболочек, выстилающих рот и желудочно-кишечный тракт.В современных цивилизациях цинга встречается редко из-за улучшения диеты и доступности продуктов, содержащих витамин С.
Синдром Гарденера-Даймонда (сенсибилизация аутоэритроцитов) — редкое заболевание, которое иногда называют синдромом болезненных синяков. Для него характерны пятна пурпуры, в основном у молодых женщин. Синдром Гарденера-Даймонда считается аутоиммунным заболеванием.
Васкулит (ангиит) — это воспалительное заболевание сосудов, которое может возникать само по себе или в сочетании с другими аллергическими или ревматическими заболеваниями.Воспаление стенок сосудов сужает кровеносные сосуды и может вызвать недостаток кровоснабжения определенных участков тела (ишемию), потерю тканей (некроз) и / или образование тромбов (тромбоз). Может быть поражен сосуд любого размера или любая часть сосудистой системы, и симптомы зависят от пораженной системы. Симптомы могут включать жар, головную боль, глубокую потерю аппетита, потерю веса, слабость, боль в животе, диарею и / или боль в мышцах и суставах. Поскольку существует множество форм васкулита, существует множество причин.Некоторые типы могут быть вызваны аллергическими реакциями или гиперчувствительностью к определенным лекарствам, таким как препараты серы, пенициллин, пропилтиоурацил, другие лекарства, токсины и другие вдыхаемые раздражители окружающей среды. Другие формы могут возникать из-за грибковой инфекции, паразитов или вирусных инфекций, в то время как в некоторых случаях очевидная причина может отсутствовать. (Для получения дополнительной информации об этом заболевании выберите «Васкулит» в качестве поискового запроса в базе данных редких заболеваний.)
Кожно-некротический васкулит — относительно частое воспалительное заболевание кровеносных сосудов, включая вены, артерии и более мелкие кровеносные сосуды ( капилляры).Это заболевание обычно поражает кожу и может возникать само по себе или в сочетании с аллергическими, инфекционными или ревматическими заболеваниями. Симптомы могут включать узелки на коже, небольшие кровоизлияния под кожей и / или поражения кожи, которые могут быть красными и плоскими (пятна). Они могут развиваться на многих частях тела, особенно на спине, руках, ягодицах и / или ногах. В некоторых случаях также могут присутствовать ульи с сильным зудом (крапивница) или кольцевидные язвы. Также могут возникать жар, общий дискомфорт (недомогание) и / или боль в мышцах или суставах.Точная причина кожно-некротического васкулита неизвестна. Некоторые поражения могут быть вызваны аллергической реакцией или гиперчувствительностью к определенным лекарствам, таким как сульфамид или пенициллин, другим лекарствам, токсинам и вдыхаемым раздражителям окружающей среды.
Болезнь Кавасаки — воспалительное заболевание детского возраста, характеризующееся лихорадкой, кожной сыпью, увеличением лимфатических узлов (лимфаденопатия), воспалением артерий (полиартериит) и воспалением кровеносных сосудов (васкулит). Воспалительные изменения вызывают деструктивные поражения кровеносных сосудов, что может привести к осложнениям, затрагивающим печень, желчный пузырь и сердце.Симптомы могут включать аномально высокую температуру, которая начинается внезапно и продолжается примерно две недели. Другие симптомы могут включать покраснение слизистой оболочки век обоих глаз (двусторонний конъюнктивит), раздражительность, усталость, покраснение (воспаление) рта и языка (стоматит), растрескивание губ, отек лимфатических узлов на шее ( шейная лимфаденопатия) и / или кожные высыпания. Точная причина болезни Кавасаки до конца не выяснена. Это может быть связано с двумя ранее неизвестными штаммами бактерий стафилококка и стрептококка и / или с возможной иммунологической аномалией.(Для получения дополнительной информации об этом заболевании выберите «Kawasaki» в качестве поискового запроса в базе данных редких заболеваний.)
Иммунная тромбоцитопения — редкое заболевание тромбоцитов, характеризующееся необъяснимым низким уровнем тромбоцитов в циркулирующей крови. Симптомы могут включать носовое кровотечение (носовое кровотечение), маленькие красные или пурпурные пятна на коже, которые представляют небольшие кровоизлияния под кожей (петехии), и / или кровотечение из прямой кишки и / или мочевыводящих путей. Может последовать анемия и вызвать слабость и утомляемость.У других людей с этим заболеванием могут наблюдаться эпизоды повышенной температуры и аномального увеличения селезенки. Специфической причины иммунной тромбоциопении не выявлено. Текущие данные подтверждают иммунологическую основу, поскольку у большинства пациентов обнаруживаются идентифицируемые антитромбоцитарные антитела. (Для получения дополнительной информации об этом заболевании выберите «Иммунная тромбоцитопения» в качестве поискового запроса в базе данных редких заболеваний.)
Тромботическая тромбоцитопеническая пурпура (ТТП) — редкое заболевание крови, характеризующееся аномально низким уровнем циркулирующих тромбоцитов в крови, аномальным разрушение эритроцитов, нарушение функции почек и нарушения нервной системы.Симптомы этого заболевания, которые начинаются внезапно, могут включать лихорадку, головную боль, пятна пурпуры на коже и слизистых оболочках, боль в суставах (артралгии), частичную потерю чувствительности в руках или ногах (парез), изменения психического статуса и / или или судороги. Точная причина ТТП неизвестна. Это может быть связано с инфекционным агентом или аутоиммунной реакцией. (Для получения дополнительной информации об этом заболевании выберите «Тромботическая тромбоцитопения пурпура» в качестве поискового запроса в базе данных редких заболеваний.)
Обнаружение отравления свинцом
Как обнаруживается отравление свинцом?
Отравление свинцом обычно обнаруживают путем измерения уровня в крови.Во многих процедурах скрининга капиллярная кровь используется в качестве тестирования в месте оказания медицинской помощи. В то время как пробы из пальца подходят для скрининговых тестов, все повышенные уровни в капиллярах должны подтверждаться взятием венозной крови, поскольку капиллярные тесты могут давать частые ложноположительные результаты. Повышенный уровень свинца в капиллярах указывает на то, что свинец присутствует в окружающей среде ребенка, даже если его уровень в венах низкий, поэтому следует начать первичную профилактику и просвещение.
Текущий график периодичности Bright Futures / AAP рекомендует проводить оценку риска при следующих посещениях здорового ребенка: 6 месяцев, 9 месяцев, 12 месяцев, 18 месяцев, 24 месяца и в возрасте 3, 4, 5 и 6 лет.Рекомендуется провести оценку риска , и сделать анализ уровня свинца в крови только в том случае, если оценка риска окажется положительной. Согласно AAP и CDC, универсальные скрининги или тесты на уровень свинца в крови больше не рекомендуются, за исключением районов с высокой распространенностью и повышенными факторами риска, как описано в отчете CDC за 2012 год, таких как старые дома.
Большинство первоначальных анализов уровня свинца в крови теперь проводится в результате положительной оценки риска или беспокойства родителей, а не потому, что у детей есть симптомы, указывающие на отравление свинцом.Однако дети всех возрастов, недавно иммигрировавшие, беженцы или усыновленные, с большей вероятностью имеют повышенный уровень свинца в крови, и их следует обследовать при первой же возможности. Кроме того, более высокому риску могут подвергаться дети, живущие в районах с более низким социально-экономическим положением.
Пациенты, соответствующие критериям программы Medicaid, также подвержены более высокому риску воздействия свинца, поскольку многие из них живут в этих районах с более низким социально-экономическим положением. Многие государственные программы Medicaid / раннего и периодического скрининга, диагностики и лечения требуют универсального анализа уровня свинца в крови при посещениях через 12 и 24 месяца, независимо от распространенности повышенных уровней в зависимости от таких факторов, как место проживания пациента.Хотя этим программам было предписано изменить свои требования, чтобы они больше соответствовали данным о распространенности (целевой скрининг), в большинстве штатов эти усилия не завершены. Для получения дополнительной информации см. Информационный бюллетень CMC HS, Планы целевого скрининга или Руководство CDC для государств, заинтересованных в переходе к целевому скринингу на содержание свинца в крови для детей, имеющих право на участие в программе Medicaid. Педиатры должны обратиться в офис Medicaid в своем штате, чтобы определить, каким требованиям они должны следовать, когда речь идет о пациентах, имеющих право на Medicaid.Эта информация доступна для большинства штатов на веб-сайте CDC. Однако педиатры могут ошибаться, проявляя осторожность, и определять уровень свинца у пациентов Medicaid и тех, кто, по их мнению, подвержен высокому риску.
Из-за воздействия свинца на развивающийся плод в некоторых штатах были разработаны рекомендации по скринингу свинца для беременных женщин. CDC недавно опубликовал руководство по скринингу беременных женщин на предмет содержания свинца, медицинскому контролю и охране окружающей среды, а также по наблюдению за матерями и младенцами, когда материнский уровень свинца составляет не менее 5 микрограммов на децилитр.Уход за младенцем включает измерение пуповины или неонатальной крови для определения исходного уровня. После рождения ребенка рекомендуется прекращать грудное вскармливание только в том случае, если уровень свинца в крови матери составляет 40 микрограммов на децилитр или более. Выше этого уровня женщины должны сцеживать молоко и отказываться от него до тех пор, пока уровень свинца в крови не упадет ниже этого ориентира.
Для семей, использующих водопроводную воду для восстановления детской смеси или сока, или в тех случаях, когда есть опасения на местном уровне, может быть рекомендовано тестирование водопроводной воды.Чтобы определить, может ли вода в доме содержать свинец, родители могут позвонить на горячую линию EPA по безопасной питьевой воде по телефону (800) 426-4791 или в местный отдел здравоохранения, чтобы узнать о тестировании воды. Колодезную воду следует проверять на содержание свинца, когда колодец новый, и проверять снова, когда беременная женщина, младенец или ребенок в возрасте до 18 лет переезжает в дом. Обсуждение использования колодезной воды для кормления младенцев см. В заявлении AAP о питьевой воде из частных колодцев. Большинство фильтров для воды удаляют свинец.
Когда требуется диагностическое тестирование?
Некоторые опытные врачи измеряют уровень свинца в крови у детей с задержкой роста, речевой или языковой дисфункцией, анемией, а также нарушениями внимания или поведения, особенно если у родителей есть особые опасения по поводу свинца или воздействия на здоровье химических веществ в окружающей среде. Однако повышенный уровень свинца в крови, который сохраняется в школе, является необычным, даже если пиковый уровень свинца в крови в возрасте 2 лет был высоким и воздействие на ребенка в домашних условиях не учитывалось.Таким образом, относительно низкий уровень свинца в крови ребенка школьного возраста не исключает более раннего отравления свинцом. Однако, если возникает вопрос об отравлении свинцом, единственный надежный способ поставить диагноз — это измерение содержания свинца в крови.

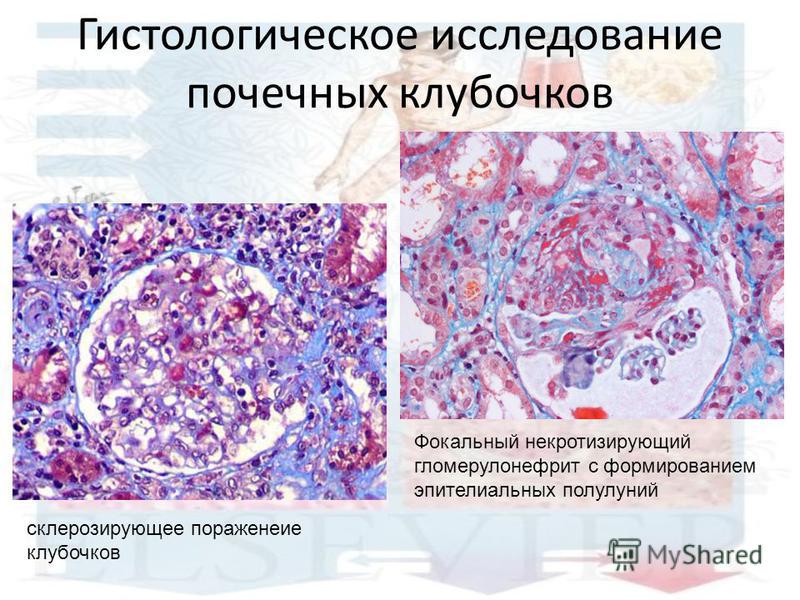

 : Геноха геморрагическая пурпура, капилляротоксикоз, пурпура анафилактическая, Шенлейна Геноха болезнь) аллергическая болезнь, характеризующаяся системным васкулитом и проявляющаяся симметричными, чаще… … Большой медицинский словарь
: Геноха геморрагическая пурпура, капилляротоксикоз, пурпура анафилактическая, Шенлейна Геноха болезнь) аллергическая болезнь, характеризующаяся системным васкулитом и проявляющаяся симметричными, чаще… … Большой медицинский словарь




 В некоторых случаях почки могут прекратить выполнять свои функции.
В некоторых случаях почки могут прекратить выполнять свои функции. При этой разновидности патологии высыпания на коже практически никогда не возникают.
При этой разновидности патологии высыпания на коже практически никогда не возникают.